|
The Korean text of this paper can be translated into multiple languages on the website of http://jksee.or.kr through Google Translator.
AbstractObjectivesRecently, energy-related research has shifted from developing alternative energy to the efficient management technology of the produced energy. As an alternative, research on phase change materials (PCMs) capable of absorbing and releasing heat as an energy medium has been conducted. This study developed a more efficient heat storage medium using activated carbon as a medium for the phase change material. At the same time, we developed a method for efficiently impregnating the phase change material into the activated carbon pores.
MethodsThe activated carbon used in this experiment was charcoal powder activated carbon (250-350 mesh) and granular activated carbon. The inorganic phase change materials used in the experiment was manganese nitrate hexahydrate. The method for impregnating the phase change material was pressurization method and dilution method. The heat absorption / emission capacity of the developed material was examined within the range of 10℃ to 50℃.
Results and DiscussionThe Scanning electron microscope (SEM) and Transmission electron microscopy energy-dispersive X-ray spectroscopy (TEM-EDX) analysis showed that the phase change material was filled in the pore of activated carbon. When the phase change material is filled by the pressurized method, the material properties of manganese nitrate hexahydrate are reflected, resulting in absorption and release of heat at each phase change temperature. As a result of experiments for the selection of the optimum solvent in the phase change material filling study using the dilution method, when ethanol was used as the solvent, the heat absorption was clearly observed even after the phase change material was loaded. As a result of selecting the optimal dilution ratio, the ratio of ethanol was determined to be 1:1 as the dilution ratio with the lowest amount of floating activated carbon. The optimal solvent removal method experimental results show that the heat absorption/release section occurred when the ethanol was removed by evaporation at 85℃ temperature.
Conclusions1) Both the pressurization method and the dilution method are filling methods in which inorganic phase change materials can be immobilized inside activated carbon, and heat absorption and release characteristics are maintained even after loading.
2) The heat absorption release was maintained for ethanol and the optimal dilution ratio was 1:1.
3) In case of the dilute solvent removal method, the heat absorption/release capacity was maintained when the solvent was removed using only the vaporization method.
요약목적최근 에너지 관련 연구는 대체에너지 개발에서 나아가, 생산된 에너지의 효율적 관리 기술 개발로 변화하고 있다. 이에 대해 에너지 저장 및 방출 기능을 가진 상전이 물질을 에너지 매체로 사용하는 연구가 꾸준히 진행되고 있다. 본 연구에서는 활성탄을 상전이 물질의 충진매체로 사용하여 보다 효율적인 열저장매체를 개발하고자 하며 동시에 활성탄 세공 내에 상전이 물질을 효율적으로 충진시키는 방법을 개발하고자 한다.
방법본 실험에 사용한 활성탄은 목탄계 분말 활성탄(250-350 mesh)과 입상활성탄을 이용하였으며 실험에 사용한 무기성 상전이 물질로는 Manganese nitrate hexahydrate을 사용하였다. 상전이 물질의 세공내 충진 방법은 가압방식과 희석방식을 이용하였으며 개발 소재의 열 흡수/방출 능력은 10-50℃ 범위 내의 온도에서 관찰하였다.
결과 및 토의가압식 및 희석식 충진 방법에 따른 상전이 물질의 활성탄 충진 여부는 SEM, TEM-EDX 및 bulk density 분석을 통해 확인하였다. 가압식 방법으로 상전이 물질을 충진 하였을 경우 Manganese nitrate hexahydrate의 물질 특성이 그대로 반영되어 각각의 상전이 온도에서 열의 흡수와 방출이 발생되어 온도변화가 지연되는 구간을 보였다. 희석 방식을 이용한 상전이 물질 충진연구에서 최적 용매 선정 실험결과 에탄올을 용매로 사용하였을 경우 상전이 물질 담지 후에도 열 흡수/방출이 뚜렷하게 관찰되었다. 최적 희석 배율 선정 실험을 통해 부유하는 활성탄이 가장 최소량에 되게 하면서 에탄올의 비율이 낮은 희석 비(1:1)를 도출하였다. 용매 제거 실험결과 85℃ 온도에서 기화하여 에탄올을 제거하였을 때의 조건이 최적으로 나타났으며, 온도변화에 따른 열 흡수/방출 특성을 평가한 결과 열 흡수/방출 현상이 관찰됨을 확인하였다.
1. 서 론전 세계적으로 과도한 화석에너지 소비에 의한 화석연료 고갈로 인해 새로운 대체 에너지 매체가 매우 필요한 실정이며, 이에 에너지 소비 및 대체에너지 개발의 관심이 증대되고 있다[1-3,24,25]. 화석에너지를 능가하는 새로운 에너지 매체의 불확실성으로 인해 최근 대체에너지(태양열, 풍력, 조력 등) 개발이 큰 화두가 되고 있으나[4-6], 이는 초기투자비용이 높고 대형 면적이 요구되며 동시에 자연 훼손의 문제 등 새로운 환경문제를 발생시키는 단점이 있다[7-9]. 이에 따라 에너지관련 기술은 사용 에너지의 절약 및 누수 에너지 방지에 초점을 둔 연구 개발로 점차 확대되고 있는데, 그 중에서도 특히 상전이 물질을 응용한 열 저장 시스템은 그 무공해성, 지속가능성, 높은열 저장 밀도로 에너지 활용에 관해 무한한 가능성을 갖는 것으로 평가된다[10,11,26,27].
상전이 물질(Phase change material, PCM)은 높은 잠열 용량을 갖고 있으며, 고체에서 액체, 액체에서 기체 등, 하나의 상태에서 또 다른 상태로 변하는 과정에서 열을 축적하거나 저장한 열을 방출하는 물질을 말한다[12]. 물질의 상 변화에 수반되는 잠열로 저장을 하면 열 저장매체의 부피와 그에 따른 공간이 매우 작아지고 일정한 온도에서 열을 방출 또는 흡수할 수 있는 장점이 있다[13,14]. PCM은 물질에 따라 상전이 온도와 용해열이 다르므로 사용 목적에 따라 활용한다면 에너지를 효율적으로 사용할 수 있으며 응용분야는 태양열 난방시스템, 직물, 단열재, 건축물 소재 분야 등과 같이 그 범위가 다양하다[15-18]. 또한 최근에는 활성탄에 상전이 물질을 도핑한 양극 촉매 물질을 미생물 전기화학 시스템 등에서 사용하고 있다[24-27].
특히 건축물 외벽을 이루는 조립식 벽체나 옥상 등에 채움제 또는 보강제로 적용할 경우 외부온도 변화에 따른 건물 내부 온도 변화를 최소화 하는 데 기여할 수 있으며 이는 건축물 냉난방 에너지 절감에 효과적이다[15,16]. PCM 물질은 크게 유기성과 무기성으로 나눌 수 있는데, 유기성 물질은 화학적으로 안정하나 비교적 비싼 편이며 무기성 물질 보다 잠열이 적다는 단점이 있다. 현재까지 유기성 상전이 물질을 소재로 합성하는 연구는 많이 되어 왔으나, 무기성 상전이 물질을 소재로 적용하기 위한 연구는 한정적이다[2,20]. 무기성 PCM 물질은 잠열과 열전도도가 높으나 소재로 적용될 시 상 변화 현상이 발생하여 PCM 물질의 누출이 발생될 수 있기 때문이다[20]. 따라서 상전이 물질의 누출을 방지할 수 있도록 Shell 물질로 캡슐화하는 연구가 활발히 수행되고 있으나, 캡슐화의 경우 상전이 물질이 캡슐 내부에 밀봉되어 있어 열전달 효율이 떨어진다는 단점이 있다[21-23]. 이에 본 연구는 무기성 PCM 물질을 다공성 물질의 세공 사이에 충진하여 PCM을 안정적으로 담지 할 수 있는 담지 기술을 개발하고자 한다. 또한 담지 기술에 따른 무기성 PCM/다공성 소재의 열 흡수/방출 특성 분석을 통해 무기성 PCM의 다공성 소재 내의 담지 안정성을 알아보았다.
2. 실험방법2.2. 무기성 상전이 물질의 활성탄 세공에 충진 방법2.2.1. 가압식본 연구에서는 두 가지 방법으로 상전이 물질을 활성탄 세공 내에 침지 하였다. 첫 번째는 고압을 가하여 충진 하는 방법(P-PIA)으로 액체상태의 상전이 물질과 활성탄을 혼합한 후 지속적으로 교반하여 혼합물 내에 기포가 관찰되지 않을 때까지 저속으로 교반하는 방법이다. 기포가 더 이상 발생되지 않은 활성탄 세공에 충진 된 상전이 물질(PCM/활성탄)을 압력용기에 넣고 압력용기 내부의 온도와 압력을 각각 50℃, 10 atm 으로 하여 48시간동안 유지하였다. 활성탄의 세공에 상전이 물질을 충진 하는 과정에서 온도를 50℃로 선정한 이유는 온도를 높임에 따라 상전이 물질의 점성이 낮아지므로 충진이 보다 용이해지며, 등온상태에서 일관된 흡착 반응을 기대할 수 있으므로 재현성을 확보할 수 있기 때문이다. PCM을 활성탄에 담지한 활성탄/PCM 혼합물을 필터링하여 분리한 후 에탄올을 이용하여 세공 내부에 충진 되지 않고 표면에 흡착된 상전이 물질을 세척하여 건조하였다.
2.2.2. 희석식두 번째 방법은 상전이 물질의 세공내 원활한 침투를 위하여 저점도성 용매로 희석한 후 상온에서 침지시키는 방법(D-V-PIA)이다. 에탄올을 용매로 사용하였으며, 상전이 물질과 1:1의 비율로 희석하였고 희석된 상전이 물질과 활성탄은 기포가 발생하지 않을 때까지 약 24시간동안 천천히 교반하였다. 교반 이후 세 가지 방법을 이용하여 희석된 에탄올을 제거하였다. 80℃ 온도로 기화하여 에탄올을 제거하는 방법(D-V-PIA), 동결건조기를 이용하여 에탄올을 제거하는 방법(D-F-PIA), 에탄올을 80℃에서 기화한 후 감압 펌프를 이용하여 에탄올을 제거하는 방법(D-D-PIA)을 사용하였다.
2.2.3. 활성탄 담지 상전이 물질의 특성평가온도측정장치는 상전이 물질이 충진 된 활성탄을 담는 유리 용기, 유리 용기의 바닥 면을 통한 1차원 열 흐름을 유도하기 위한 단열재, 충진 한 매체의 열의 흡수 및 방출을 측정하는 온도계측기, 온도조절챔버(TC-ME-065, JEIO TECH, Korea)로 구성되어 있다. 무기성 상전이 물질이 충진 된 활성탄을 유리용기에 압밀하여 30 mm 두께로 충진 하였으며 유리 용기는 외경이 30 mm, 높이 108 mm, 옆면 두께 1.2 mm, 밑면 두께 1 mm이다. 시료를 담은 유리 용기는 폴리우레탄폼 소재의 단열재로 감싸 유리용기 밑면을 통하여 열에너지가 이동하도록 유도하였다. 온도 측정 센서는 유리용기 바닥 면에서 1 cm 떨어진 지점에 위치하도록 하였다. 마지막으로 준비된 상전이 물질을 40 L 용량의 온도조절챔버에 넣어 외부 온도를 조절하였고 10초에 한 번씩 온도를 측정하였다. 활성탄 세공 내에 무기성 상전이 물질의 충진 여부를 정성적으로 파악하기 위하여 scanning electron microscope (SEM, Hitachi S-4800, Japan), 충진 된 활성탄의 단면에 대한 X-ray photoelectron spectroscopic (XPS, Thermoscientific K-α, USA), Transmission electron microscopy (TEM)과, Transmission electron microscopy energy-dispersive X-ray (TEM-EDS) mapping 분석을 하였다.
3. 결과 및 고찰3.1. 가압식 방법으로 제조된 PCM/활성탄의 열 흡수/방출 특성가압방식으로 활성탄 세공에 PCM을 주입한 PCM/활성탄의 온도변화에 따른 무게 손실 측정 결과, 약 4%의 무게 손실률을 나타내었으며 무게 손실이 거의 발생되지 않음을 확인하였다. Fig. 1은 PCM/활성탄 물질의 온도변화에 따른 열의 흡수 및 방출을 반복적으로 수행하여 나타낸 결과이다. 35℃의 상전이 온도를 갖는 Mn(NO3)2・6H2O의 물질 특성이 그대로 반영되어 각 상전이 온도에서 열의 흡수와 방출이 발생되어 온도변화가 지연되는 구간이 나타났다. 이를 통해 가압방식으로 상전이 물질을 담지 할 경우 상전이 물질의 상 변화 특성이 담지 이후에도 유지됨을 확인하였다.
3.2. 희석식 방법으로 제조된 PCM/활성탄의 열 흡수/방출 특성3.2.1. 동결건조 및 희석에 따른 상전이 물질의 열 흡수/방출 특성 변화
Fig. 2는 동결 건조된 Mn(NO3)2・6H2O와 에탄올에 희석 후 동결 건조된 Mn(NO3)2・6H2O의 온도변화를 측정한 결과이다. 회색 점선은 외기 온도를 나타내며 10℃로 유지되었다. 빨간색 실선은 물의 온도를 나타내며 60℃ 에서부터 외기 온도인 10℃와 열적평형을 이룬다, 파란색 실선은 에탄올에 희석 후 동결 건조된 Mn(NO3)2・6H2O의 온도 변화이며 열 흡수/방출 특성을 응용할 만한 상전이 구간이 발현되었다고 보기 어렵다. 초록색 점선은 Mn(NO3)2・6H2O의 온도변화를 나타낸다. 주목할 점은 Mn(NO3)2・6H2O을 동결건조하여 다시 용융 시키면 동결건조하지 않은 Mn(NO3)2・6H2O과 유사한 그래프 개형을 나타내는 현상이다. 따라서 Mn(NO3)2・6H2O은 동결건조 후에도 결정화가 잘 일어나며 상전이 구간이 뚜렷하게 나타나지만 에탄올을 혼합한 Mn(NO3)2・6H2O은 동결건조 후에 결정구조를 잘 형성하지 못하는 것을 확인할 수 있다.
3.2.2. 희석 용매에 따른 무기성 상전이 물질이 충진 된 활성탄의 열 흡수/방출 특성 영향PCM 희석을 위해서는 PCM에 대한 용해도가 높고 PCM의 결정 수에 영향을 미치지 않아야 하므로 100℃ 미만의 온도에서 증발 되어야 하며 마지막으로 용매가 증발된 이후에도 PCM의 열 흡수/방출 기능이 회복되어야 한다. 이에 최적 용매 선정을 위해 메탄올, 에탄올, 아세톤을 용매로 선정하여 실험을 수행하였다. 용매에 의한 열 흡수/방출 능력 방해 영향을 평가하기 위하여 Mn(NO3)2・6H2O과 용매를 17:3으로 혼합한 혼합물 20 g, Mn(NO3)2・6H2O과 용매를 17:3으로 혼합한 후 용매를 85℃에서 증발시킨 시료 17 g을 준비하여 각 세 물질의 열 흡수/방출 특성을 평가하였다. Fig. 3는 메탄올, 에탄올, 아세톤 각 물질에 대한 시간에 따른 온도변화의 결과이다. 희석되지 않은 Mn(NO3)2・6H2O의 경우 Fig. 3의 실선과 같이 16℃까지 과 냉각 현상으로 인하여 응고하지 못하다가 시간이 지나면서 27℃까지 온도가 상승하며 잠열을 발현하여 열의 방출이 발생됨을 확인하였다. 반면에 메탄올에 희석한 시료 및 메탄올에 희석 후 메탄올을 증발시킨 시료의 경우열 흡수/방출 구간이 발생하지 않아 메탄올은 희석 용매로 적절하지 않음을 확인하였다(Fig. 3(a)). 메탄올과의 희석 이후에 상전이구간이 발생하지 않는 것은 메탄올과의 혼합과정에서 화학결합구조가 파괴되었거나 메탄올이 수화염의 결정화를 방해하는 역할을 한 것으로 판단된다.
에탄올을 용매로 사용하였을 경우(Fig. 3(b)), 희석된 Mn(NO3)2・6H2O 용액의 상전이가 분명하게 나타나는 것을 관찰할 수 있었다. 이는 에탄올의 희석과정에서도 Mn(NO3)2・6H2O의 물리화학적 특성이 변화하지 않았음을 의미하고, 다만 희석으로 인해 열의 흡수 및 방출량이 감소한 것으로 판단된다. 에탄올을 증발시켜 제거한 이후에는 상전이 구간의 회복이 명확하게 관찰되었으나 상전이가 발생하는 온도가 15℃ 가량 낮아진 것을 확인 할 수 있었다. 이 결과로 무기성 상전이 물질인 수화염을 에탄올로 희석하여 다시 기화시키는 과정이 상전이 물질의 결정화에는 영향을 미치나 잠열의 발현을 완전하게 방해하지 않는 것을 알 수 있었다. 마지막으로 아세톤을 사용하였을 경우(Fig. 3(c)), 아세톤에 의해 희석된 Mn(NO3)2・6H2O 용액은 열의 방출로 인한 온도감소 완화구간이 미세하게 나타나며 희석 후 아세톤을 모두 증발시킨 Mn(NO3)2・6H2O는 상전이 구간이 Mn(NO3)2・6H2O 원액과 가장 유사한 열/흡수 방출 특성을 보였다. 그러나 아세톤은 극성 PCM과 수화물과 혼합되지 않고 층이 분리되는 현상이 발생하였으며, 아세톤과 Mn(NO3)2・6H2O의 혼합물에 활성탄을 넣은 경우, 활성탄이 아세톤과 수화물 층 사이에서 부유하며 아세톤이 활성탄 세공 내에 충진되는 현상을 보여 PCM 충진을 위한 용매로는 적합하지 않은 용매임을 확인하였다. 본 실험을 통해 무기성 상전이 물질을 희석하기 위한 용매로 에탄올이 선정되었다. 동시에 용매와의 희석을 통해 무기성 상전이 물질의 점도를 감소시키고 활성탄과의 친화도를 향상시켜 활성탄 세공 내에 충진시킨 뒤, 용매을 증발시켜 제거하는 방법으로 열 흡수/방출기능을 가진 활성탄의 제조가 가능함을 확인 하였다.
3.2.3. 활성탄 담지를 위한 무기성 상전이 물질과 에탄올의 희석 비율 결정에탄올을 최적 용매로서 선정한 후 최적 희석 비율을 도출하기 위한 실험을 수행하였으며, 시료는 Mn(NO3)2・6H2O 원액, Mn(NO3)2・6H2O과 에탄올의 비율을 2:1, 1:1, 1:2로 혼합한 혼합액을 사용하였다. Mn(NO3)2・6H2O과 에탄올의 비율이 2:1일 때는 활성탄의 침강이 매우 느린 것을 보였으며, 1:1로 에탄올의 희석 비율에 커짐에 따라 활성탄의 침강성이 증가하여 희석된 상전이 물질이 세공 내로 침투할 때 발생되는 하여 발생한 기포가 많아지는 것을 관찰할 수 있었다. 혼합액에 활성탄을 담지한 10분 후, 에탄올의 비율을 1:2로 하였을 때의 활성탄의 침강성 및 기포발생량은 1:1로 하였을 때와 비슷하였다(Fig. 4). 따라서 부유하는 활성탄이 최소량이 되게 하면서 에탄올의 비율이 낮은 희석비로서 1:1로 결정하였다.
상전이 물질의 활성탄 충진 메커니즘은 주로 모세관 응축에 의한 흡착에 기인하며, 다공성일수록 흡착량이 증가한다[28]. 본 연구에서 사용된 활성탄은 약 23-43 Å의 비표면적 1,000 m2/g 이상의 Meso-pore 범위의 세공이며, 모세관 현상이 가장 두드러지게 발생하는 공극의 범위이기도 하다. 상전이 물질의 활성탄 충진은 공극 크기와 밀접한 관련이 있는데, 크기가 작은 경우 상전이 물질의 유동성이 제한되어 결정화에 제약이 있고 공극이 큰 경우에는 모세관 현상을 기대하기 어렵다. 무기성 수화물의 점도를 낮춰 활성탄 세공으로의 확산을 유도하기 위해 희석된 Mn(NO3)2・6H2O/에탄올 혼합물은 모세관 현상 및 상호정전기력(Electrical force)에 의한 활성탄과의 소수성 결합 등을 통해 물리적 흡착을 하게 된다. 상전이 물질은 높은 수화물 함량으로 인해 열을 방출하는 냉각과정에서 액체와 고체가 분리되는 과냉각 현상이 있을 수 있으나[14], 본 실험에서는 상전이 물질을 활성탄 세공에 담지하여 과냉각이 일어나지 않았다. 이는 활성탄의 미세 세공 내 충진된 상전이 물질이 팽창 및 수축을 반복하면서, 세공벽 내 상전이 물질의 움직임(moving)을 일으켜 과냉각 현상을 방지할 수 있는 것으로 판단된다.
3.2.4. 용매 제거 방법에 따른 무기성 상전이 물질이 충진 된 활성탄의 열 흡수/방출 특성 영향무기성 상전이 물질의 원활한 담지를 위해 사용된 용매를 다양한 형태로 제거하여 제거 방법에 따른 무기상전이 물질 충진 활성탄의 열 흡수/방출 특성을 평가 하였다. 80℃ 온도로 기화하여 에탄올을 제거하는 방법(D-V-PIA), 동결건조기를 이용하여 에탄올을 제거하는 방법(D-F-PIA), 에탄올을 80℃에서 기화한 후 감압 펌프를 이용하여 에탄올을 제거하는 방법(D-D-PIA)을 사용하였다. 우선 –85℃에서 동결 건조를 통하여 에탄올을 제거하였을 경우와 에탄올을 85℃에서 기화한 후 감압 펌프를 이용하여 제거하였을 경우 열 흡수/방출 구간이 발생하지 않음을 확인하였다. 반면에 85℃ 온도에서 기화하여 에탄올을 제거하였을 경우 온도 변화에 따른 열 흡수/방출 특성을 평가한 결과 Fig. 5와 같이 열/흡수 방출 현상이 관찰됨을 확인하였다. 동결건조 및 감압 펌프 이용법 모두 감압 방식을 활용하는데, Table 3에서 제시한 바와 같이 용매 제거 후 상전이 물질의 벌크무게가 감소하는 것으로 보아 감압 방식에 의해 상전이 물질이 활성탄 세공 내에서 외부로 상당부분 빠져나가기 때문인 것으로 판단된다. 85℃ 온도에서 기화하여 에탄올을 제거하는 방법으로 충진된 무기성 상전이 물질의 반복성 및 소재의 안정성을 알아보기 위해 열 흡수/방출의 장시간 반복실험을 수행하였다. Fig. 6는 30시간 동안 주기적으로 변하는 온도에 따른 PCM/활성탄 물질의 열 흡수/방출 온도변화를 나타낸 것이다. 챔버 내 온도변화의 설정은 0℃부터 50℃까지 오른 후 다시 0℃로 내려오는 승온 및 냉각을 반복하고 10 cycle 온도변화 반복에 따라 PCM/활성탄 물질의 온도를 측정하였다. 주변 온도가 50℃까지 상승 할 때, PCM/활성탄 물질의 온도변화속도는 느린 것을 나타냈으며 최대 45.5℃까지 상승한다. 주변 온도가 0℃로 냉각될 때도 PCM/활성탄 물질의 온도변화속도는 느린 것을 보이며, 25℃와 19℃ 근처 온도에서 상전이가 일어난 후 온도는 약 7℃까지만 떨어지는 것을 나타낸다. 상전이 물질이 에너지를 받으면 활성탄으로의 열전달 시간차가 생기는데, 온도에 따른 열 흡수/방출 시 상전이 물질 내에 축열이 생기는 것으로 판단된다[14,28]. 위와 같이 PCM/활성탄 물질은 10회 이상의 반복실험에도 열 흡수/방출 능력이 일정하게 유지되는 것을 보였으며, 이는 담지 된 상전이 물질이 액화와 응고 상전이과정에서도 활성탄 세공 외부로의 이탈이 없이 안정적으로 담지 되었음을 보여준다.
3.3. 무기성 상전이 물질이 충진 된 활성탄의 물리적 특성각 방법에 의해 상온 상전이 물질이 충진 된 활성탄의 bulk density를 Table 3에 나타내었다. 고압을 가하여 Mn(NO3)2・6H2O을 활성탄 내에 충진 하였을 때 bulk density는 0.806 g/ml 이며, 이를 상대적으로 상전이 물질 충진량을 비교할 수 있다. 에탄올 희석 후 건조 방법을 다르게 한 세가지 방법에 대하여 bulk density 결과를 비교해 보았을 때, 상전이 물질을 희석하여 충진 한 후 80℃ 온도로 기화하여 에탄올을 제거하는 방법(D-V-PIA)이 가장 많은 양의 상전이 물질을 충진 할 수 있는 방법임을 확인 하였다.
활성탄 세공 내에 무기성 상전이 물질의 충진 여부를 정성적으로 파악하기 위하여 SEM, 충진된 활성탄의 단면에 대한 XPS, TEM, EDS mapping 분석을 하였다.
가압식 방법을 이용하여 Mn(NO3)2・6H2O가 충진 된 분말 활성탄의 표면을 전자현미경으로 분석하여 Fig. 7에 나타내었다. Fig. 7(a)는 충진 전의 분말 활성탄의 표면이며 (b)는 Mn(NO3)2・6H2O 충진한 뒤의 분말 활성탄의 표면을 촬영한 결과이다. 상전이 물질을 충진한 뒤, 불균일한 결정들이 분말 활성탄 표면을 덮고 있는 것을 관찰할 수 있다. 이 결과로 가압방식을 통해 무기성 상전이 물질이 활성탄 내부에 존재하여 고정되어있음을 확인하였다.
충진 과정을 통해 활성탄의 단면에 어떤 원자들이 흡착되어 있는지 파악하기 위하여 EDS mapping 분석을 수행하였다. Fig. 8(a)는 Mn(NO3)2・6H2O이 충진 된 분말 활성탄의 단면에 대한 FE-TEM 촬영 사진이며, Fig. 8(b)와 (c)는 Fig. 7(a) 활성탄에 대한 EDS mapping 분석 결과를 나타낸 것이다. Fig. 8(b)는 탄소에 대한 mapping 결과를 나타내며 탄소는 활성탄을 구성하는 주요물질이기 때문에 전체적으로 고루 분포되는 것을 확인할 수 있다(시료를 고정시키기 위한 탄소테이프의 영향으로 시료 주변 또한 탄소가 검출되었음). Fig. 8(c)는 망간에 대하여 맵핑한 결과이다. Fig. 8(a)와 비교했을 때, Fig. 7(a)에서 진하게 촬영된 부분이 Fig. 8(c)에서 나타내는 망간의 분포와 동일 부분임을 알 수 있다. 즉, 가압방식으로 무기성 상전이 물질을 활성탄에 충진 할 경우 활성탄 세공 내부뿐만 아니라 표면에도 분포하게 됨을 확인하였다. 이를 토대로 친수성인 무기성 상전이 물질을 세공 내에 효율적으로 주입시키기 위해서는 희석 방법이 더욱더 적합함을 확인할 수 있었다.
Fig. 9은 Mn(NO3)2・6H2O을 활성탄에 충진하기 전과 충진한 뒤 각 시료의 단면에 대하여 XPS 분석 결과를 나타낸 것이다. Fig. 9(a)는 충진 전의 활성탄 단면에 존재하는 원자는 탄소 뿐 만 아니라 산소, 칼슘, 루미늄 등이 있는 것을 나타낸다. 또한 Fig. 9(b)를 통해 Mn(NO3)2・6H・O을 충진 한 활성탄의 단면에 분포하는 원자의 종류와 각각의 농도가 충진 전과 다른 것을 알 수 있다. 충진 후에 산소 원자의 농도가 더 높아졌으며 망간, 질소로 인한 새로운 피크가 형성되었다. 이 결과는 무기성 상전이 물질을 활성탄에 충진 한 경우, 산소와 수소분자를 포함하는 치환기가 수소결합에 이용되어 활성탄 표면에 무기성 상전이 물질이 견고하게 담지 되었음을 나타낼 수 있다. 또한 단면에서 상전이 물질을 구성하는 원자를 관찰할 수 있었으며, 활성탄 세공 내에 무기상전이 물질이 누출되지 않고 안정적으로 담지 될 수 있음을 시사했다.
4. 결 론본 논문은 무기성 상전이 물질을 캡슐화 하여 누출이 없이 안정적으로 적용할 수 있도록 하였고, 무기성 상전이 물질을 효율적으로 세공내에 담지시킬 수 있는 여러가지 방법론에 대한 연구를 수행하였으며 주요 결론은 다음과 같다.
1) 가압방식 및 희석방식 모두 무기성 상전이 물질이 활성탄 내부에 고정시킬 수 있는 상전이 충진 방식이며 담지 이후에도 열 흡수/방출 특성이 유지된다.
2) 희석방식 사용 시 용매로서 메탄올을 사용하였을 경우 상전이 물질의 열 흡수/방출 능력이 사라지는 반면 에탄올의 경우 열 흡수/방출이 유지되었으며 최적 희석 비율은 1:1임을 확인하였다.
3) 희석용매 제거 방법에 있어 동결건조 및 기화 후 감압을 이용하여 제거하였을 경우 열 흡수/방출 능력을 상실한 반면 기화방식만을 이용하여 용매를 제거하였을 경우 열 흡수/방출 능력을 유지하였다.
NotesDeclaration of Competing Interest The authors declare that they have no known competing financial interests or personal relationships that could have appeared to influence the work reported in this paper. Fig. 1.Heat absorption/release characteristics of the activated carbon filled with the Mn(NO3)2•6H2O (PCM/AC) using the pressurization method. 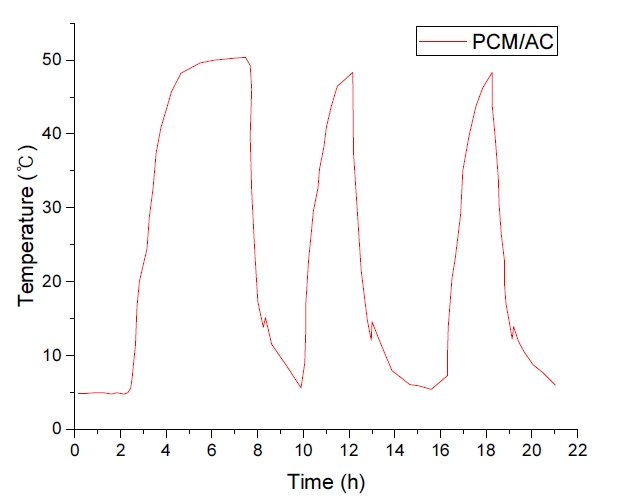
Fig. 3.Heat absorption/release characteristics of a PCM and the PCM diluted in solvents (a) methanol, (b) ethanol, (c) acetone. 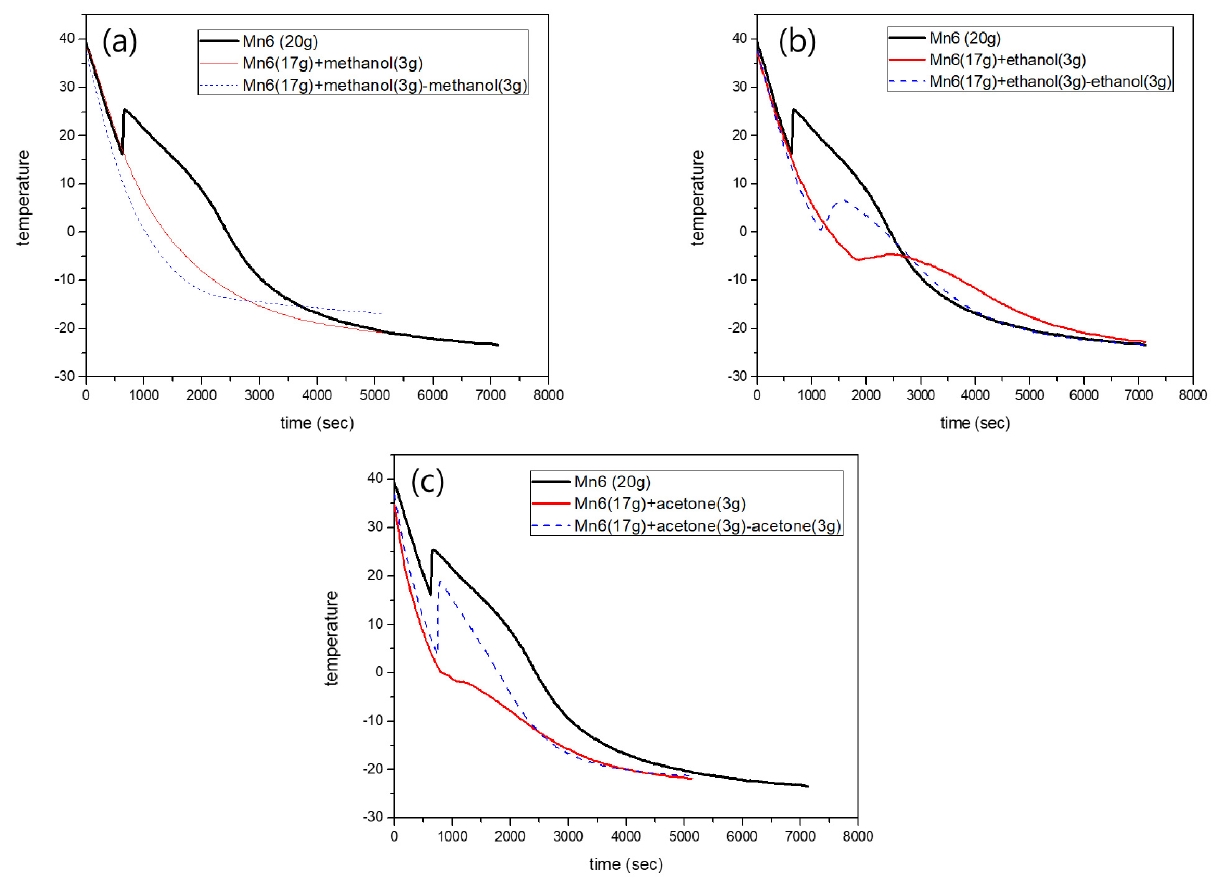
Fig. 4.Comparison of Activated carbon sedimentation according to the dilution ratio of Mn(NO3)2•6H2O and ethanol 
Fig. 5.Heat absorption/release characteristics of Activated carbon filled with Mn(NO3)2•6H2O which solvent was removed through vaporization. 
Fig. 6.Heat absorption/release characteristics of Activated carbon filled with Mn(NO3)2•6H2O in 10 consecutive cycles. 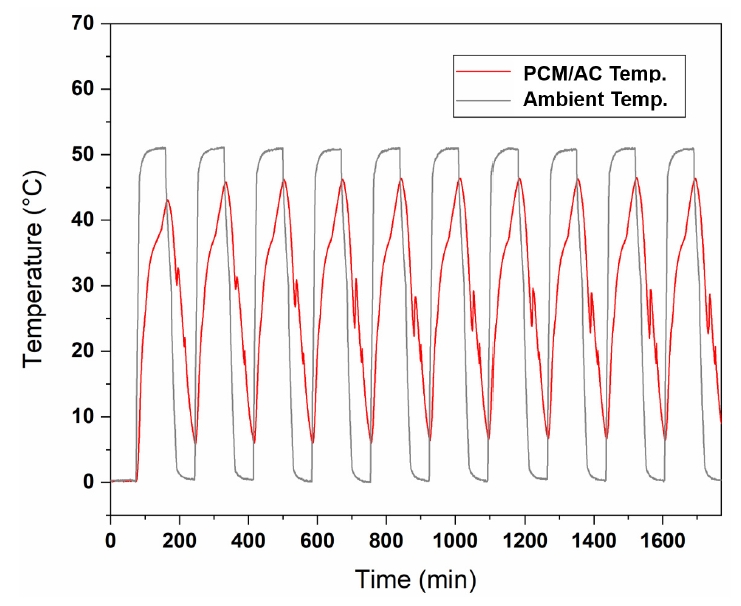
Fig. 8.TEM image of (a) AC filled with Mn(NO3)2•6H2O, (b) Carbon Mapping EDS, and (c) Mn Mapping EDS. 
Table 1.Activated carbons used to embed PCMs. References1. K. Faraj, M. Khaled, J. Faraj, F. Hachem, C. Castelain, Phase change material thermal energy storage systems for cooling applications in buildings: A review, Renew. Sust. Energ. Rev., 119, 109579(2020).
2. S. F. Li, Z. Liu, X.-J. Wang, A comprehensive review on positive cold energy storage technologies and applications in air conditioning with phase change materials, Appl. Energy., 255, 113667(2019).
3. F. Keller, R. P. Lee, B. Meyer, Life cycle assessment of global warming potential, resource depletion and acidification potential of fossil, renewable and secondary feedstock for olefin production in Germany, J. Clean. Prod., 250, 119484(2020).
4. L. Kumar, M. Hasanuzzaman, N. A. Rahim, Global advancement of solar thermal energy technologies for industrial process heat and its future prospects: A review, Energy Convert. Manag., 195, 885-908(2019).
5. T. Simla, W. Stanek, Reducing the impact of wind farms on the electric power system by the use of energy storage, Renewable Energy., 145, 772-782(2020).
6. M. Nguyen, H. Jeong, H. Tran, J. Park, C. Yang, Energy capture evaluation of tidal current turbines arrays in Uldolmok strait, South Korea. Ocean Eng., 195, 106675(2020).
7. C. Demir, R. Cergibozan, Does alternative energy usage converge across Oecd countries?, Renew. Energy., 146, 559-567(2020).
8. T. R. Shah, H. M. Ali, Applications of hybrid nanofluids in solar energy, practical limitations and challenges: A critical review, Solar Energy., 183, 173-203(2019).
9. Y. Zhang, J. Ren, Y. Pu, P. Wang, Solar energy potential assessment: A framework to integrate geographic, technological, and economic indices for a potential analysis, Renewable Energy., 149, 577-586(2020).
10. E. A. Abdelaziz, R. Saidur, S. Mekhilef, A review on energy saving strategies in industrial sector, Renew. Sust. Energ. Rev., 15, 150-168(2011).
11. R. Saidur, N. A. Rahim, M. Hasanuzzaman, A review on compressed-air energy use and energy savings, Renew. Sust. Energ. Rev., 14, 1135-1153(2010).
12. N. Ahmed, K. E. Elfeky, L. Lu, Q. W. Wang, Thermal and economic evaluation of thermocline combined sensible-latent heat thermal energy storage system for medium temperature applications, Energy Converts. Manag., 189, 14-23(2019).
13. L. Lin, X. Liu, T. Zhang, X. Liu, Energy consumption index and evaluation method of public traffic buildings in China, Sustain. Cities. Soc., 57, 102-132(2020).
14. J. Bae, K. S. Kim, Thermal Characteristics of Embedded PCMs in the Pore of Activates Carbon, J. Korean. Soc. Environ. Eng., 41, 582-589(2019).
15. M. Ashouri, B. C. M. Fung, F. Haghighat, H. Yoshino, Systematic approach to provide building occupants with feedback to reduce energy consumption, Energy., 194, 116813(2020).
16. E. Negev, A. Yezioro, M. Polikovsky, A. Kribus, J. Cory, L. Shashua, A. Golberg, Israel, Energy. Build., 204, 109460(2019).
17. H. Kang, M. Lee, T. Hong, J. K. Choi, Determining the optimal occupancy density for reducing the energy consumption of public office buildings: A statistical approach, Build. Environ., 127, 173-186(2018).
18. A. Sarl, K. Kaygusuz, Thermal performance of myristic acid as a phase change material for energy storage application, Renewable energy., 24, 303-317(2001).
19. Q. Mao, Y. Zhang, Thermal energy storage performance of a three-PCM cascade tank in a high-temperature packed bed system, Renew. Energy., 152, 110-119(2020).
20. H. Akeiber, P. Nejat, M. Majid, M. Wahid, F. Jomehzadeh, I. Famileh, J. Calautit, B. Hughes, S. Zaki, A review on phase change material (PCM) for sustainable passive cooling in building envelopes, Renew. Sust. Energ. Rev., 60, 1470-1497(2016).
21. F. Samimi, A. Babapoor, M. Azizi, G. Karimi, Thermal management analysis of a Li-ion battery cell using phase change material loaded with carbon fibers, Energy., 96, 355-371(2016).
22. P. Chandrasekaran, M. Cheralathan, V. Kumaresan, R. Velraj, Enhanced heat transfer characteristics of water based copper oxide nanofluid PCM (phase change material) in a spherical capsule during solidification for energy efficient cool thermal storage system, Energy., 72, 636-642(2014).
23. X. Wan, C. Chen, S. Tian, B. Guo, Thermal characterization of net-like and form-stable ML/SiO2 composite as novel PCM for cold energy storage, J. Energy Storage., 28, 101276(2020).
24. B. Koo, S. Jung, Improvement of air cathode performance in microbial fuel cells by using catalysts made by binding metal-organic framework and activated carbon through ultrasonication and solution precipitation, Chem. Eng. J., 424, 30388(2021).
25. S. Son, B. Koo, H. Chai, H. Tran, S. Pandit, S. Jung, Comparison of hydrogen production and system performance in a microbial electrolysis cell containing cathodes made of non-platinum catalysts and binders, J. Water Process Eng., 40, 101844(2021).
26. T. Nam, H. Kang, S. Pandit, S. Kim, S. Yoon, S. Bae, S. Jung, Effects of vertical and horizontal configurations of different numbers of brush anodes on performance and electrochemistry of microbial fuel cells, J. Clean. Prod., 277, 124125(2020).
|
|
|||||||||||||||||||||||||||||||||||||||