1. 서 론
현재 국내에서는 24기의 원자력 발전소가 가동 중이며 2017년 6월과 2019년 12월에 고리 1호기와 월성 1호기가 각각 영구 정지되었다. 이에 따라 원자력 발전소 운전과정에서 발생하는 원전폐기물과 함께, 영구 정지된 원자력 발전소의 제염 및 해체과정에서 다양한 방사성핵종을 포함한 많은 양의 액체 방사성폐기물이 발생할 것으로 예상된다. 방사성핵종 가운데 세슘은 원자로에서 우라늄의 핵분열 과정에서 약 6%의 높은 비율로 생성되며 액체 방사성 폐기물에서 저농도(0.003∼0.31 µg/L)로 존재한다[1]. 특히, 137Cs은 약 30년 정도의 긴 반감기를 가지고 베타 붕괴를 거쳐 강한 감마선을 방출한다. 또한 높은 수용성과 휘발성으로 인해 생태계로 이동이 용이하기 때문에 생태계에 매우 높은 위험성을 주는 핵종으로 분류된다[2]. 따라서 액체 방사성폐기물 내에 포함된 세슘을 효과적으로 처리할 수 있는 소재 및 공정개발이 필요한 실정이다.
세슘의 처리 방법에는 이온교환법, 응집법, 침전법, 막여과법, 용매추출법, 역삼투법, 기포분리법, 흡착법 등이 있다[3,4]. 다른 처리법과 비교하여 흡착법은 처리 효율성이 높고, 공정이 간단하며 적용이 쉽고, 에너지 소비가 없는 경제적인 방법이다. 대표적인 세슘 흡착제는 제올라이트, 카올린, 몬모릴로나이트, 활성탄, 인 몰리브덴산 암모늄(Ammonium molybdophosphate), 바이오폴리머, 프러시안 블루(Prussian blue) 등이 있다[1,5]. 이러한 다양한 흡착제 가운데 프러시안 블루는 진한 파란색의 색소로서, 다른 흡착제에 비해 제조가 쉽고 저렴하며 세슘 흡착률이 높아 체르노빌 원자력발전 사고와 후쿠시마 방사능 유출 사고에서 방사성 세슘의 해독제로서 사용되었다[6]. 프러시안 블루가 높은 세슘 흡착률을 가지는 이유는 프러시안 블루의 격자구조 크기가 수화된 세슘이온의 크기와 유사해 다른 일가 양이온(K+, Na+)보다 세슘에 대해 높은 선택성을 갖기 때문이다[7-10].
바이오차는 바이오매스(농업부산물, 하수슬러지, 유기성 폐기물 등)를 산소가 제한된 조건에서 열분해하여 제조한 탄소성 물질이다[11,12]. 바이오차는 풍부한 표면 기능기, 넓은 비표면적과 양이온 교환능력, 다양한 크기의 기공을 통해 수중의 양이온성 오염물질을 효과적으로 제거할 수 있는 것으로 알려져 있다[13]. 최근 이러한 바이오차의 특성 때문에 농업 및 산림 부산물로 제조된 다양한 바이오차를 이용하여 물속의 세슘 제거에 관한 연구가 보고되었다[14-17]. 2019년 기준으로 국내 커피박 폐기물 발생 추정량은 약 15만 톤으로, 커피 소비량 증가와 함께 꾸준히 증가하고 있는 추세이다. 이러한 커피박 폐기물은 다양한 유기탄소(셀룰로스, 헤미셀룰로스, 리그닌 등)와 산소 작용기(-OH, -COOH 등)를 포함하고 있어 바이오차의 원료로서 굉장한 이점을 가지고 있다[18-20]. 현재까지 커피박 바이오차 및 그 복합체를 이용하여 다양한 중금속(카드륨, 니켈, 구리, 비소 등)과 염료(콩고레드, 메틸렌블루 등)의 흡착 반응과 흡착량에 대한 연구들이 보고되었지만[21-27], 방사성핵종인 세슘에 대한 흡착 연구는 아직 부족한 실정이다. 따라서, 본 연구에서는 커피박 바이오차 표면을 프러시안 블루로 담지한 흡착제를 합성하여 액체 방사성폐기물 내의 세슘 제거 성능을 평가하고자 한다.
2. 실험방법
2.1. 실험재료 및 방법
프러시안 블루 합성은 Iron(Ⅲ) chloride hexahydrate (FeCl3·6H2O, Daejung chemicals, Korea)와 Potassium hexacyanoferrate(II) trihydrate (K4[Fe(CN)6]·3H2O, Daejung chemicals, Korea)를 사용하였다. 흡착 실험 시, 모의 폐수는 Cesium nitrate (CsNO3, Sigma Aldrich, USA)를 초순수에 녹여 제조하였다. 바이오차의 원료인 커피박은 대전의 한 커피 전문점에서 제공받았다. 증류수로 세척한 커피박 바이오매스를 세라믹 용기에 담은 후 질소가스로 산소 유입을 차단한 전기로 (Thermolyne 48000, Thermolyne, USA)에 넣고 10℃/min으로 승온하여 400℃에서 5시간 동안 열분해하였다. 열분해 후, 상온까지 식힌 바이오차를 1 mm 이하로 분쇄하여 아세톤과 증류수를 이용해 바이오차 표면 및 기공에 남아있는 불순물을 제거하고 60℃ 오븐에서 24시간 이상 건조하였다.
2.2. 프러시안 블루-바이오차 합성 및 특성 분석
커피박 바이오차 1 g을 초순수 200 mL에 넣고 초음파 분쇄기(Powersonic 620, Hwashin technology company, Korea)를 사용하여 약 1시간 동안 분산시켰다. 분산된 용액에 9 M FeCl3·6H2O 용액(170 mL)을 첨가하고 90℃에서 1시간 동안 교반하였다. 이후, 교반된 용액에 15.6 M K4[Fe(CN)6]·3H2O 용액(85 mL)을 천천히 한 방울씩 주입하였다. 노란색에서 푸른색으로 색 변화가 관찰되면 90℃에서 3시간 동안 추가로 더 교반하였다. 다음으로 원심분리 과정을 거쳐 상등액을 제거하고 침전된 반응물을 초순수로 5회 이상 세척하였다. 마지막으로 세척한 반응물을 -70℃에서 24시간 동안 동결 건조하고 건조된 흡착제를 막자사발로 곱게 분쇄하여 유리 바이알에 보관하였다. 합성에 사용한 프러시안 블루(Prussian blue), 커피박 바이오차(Coffee ground biochar) 및 프러시안 블루를 담지한 커피박 바이오차(Prussian blue immobilized coffee ground biochar)는 PB, CGBC 및 PB-CGBC로 명명하였다. 흡착제의 물리·화학적 특성 분석은 FT-IR (Fourier transforminfrared spectroscopy, PerkinElmer, USA), XRD (X-ray diffractometer, Rigaku, Japan), FE-TEM (Field emissiontransmission electron microscope, FEI company, Netherlands), BET (Brunaur-Emmett-Teller, BELSORP-max, Japan) 및 zeta potential analyzer (Otsuka, Japan)을 이용하였고 이를 통해 CGBC와 PB-CGBC의 다양한 표면 기능기, 결정 및 입자 형태, 표면 구조/형태 유추 및 원소 구성을 확인하였다.
2.3. 회분식 흡착 실험
흡착성능평가는 회분식 실험을 통해 이루어졌다. 먼저, 50 mL 코니칼튜브에 1 mM의 세슘 용액과 PB-CGBC 2.5 g/L 넣고 150 rpm에서 72시간 동안 교반하였다. 시료 용액의 pH 값은 0.1 M HCl과 0.1 M NaOH으로 조정하였다. 이후, 일정 시간 간격으로 반응한 용액을 샘플링 및 필터링(0.22 µm)하였고 샘플링 용액은 ICP-OES (Inductively coupled plasma-optical emission spectroscopy, PerkinElmer, USA)로 분석하였다. PB-CGBC의 흡착량(qe)은 다음 식 (1)에 의해 계산하였다.
여기서, Co (mg/L)는 수용액 상의 세슘이온의 초기 농도, Ce (mg/L)는 수용액 상의 세슘이온의 평형 농도, V (L)는 수용액의 부피, m (g)은 실험에 사용된 흡착제량을 의미한다. 흡착 영향 인자는 pH (4∼10), 반응시간(0.5∼72시간), 온도(15∼35℃) 범위에서 조사하였고, 이 결과를 바탕으로 흡착속도 모델, 열역학적 모델, 등온흡착모델에 적용하여 세슘 흡착 양상을 파악하였다. 또한, 실험조건마다 최소 3회 이상 반복실험을 진행하였다.
3. 결과 및 고찰
3.1. 흡착제의 특성 분석
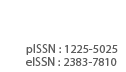
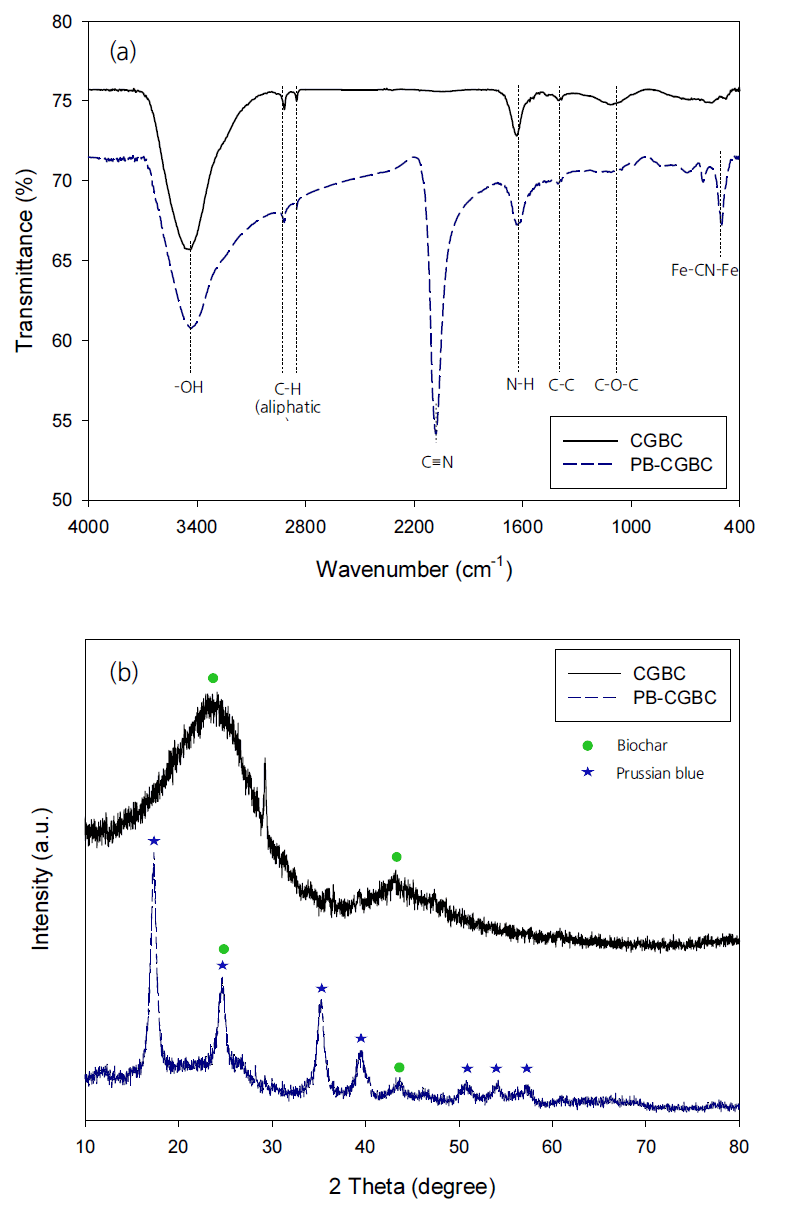
CGBC와 PB-CGBC의 표면기능기를 관찰하기 위해 FT-IR 분석을 실시하였다(Fig. 1(a)). CGBC와 PB-CGBC에서 공통적으로 3,500 cm-1에서 수산기(-OH), 2,921 cm-1과 2,846 cm-1에서 지방족기(C-H), 1,600 cm-1에서 N-H기, 1,402 cm-1에서 방향족기(C-C), 1,109 cm-1에서 C-O-C기가 발견되었다[28-30]. 이들은 주로 바이오차에서 보편적으로 많이 관찰되는 기능기들이다. 또한, 합성한 PB-CGBC의 2,083 cm-1과 499 cm-1에서 프러시안 블루의 C≡N기와 Fe-CN-Fe기가 관찰되었다[31]. Fig. 1(b)는 CGBC와 PB-CGBC의 결정구조를 관찰하기 위한 XRD 결과를 나타낸다. 먼저, 2θ=24o와 2θ=43o에서 바이오차에서 주로 발견되는 크고 넓은 회절피크가 관측되었으며, 이는 CGBC와 PB-CGBC의 구조가 불규칙적인 비결정성 구조라는 것을 나타낸다[32,33]. PB-CGBC의 2θ=17°, 24°, 35°, 39°, 51°, 54°, 57°에서는 프러시안 블루에서 나타나는 주요 회절 피크가 나타났다[8,31]. Fig. 2는 FE-TEM에 기반한 원소 맵핑(Elemental mapping) 분석 결과로서, PBCGBC에서 프러시안 블루의 Fe 성분이 관찰되었고(Fig. 2(a)), 세슘 흡착 후 PB-CGBC에 세슘이 흡착되었음(Fig. 2(b))을 확인할 수 있었다. 마찬가지로 Fig. 3의 EDX 결과에서도 흡착 전후에 PB-CGBC의 Fe 성분이 관찰되었고(Fig. 3(a)), 흡착 후에 PB-CGBC의 세슘 성분이 관찰되어(Fig. 3(b)) 같은 양상을 띠었다. 따라서 흡착제 특성 분석을 통해 커피박 바이오차 표면에 프러시안 블루의 담지 여부와 PB-CGBC의 세슘 흡착 능력을 확인할 수 있었다.
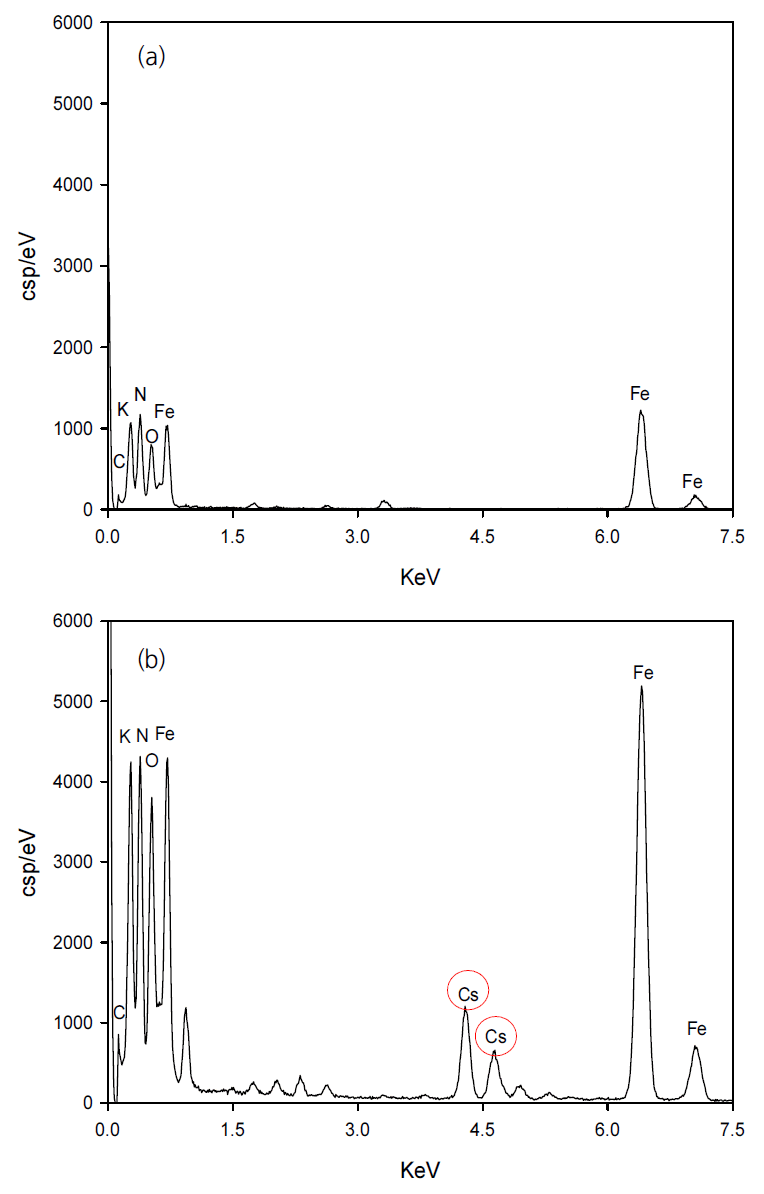
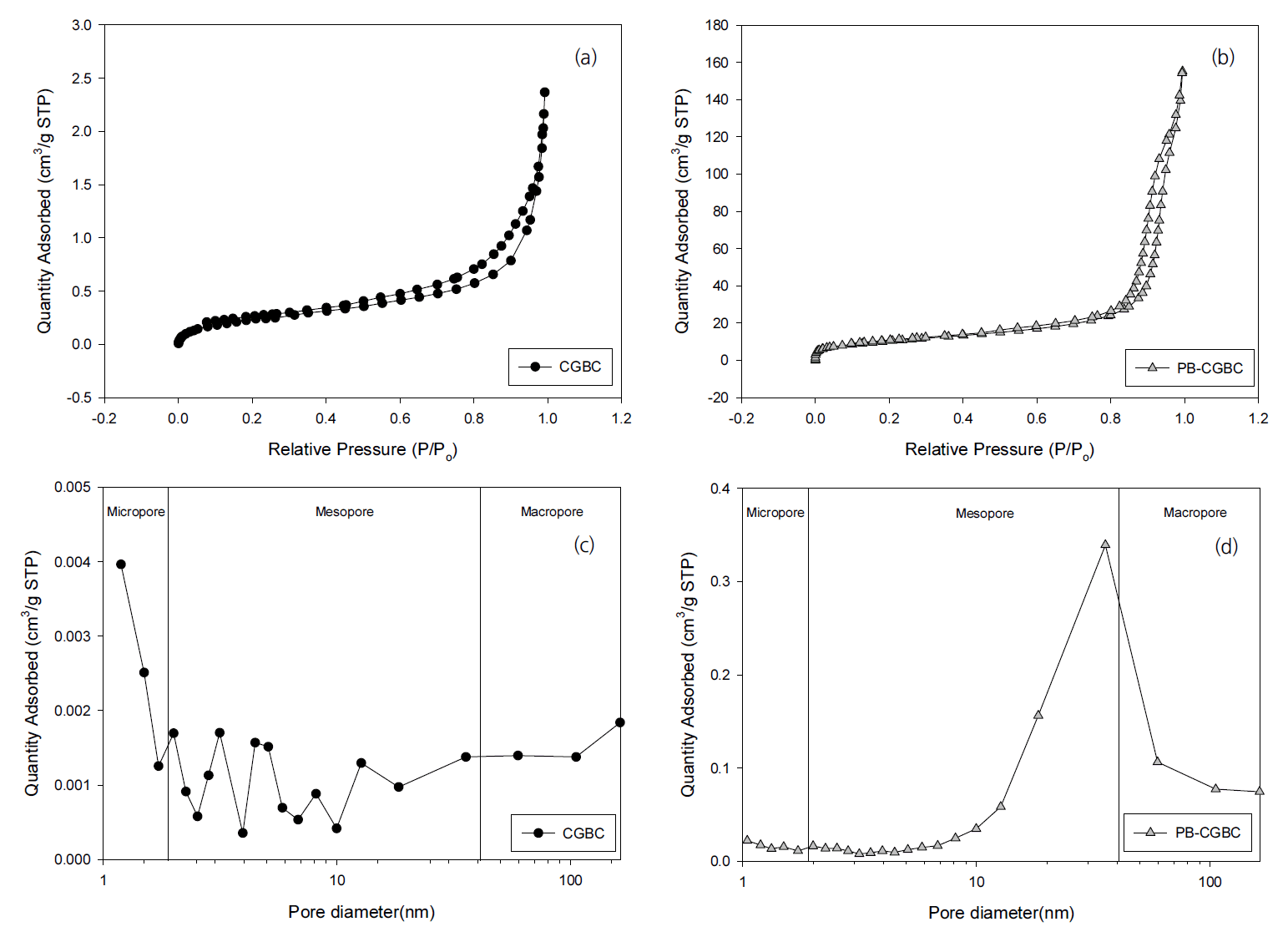
Table 1은 CGBC와 PB-CGBC의 BET 분석 결과를 나타낸다. CGBC 표면과 기공 내부에 프러시안 블루 입자가 부착되어 PB-CGBC의 비표면적과 기공 부피가 상대적으로 증가하였음을 확인할 수 있다. CGBC와 PB-CGBC의 질소 흡/탈착 등온선과 기공 크기 분포도는 Fig. 4에 나타내었다. IUPAC(International Union of Pure and Applied Chemistry) 기공 유형 분류에 따라, 질소 흡/탈착 등온선(Fig. 4(a)와 (b))은 IV 타입으로, 이 결과는 CGBC와 PB-CGBC가 메조기공(Mesopore, 2-50 nm)을 주로 가진 흡착제임을 보여준다. 또한, Fig. 4(c)로부터 CGBC가 메조기공뿐만 아니라 마이크로기공(Micropore, <2 nm)과 매크로기공(Macropore, >50 nm)을 가진 다공성 구조임을 예측할 수 있다. 이러한 CGBC는 합성과정을 통해 프러시안 블루 입자가 기공을 채우면서 메조기공을 주로 가진 PB-CGBC로 합성되었음을 알 수 있다(Fig. 4(d)).
3.2. pH 영향
액체 방사성폐기물의 pH는 대상 방사성핵종 제거에 상당한 영향을 주는 영향인자로 알려져 있다. 본 연구에서 pH 실험은 온도 25℃, 흡착제량 2.5 g/L, 초기 세슘이온 농도 1 mM로 하여 pH 4∼10 범위에서 이루어졌다(Fig. 5). pH가 4에서 8까지 증가함에 따라 PB-CGBC의 흡착량은 증가하였다. 이는 산성조건에서 보다 많은 수소이온이 세슘이온과 바이오차 표면의 흡착 부위를 경쟁했기 때문이다[34]. pH를 8 이상으로 증가시킬 때는 흡착률의 급격한 감소가 관찰되었다. 이는 알칼리 조건에서 철 이온과 수산화 이온과의 강력한 상호작용을 인하여 PB-CGBC 내의 Fe-CN-Fe 결합이 끊어져 프러시안 블루의 구조가 파괴됨으로써 흡착능이 감소한 것으로 보인다[9,35]. pH 변화에 따른 흡착량 변화뿐만 아니라 PB-CGBC의 제타전위 변화도 관찰하였다(Fig. 5). pH가 7에서 4로 감소할 때 제타전위는 증가하였는데, 이는 pH가 감소하면서 증가한 수소이온에 의해 PB-CGBC의 기능기 일부가 양자화(Protonation)되어 표면 음전하가 감소하였기 때문이다[36]. pH 값이 7보다 클 때도 제타전위가 증가하는 것을 관찰할 수 있었다.
3.3. 온도 영향 및 열역학적 모델
온도가 PB-CGBC의 세슘이온 흡착에 미치는 영향을 평가하고자 15, 25, 35℃ 조건에서 초기 세슘 농도 1 mM, pH 8, 흡착제량 2.5 g/L로 하여 실험을 수행하였다(Fig. 6). 온도가 15℃에서 35℃로 증가함에 따라 흡착량은 41.74 mg/g에서 32.28 mg/g으로 감소하였다. 이는 PB-CGBC의 세슘이온 흡착이 발열 반응이기 때문이다. 또한, PB-CGBC의 흡착 특성에 대한 열역학적 해석을 위하여 Gibbs 자유에너지 변화량(∆Go), 엔탈피 변화량 (∆Ho), 엔트로피 변화량 (∆So)을 아래 식 (2)와 (3)으로부터 산출하였다.
여기서, Kc (qe/Ce)는 흡착 평형상수이며, R은 기체상수(8.314 J/mol·K), T는 절대온도(K)를 의미한다. lnKc와 1/T에 대한 직선식의 기울기와 절편으로부터 구한 ∆H와 ∆S은 각각 –33.36 kJ/mol과 –60.0 J/mol·K이었다(Table 2). 온도가 15, 25, 35℃로 증가할수록 ∆Go는 –17.39, –16.48, –16.28 kJ/mol로 증가하였는데, 이는 온도가 증가하면 흡착의 자발성이 감소한다는 것을 의미한다. 이러한 결과는 선행 연구된 프러시안 블루 복합체의 세슘 흡착 양상과 유사하였다[35,37]. 음의 ∆Ho (-33.36 kJ/mol) 값은 PB-CGBC의 세슘 흡착이 발열반응임을 열역학적으로 뒷받침하며, 저온에서 반응이 더 잘 일어남을 의미한다. 그리고 ∆Ho의 절대값이 25 kJ/mol 보다 큰 경우는 화학적 흡착이 강함을 나타내므로, PB-CGBC의 세슘 흡착은 화학적 흡착이 우세함을 유추할 수 있다[38,39]. 또한, 음의 ∆So (–60.0 J/mol·K) 값은 PB-CGBC에 세슘이온이 흡착되면서 흡착제와 용액의 계면 사이에서 무질서도가 감소하였다는 것을 의미한다.
3.4. 동력학적 모델
PB-CGBC에 대한 세슘이온 흡착의 동력학적 특성을 조사하기 위하여, 유사 1차 속도식(Pseudo-first-order model), 유사 2차 속도식(Pseudo-second-order model) 및 Elovich 속도식 모델에 적용하였으며, 관련된 흡착 반응속도 모델은 아래 식 (4), (5) 및 (6)과 같다.
여기서, qe (mg/g)는 평형 흡착량, qt (mg/g)는 시간 t에서의 흡착량, k1 (hr-1)은 Lagergren 일차 속도상수, k2 (g/mg·hr)는 유사 이차 속도상수, α (g/mg·hr)는 초기 흡착속도, β (mg/g·hr)는 화학흡착에 대한 Elovich 상수를 나타낸다. 서로 다른 온도에서 진행한 PB-CGBC에 대한 세슘이온 흡착 실험결과에 각 동력학적 모델들을 적용하였다(Table 3). Elovich 모델의 R2 값은 0.99 이상으로 유사 1차 및 2차 반응속도식 모델보다 실험값과 예측값의 상관관계가 높은 것으로 나타났다. 따라서, 흡착반응의 속도결정 단계가 세슘이온과 PB-CGBC 표면 반응기의 화학적 반응임을 알 수 있다. 특히, 15, 25, 35℃의 온도에서 α값이 β값보다 매우 큰 것을 확인할 수 있는데, 이는 흡착 반응이 비가역적임을 의미한다[40].
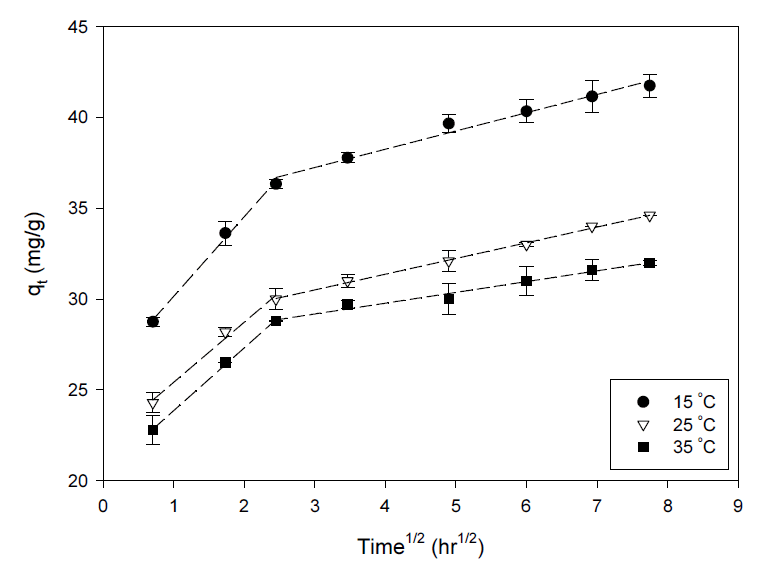
입자내 확산 메카니즘을 확인하기 위해서, Weber-Morris 입자내 확산 모델식 (7)을 적용하였다.
여기서, ki (mg/g·h0.5)는 입자내 확산속도상수, C는 절편을 나타낸다. 입자내 확산식에 15, 25, 35℃의 온도에서의 흡착 데이터를 적용하였을 때, 기울기가 다른 두 개의 직선으로 나타났다(Fig. 7). 초기 직선식 단계는 세슘이온이 용액에서 흡착제 외부표면으로 확산되면서 빠르게 흡착반응이 진행된 외부 표면 흡착단계에 해당되며, 두 번째 단계는 입자내 세공확산이 점진적으로 이루어지는 흡착단계로서 천천히 최종평형에 도달하는 단계이다. 각기 다른 온도에서 직선의 기울기로부터 얻은 입자내 확산속도상수를 Table 4에 나타내었다. 첫 번째 직선구간에 해당하는 외부물질전달 상수값(ki1)들이 두 번째 직선 구간으로부터 얻어진 입자내 확산상수값(ki2)들 보다 훨씬 큰 것을 확인할 수 있으며, 이로부터 입자내 세공확산에 의한 흡착단계가 율속단계인 것을 알 수 있었다. 세공내 입자간 확산에 해당하는 두 번째 직선 구간의 절편 값들은 확산경계층의 두께에 대한 정보를 제공한다. 온도가 증가함에 따라 경계층 두께가 감소하는 것을 확인할 수 있는데, 이는 높은 온도에서 증가된 열적 에너지에 의한 무작위 운동이 증가함에 따라 표면 확산이 보다 더 중요해진다는 것을 나타낸다.
3.5. 반응 시간 및 초기 농도의 영향
반응 시간과 초기 농도 변화에 따른 PB-CGBC에 대한 세슘 흡착 결과를 Fig. 8에 나타내었다. 실험은 초기 세슘 농도 1∼10 mM, pH 8, 온도 15℃, 흡착제량 2.5 g/L 조건에서 72시간까지 진행하였다. 모든 농도에서 24시간까지 흡착량이 빠르게 증가하는 경향을 보이다가 24시간 이후부터 평형에 도달하였다. 이는 반응 초기에 세슘이온이 흡착할 수 있는 반응기가 PB-CGBC 표면에 충분히 존재하다가 일정 시간이 지난 후 포화되었음을 의미한다. 또한, 농도가 1 m M에서 10 mM로 증가하면서 흡착량이 41.7 mg/g에서 103.0 mg/g으로 증가하였는데 이는 흡착 구동력인 농도차의 증가 때문이다.
3.6. 등온흡착식
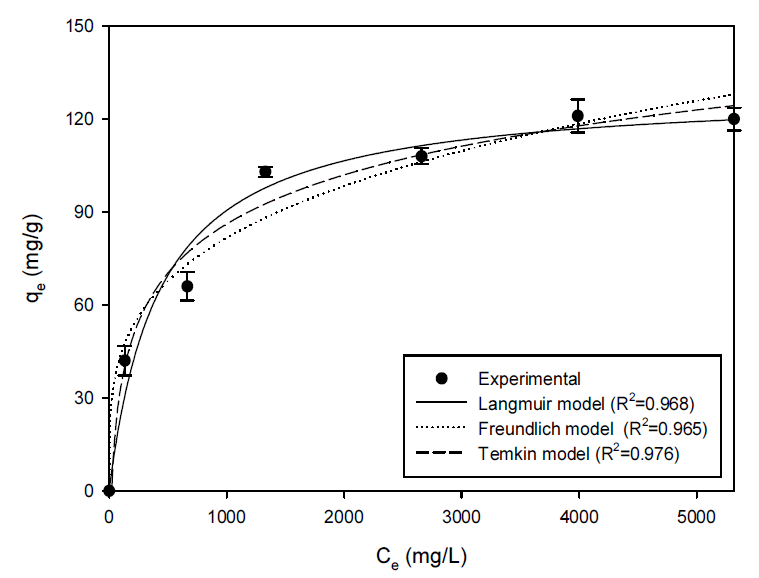
흡착공정에서 등온흡착 모델에 대한 예측은 공정의 설계 및 적용에 중요한 결정사항이다. 따라서 영향인자 실험을 기반으로 하여 초기 세슘 농도 1∼40 mM에서 pH 8, 온도 15℃, 흡착제량 2.5 g/L 조건에서 등온흡착 실험을 진행하였다. 실험 결과는 아래 제시된 등온흡착모델인 Langmuir 모델, Freundlich 모델 및 Temkin 모델 관련한 아래 식 (8), (9) 및 (10)를 적용하였다(Fig. 9).
여기서, qmax (mg/g)는 최대흡착량, KL (L/mg)는 Langmuir 등온 상수, KF (L/g)는 Freundlich 등온 상수, Ar (L/g)는 Temkin 등온 상수, n은 Freundlich 지수, b는 Temkin 상수를 나타낸다. Table 5에 나타나 있듯이 PB-CGBC에 대한 세슘이온의 흡착은 Temkin 모델 (R2=0.976), Langmuir 모델 (R2=0.968), Freundlich 모델 (R2=0.965) 순으로 상관계수 (R2)가 큰 것으로 나타났다. 초기 세슘 농도 40 mM으로부터 얻어진 PB-CGBC의 최대흡착량은 120.00 mg/g으로 나타났는데 이는 Langmuir 모델에서 구한 이론적인 최대 흡착량 129.57 mg/g에 근접한 값이다. 본 연구에서 얻어진 PB-CGBC의 최대 흡착량(qmax)을 현재까지 연구된 프러시안 블루 기반 흡착제와 생물흡착제의 최대흡착량과 비교하였을 때, 기존에 보고된 흡착제보다 PB-CGBC가 보다 더 우수한 세슘이온 흡착성능을 가지고 있음을 확인할 수 있었다(Table 6).
Langmuir 모델의 KL값에 기반한 무차원 분리계수 (RL)를 다음 식 (11)에 의해 계산하여 흡착처리의 적합 여부를 판단하였다.
여기서, RL > 1이면 흡착이 일어나지 않고, RL=1이면 흡착은 선형적으로 일어나고, 0 < RL <1이면 효율적인 흡착이 가능하며, RL=0이면 흡착은 비가역적이다. 본 실험에서 얻은 PB-CGBC의 무차원 분리계수는 모든 온도에서 RL=0.07∼0.77로 모두 0과 1사이에 존재하였기에 PB-CGBC에 의한 세슘이온의 흡착처리가 효과적인 공정이라는 것을 확인할 수 있었다.
4. 결 론
본 연구에서는 프러시안 블루로 담지된 커피박 바이오차(PB-CGBC)를 합성하여 액체 방사성폐기물 내의 세슘이온을 흡착 반응에 의해서 제거하고자 하였다. FT-IR, XRD, FE-TEM, BET 및 제타전위 특성 분석 결과로부터, PB-CGBC 표면에 풍부한 기능기 그룹이 존재하고 독특한 표면 구조를 가지고 있음을 확인할 수 있었다. PB-CGBC에 의한 세슘이온 흡착량은 pH를 4에서 8까지 증가시켰을 때, 흡착량은 증가하였으나 pH 값이 9 이상일 때는 프러시안 블루의 Fe-CN-Fe 결합이 끊어져 흡착량이 감소하였다. PB-CGBC에 대한 세슘이온 흡착은 온도가 증가함에 따라 Gibbs 자유에너지가 증가하였으며, 이는 온도가 증가할수록 흡착공정의 자발성이 감소함을 나타낸다. 또한, ∆Ho가 음의 값을 가지므로 PB-CGBC의 세슘이온 흡착반응이 발열반응임을 열역학적으로 뒷받침해 주었다. 동력학적 실험결과는 Elovich 모델이 유사 일차 및 이차 반응속도식보다 일치도가 높았다. 입자내 확산식으로부터 PB-CGBC 입자내 세공확산에 의한 흡착단계가 흡착반응 율속단계인 것을 알 수 있었다. 또한, 등온흡착 실험 결과로부터 Temkin 모델이 가장 높은 일치도를 나타내었으며, PB-CGBC의 최대흡착량은 선행 연구된 프러시안 블루 기반의 흡착제보다 우수하였다. 이러한 실험결과로부터 본 연구에서 합성된 PB-CGBC는 액체 방사성폐기물 내의 세슘이온을 효과적으로 제거할 수 있는 흡착제임을 확인할 수 있었다.