역삼투 공정에 적용 가능한 시판 염소중화제의 효율 비교
Comparison of Commercial Dechlorination Chemicals used in Reverse Osmosis Processes
Article information
Abstract
목적
역삼투 공정에 주로 사용되는염소중화제인 아황산수소나트륨(SBS)의 경우 사용시 악취 문제가 발생하여 이를 대체할 수 있는 중화제를 찾고자 하였다.
방법
경제성, 사용편의성, 생태독성 등을 고려하여 후보군(메타중아황산나트륨(SM), 티오황산나트륨(ST), 아황산나트륨(SS))을 선정하고 유기물 유무에 따른 잔류염소의 변화, 염소중화제별 적정 주입량 비교, 염소 중화시 처리수의 pH에 따른 영향 등을 실험하였다.
결과 및 토의
염소중화제 주입시 이론적 염소제거 지점에서 염소가 전부 제거되지 않고 약 10~40%가량 남았다. 평가된 세 가지 중화제 모두 초순수를 이용한 실험에서 이론적 주입량보다 1.6~2.6배(ST 1.6배, SM 1.9배, SS 2.6배) 많은 양을 주입해야 염소를 완전히 중화할 수 있었다. 수돗물을 이용한 실험에서는 1.8~3.1배(ST 1.8배, SM 2.2배, SS 3.1배) 많은 양을 주입해야 한다. 주입량만 고려하면 염소 중화를 위한 처리수의 pH가 9 이상이면 ST를 사용하고 pH 9 이하이면 SM을 사용하는 것이 염소제거에 효율적이다.
결론
제품 가격과 사용자 편의성을 고려한다면 악취문제를 해결할 수 있는 ST를 염소중화제로 사용하는 것이 합리적이다.
Trans Abstract
Objectives
The objective of this study was to find a promising dechlorination chemical which can replace sodium bisulfite (SBS), which is mainly used as a dechlorination agent in reverse osmosis processes but can cause odor issues.
Methods
Candidate chemicals were selected in consideration of economic feasibility, ease of use, and toxicity. These included sodium metabisulfite (SM), sodium thiosulfate (ST), and sodium sulfite (SS). We investigated the effect of organic matters in water on residual chlorine decomposition and compared the appropriate injection amounts for each dechlorination chemicals. Also, the effect of the pH of treated water upon dechlorination was assessed.
Results and Discussion
Upon injection of dechlorination chemicals at the theoretical chlorine removal point, the chlorine was not completely removed but 10% to 40% remained. In ultrapure water, it was possible to completely dechlorinate by injecting 1.6 to 2.6 times more than the theoretical injection amount: 1.8, 2.2, and 3.1 times more for ST, SM, and SS, respectively. Considering only the injection amount, ST is an efficient dechlorination chemical for water with pH 9 or higher, and SM is for pH 9 or less
Conclusion
Considering the product price and user convenience, it is feasible to use ST, which can resolve the odor problem.
1. 서 론
역삼투(Reverse Osmosis: RO) 공정은 하폐수처리수 재이용과 해수 및 기수 담수화, 그리고 순수 및 초순수 생산 분야에서 활용이 증가하고 있다. 물 재이용 분야에서는 한정된 수자원의 재활용과 안정적인 용수 확보 측면에서 그 사용량이 늘어나고 있는데, 우리나라의 경우 2020년 하수도 통계에 따르면 전국 111개의 하수처리수 재이용시설이 운영되고 있으며 연간 하수처리량(7,375,622천톤)의 약 15.5% 수준인 1,144,705천톤이 재이용되고 있다. 하수처리수를 재처리하여 이용하기 위한 공정으로 활성탄 흡착, 막여과(정밀여과, 한외여과), 고도산화, 역삼투 공정 등이 사용되는데, 이 중 RO 공정은 이온성 물질까지 제거할 수 있어 하수처리수 재이용시설에 주로 사용되고 있다[1-3]. 해수담수화 분야에서도 RO 공정의 사용이 증가하고 있는데 RO 기반 해수담수화 플랜트는 2006년 58.6%에서 2018년 81.1%까지 증가하였고, 2014년 이후에 신설된 담수화 플랜트의 대부분이 RO공정 기반으로 설립되고 있다[4]. 순수 및 초순수 생산 분야도 최근 산업 고도화에 따라 수질 요구조건이 다양해지고 있으며 RO공정의 사용이 대부분 필요하다[5-7].
이렇듯 RO공정의 수요는 늘어나고 있지만 RO공정을 수처리에 적용하는 경우 가장 문제가 되는 것은 막오염(Membrane Fouling)이다. 막오염이란 막 표면이나 세공에서 물질의 흡착, 부착 그리고 축적 등과 같은 현상이 일어나 물의 유속을 저하시키는 것을 의미하며 크게 입자성 콜로이드와 용존 유기물질, 그리고 미생물의 성장에 의한 막오염 등이 있다[8]. 이 중 콜로이드와 용존 유기물질에 의한 막오염은 전처리 공정인 응집·침전으로 어느 정도 저감이 가능하지만, 미생물의 성장에 의한 막오염을 막기 위해서는 산화제/소독제 주입 등의 화학적 전처리가 필요하다.
이러한 막오염을 막기 위해 일반적으로 차아염소산나트륨(NaOCl), 염소(Cl2), 오존(O3) 등과 같은 산화성 소독제를 주입하는 경우가 많다. 그 중 염소를 넣어서 처리하는 방법이 일반적이지만 막오염을 막기 위해 투입한 염소가 후단의 RO 막에 직접 닿는 경우 막이 산화되어 수명이 줄어들게 되고 그로 인해 막 교체 주기가 짧아지게 된다[9-12]. 이러한 문제를 해결하기 위해 현재는 투입한 염소를 제거하기 위한 염소중화제를 전처리 과정과 RO공정 사이에 투입하고 있으며 환원제로는 아황산수소나트륨(Sodium Bisulfite: SBS)이 일반적으로 사용되고 있다[13-14].
RO 공정중 SBS를 중화제로 사용시 황산화물이 발생하게 되며 이는 악취의 원인이 된다. 하지만 SBS는 사용자가 직접 주입해야 함으로 현장 작업자의 애로사항이 많은 실정이다. 작업현장에서는 SBS를 대체할 수 있는 염소중화제에 대한 필요성이 높으나 대체물질에 대한 연구는 국내에서 한정적으로 진행되고 있어[15] 본 연구를 통해 시판되는 염소중화제의 효율을 평가하였다. 시판되는 염소 중화제 중 후보군을 선정하고 현장 적용을 위해 각 염소중화제에 의한 이론적 염소 제거 양과 실제치를 비교·평가하였다.
2. 실험방법
2.1. 염소중화제 선정
본 실험을 위한 염소중화제를 선정하기 위해 후보군인 Sodium Thiosulfate, Sodium Sulfite, Sulfur Dioxide, Hydrogen Peroxide, Ammonium Chloride, Sodium Metabisulfite, Calcium Thiosulfate, Ascorbic Acid의 경제성, 사용 편의성, 생태독성 등을 고려하여 메타중아황산나트륨(Sodium Metabisulfite: SM), 티오황산나트륨(Sodium Thiosulfate: ST), 아황산나트륨(Sodium Sulfite: SS)의 3종을 선정하였다. 메타중아황산나트륨(Sodium Metabisulfite)은 물에 녹이면 아황산수소나트륨이 되므로 대조군으로 선정하였다.
경제성 면에서 3가지 물질은 가장 많이 사용되는 아황산수소나트륨(Sodium Bisulfite)과 비슷한 가격대이므로 사용하는데 큰 문제는 없을 것으로 보이며, 사용 편의성 부분으로는 3가지 물질 모두 액체 형태이기 때문에 주입하는데 큰 어려움은 없을 것으로 보인다. 각 물질의 생태 독성을 비교해 보면, 메타중아황산나트륨(Sodium Metabisulfite)의 경우 화학적으로는 무독성을 띄어 생체에 무해하나 물 속에 녹아 용존산소 농도나 pH가 변할 경우 일부 독성이 발생될 수도 있다. 하지만 염소중화 과정을 거친 이후 남아있는 양은 아주 소량이거나 모두 반응하고 없어지고, 또한 RO 공정을 거치기 때문에 사용하는데 큰 문제는 없을 것으로 판단된다. 티오황산나트륨(Sodium Thiosulfate)과 아황산나트륨(Sodium Sulfite)의 경우 50~200 mg/L의 농도에서 독성이 관찰되지 않았다[16]. 각 물질에 대한 CAS No., pH, 비중, 화학식, 이론적 주입비 등을 Table 1에 정리하였다.
2.2. 유기물 유무의 영향 실험
처리수 내 유기물의 유무가 잔류염소 소모에 미치는 영향을 파악하기 위해 초순수(DI water; 18.2 MΩ/cm 이하)와 수돗물(Tap water)을 사용하여 비교 실험을 수행하였다. 실험에 사용한 수돗물은 TOC 1.32 mg/L, UVA254 0.020, pH 7.21이었다. 수돗물과 초순수는 각각 2개씩 준비하여 하나는 닫힌계(closed: 공기 접촉이 없는 상태) 에서 측정하였으며, 다른 하나는 열린계(open: 공기 중 노출상태)에서 측정을 진행하여 염소의 휘발에 의한 변화도 관찰하였다. 본 실험에서 주입한 염소는 차아염소산나트륨이며 초기 주입농도는 5 mg/L Cl2이었다. 모든 실험은 3회 반복으로 수행하였다.
잔류염소는 수질오염공정시험기준 잔류염소-비색법(ES 04309.1b)와 US EPA Method 330.5에 따라 DPD 시약(Hack, USA)을 사용하여 염소측정기(Hack, Pocket ColorimeterⅡ)로 측정하였다.
2.3. 염소중화제별 염소제거 실험
염소중화제로 선정한 3가지 물질인 SM, ST, SS를 사용하여 각 중화제별 잔류염소 제거에 필요한 이론적 주입량과 실제주입량을 비교하는 실험을 진행하였다. 수돗물(Tap)과 초순수(DI) 시료에 각각 5 mg/L의 염소를 주입하고 각 중화제의 이론적 염소제거 지점부터 시작하여 잔류염소가 완벽히 제거(0.02 mg/L 이하)되는 지점까지 측정하였다.
2.4. pH에 따른 염소제거 실험
염소중화제의 종류에 따른 염소 제거효율 실험 후 선정된 물질을 사용하여 pH 변화(pH 5~10)가 잔류염소 제거효율에 미치는 영향을 분석하였다. pH 영향을 위한 실험은 초순수(DI)의 경우 산/염기 주입만으로 조정이 힘들어 완충(Buffer) 용액을 만들어야 하는데 본 실험의 목적과 맞지 않아 수돗물(Tap)로만 실험하였다. pH 5, 6, 7 시료는 염산(HCl)을 사용하여 농도를 맞추고, pH 8, 9, 10 시료는 수산화나트륨(NaOH)을 사용하여 농도를 맞추었다. pH를 맞춘 시료에 각각 5 mg/L의 염소를 주입하고 염소중화제를 사용하여 염소제거효율을 측정하였다.
3. 결과 및 고찰
3.1. 유기물 유무에 따른 잔류염소 변화
RO 처리수 내 유기물의 유무가 잔류염소 소모에 미치는 영향을 파악하기 위해 초순수(DI)와 수돗물(Tap)을 사용하여 비교 실험을 수행한 결과를 Fig. 1에 나타내었다. 닫힌계와 열린계를 비교하여 염소 주입 후 0, 0.2, 1, 5, 10, 20, 30분 간격으로 잔류염소를 측정하여 휘발에 의한 염소의 감소를 측정하였다.

Variation of residual chlorine in (a) DI water and (b) Tap water after spiking of chlorine (C0 = 5 mg/L Cl2).
초순수는 공기와 접촉이 없는 경우 잔류염소가 일정하게 유지되었으나, 공기 접촉 5분 후 염소량이 약 8% 감소하고 서서히 감소 추세를 나타냈다. 수돗물로 실험한 경우 열린계와 닫힌계 모두 1분 안에 잔류염소 농도가 10% 정도 빠르게 감소하였고, 열린계에서는 5분 후 20%까지 감소하였다. 수돗물 내 유기물의 염소요구량은 반응 10분 후에 0.8 mg-Cl2/mg- TOC로 이전의 낙동강 수계 정수장을 대상으로 한 연구의 결과와 유사하게 나타났다[17]. 염소요구량은 반응 5분 이내에 빠르게 나타났으며 측정완료 시점이었던 30분 부근에서는 큰 차이가 없었다. 수돗물을 대상으로 한 실험에서 열린계와 닫힌계의 잔류염소 차이와 초순수에서의 차이가 거의 같으므로 유기물의 유무가 염소의 휘발에 미치는 영향은 없다고 볼 수 있다.
3.2. 염소중화제별 적정 주입량 비교
염소와 반응하여 중화시키는 이론적 주입량과 실제 주입량의 차이는 현장 적용에 있어 매우 중요하다. 계산을 통해 잔류염소 농도에 맞는 중화제의 비율을 맞춰서 주입하는 것이 가장 이상적이나 원수의 성상과 주입 약품의 순도에 따라 중화제의 주입량이 달라질 수 있다. RO공정 처리대상수의 수질과 유사한 수돗물(Tap)을 대상으로 염소중화제의 이론적 주입량과 실제 주입량의 차이를 비교한 결과를 Fig. 2에 나타내었다. 비교를 위하여 초순수(DI)에도 같은 비율을 주입하고 실험을 수행하였다. 본 연구에서 사용된 염소중화제가 고순도의 시약 등급이라면 초순수에서는 이론적 주입량과 실제주입량의 차이가 없어야하나 시판되는 염소중화제를 사용하였으므로 두 주입량에 차이가 발생함을 볼 수 있다(Fig. 2).
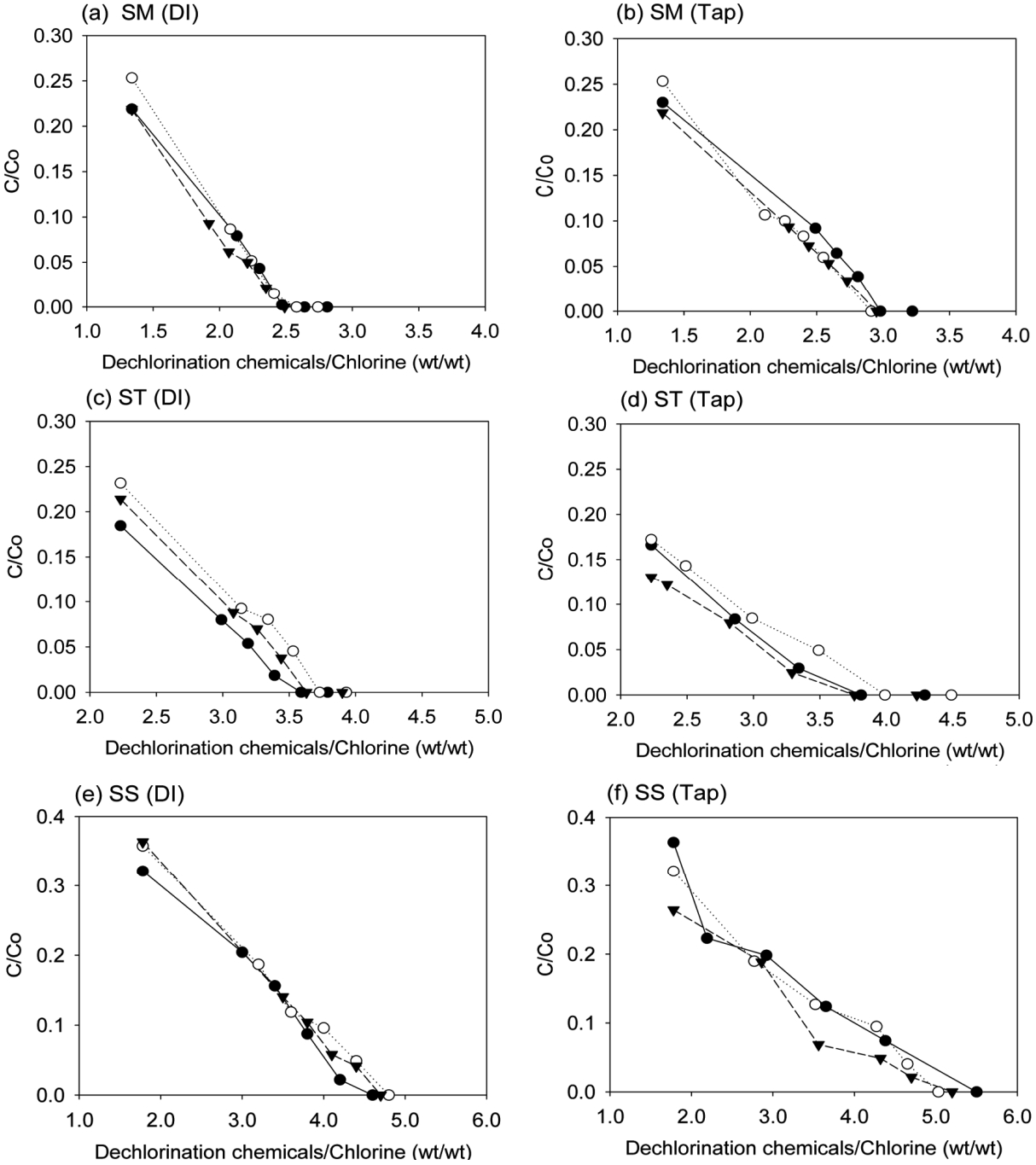
Residual chlorine(C/C0) versus injection ratios of dechlorination chemical to chlorine in DI water (a, c, e) and in Tap water (b, d, f).
초순수(DI)에서 염소중화제 SM의 이론적 100% 제거비는 1.34 kg-DC/kg-Cl2이므로 이론적 제거지점에서 100%의 염소가 제거되어야 하나 실제로는 75~78%의 염소가 제거되었으며, 잔류염소를 완전히 제거하기 위해서는 중화제를 2.5 kg-DC/kg-Cl2의 비율까지 주입해야 했다(Fig. 2(a)). 실제 주입량은 이론적 주입량의 1.9배가 필요한 것이다. 이런 차이가 발생한 것은 사용된 중화제가 100% 순도가 아닌 시판용으로 불순물이 포함되었기 때문으로 판단된다. 수돗물(Tap)에서는 중화제 SM을 3.0 kg-DC/kg-Cl2의 비율(이론적 주입량의 2.2배)까지 주입해야 했다(Fig. 2(b)). 따라서 실제 RO 공정의 처리 대상수에도 중화제를 이 비율 또는 이상으로 주입해야 염소에 의한 RO 막의 손상을 막을 수 있을 것이다.
초순수(DI)에서 염소중화제 ST는 이론적 100% 제거비(2.23 kg-DC/kg-Cl2)에서 77~82%의 염소가 제거되었으며, 잔류염소를 완전히 제거하기 위해서는 중화제를 3.6 kg-DC/kg-Cl2의 비율(이론적 주입량의 1.6배)까지 주입해야 했다(Fig. 2(c)). 수돗물(Tap)에서는 중화제 ST를 3.8 또는 4.0 kg-DC/kg-Cl2의 비율(이론적 주입량의 1.8배)까지 주입해야 했다(Fig. 2(d)).
초순수(DI)에서 염소중화제 SS는 이론적 100% 제거비(1.78 kg-DC/kg-Cl2)에서 77~82%의 염소가 제거되었으며, 잔류염소를 완전히 제거하기 위해서는 중화제를 4.7 kg-DC/kg-Cl2의 비율(이론적 주입량의 2.6배)까지 주입해야 했다(Fig. 2(e)). 수돗물(Tap)에서는 중화제 SS를 5.2 또는 5.5 kg-DC/kg-Cl2의 비율(이론적 주입량의 3.1배)까지 주입해야 했다(Fig. 2(f)). SS는 비교 대상이었던 염소중화제 중 이론적 투입량 대비 실제 투입량이 차이가 가장 크며 초순수와 수돗물에 적용한 주입량의 차이도 가장 크게 나타나 경제성이 낮은 것으로 판단된다.
초순수(DI)에서 수행한 실험에서 염소중화제와 염소의 비(wt/wt)를 보면 SM의 경우 염소 양의 2.5배, ST의 경우 3.6배, SS의 경우 4.7배 정도 투입 시 잔류염소가 모두 제거되었다. 세 가지 염소중화제 모두 이론적 제거지점에서 염소를 모두 제거하지는 못하였는데 사용된 중화제가 100% 순도가 아니고 시판용으로 불순물이 포함되었기 때문으로 판단된다. 수돗물에서는 세 중화제 모두 초순수보다 많은 양을 투입해야 잔류염소를 제거할 수 있었는데, 이는 물에 있는 불순물과 염소중화제가 반응하였기 때문일 것이다.
3.3. 염소 중화시 처리수 pH의 영향
앞선 실험에서 염소를 제거하기 위한 중화제 투입비가 낮은 SM과 ST를 대상으로 pH 변화에 따른 잔류염소 제거율을 비교하였다(Fig. 3). SM의 경우 pH에 따른 중화제 투입비(또는 잔류염소 제거율)의 변화가 거의 없었으나, ST는 pH가 높아질수록 중화제 투입비가 낮아졌다(즉, 잔류염소 제거율이 높아졌다). SM과 ST는 pH 9에서 비슷한 염소 제거율을 보였으며 pH 10이 넘어가는 경우 ST의 투입비가 SM의 투입비보다 낮아졌다. 따라서 pH가 9 이상인 처리수는 ST를 사용하는 편이 잔류염소를 제거하는데 효율적일 것이며, pH 9 이하에서는 SM을 사용하는 것이 합리적이다. 이것은 제품의 가격을 고려하지 않았을 때 비교이고 가격을 고려하면 다소 다를 수 있다. 시판되는 25 kg 제품의 단가가 SM은 1200원/kg이고 ST는 800원/kg이다. 따라서 ST를 SM보다 1.5배 많은 양으로 주입하더라도 SM과 비용은 같다. 가격을 고려할 경우 1 kg의 염소를 제거하는데 필요한 SM 3.2 kg과 ST 4.8 kg이 같은 가격이다. 따라서 가격을 고려하면 pH에 관계없이 ST를 사용하여 SM 사용시 발생 가능한 악취 문제를 피해갈 수 있을 것으로 판단된다.
4. 결 론
RO공정을 사용하는 현장에서 악취문제를 일으킬 수 있는 염소중화제인 SBS를 대체하기 위한 중화제를 찾기 위해 메타중아황산나트륨(Sodium Metabisulfite: SM), 티오황산나트륨(Sodium Thiosulfate: ST), 아황산나트륨(Sodium Sulfite: SS)을 비교・평가하고 다음과 같은 결론을 도출하였다.
1) 평가된 세 가지 중화제 모두 초순수를 이용한 실험에서 이론적 주입량보다 1.6~2.6배(ST 1.6배, SM 1.9배, SS 2.6배) 많은 양을 주입해야 염소를 완전히 중화할 수 있었다. 수돗물을 이용한 실험에서는 1.8~3.1배(ST 1.8배, SM 2.2배, SS 3.1배) 많은 양을 주입해야 한다. 이는 현장에서 사용하는 중화제가 100% 순도가 아니고 불순물이 포함되었기 때문으로 판단된다.
2) 주입량만 고려하면 염소 중화를 위한 처리수의 pH가 9 이상이면 ST를 사용하는 편이 잔류염소를 제거하는데 효율적이며, pH 9 이하이면 SM을 사용하는 것이 합리적이다.
3) 가격을 고려하면 pH에 관계 없이 ST를 사용하여 SM(또는 SBS) 사용시 발생 가능한 악취 문제를 피해갈 수 있다.
Acknowledgements
이 연구는 금오공과대학교 학술연구비로 지원되었음(2019).
Notes
Declaration of Competing Interest
The authors declare that they have no known competing financial interests or personal relationships that could have appeared to influence the work reported in this paper.


