농업환경에서 발생하는 미세플라스틱 필름의 Cd, Pb 흡착 특성
Adsorption Characteristics of Cd and Pb on Microplastic Films Generated in Agricultural Environment
Article information
Abstract
목적
플라스틱은 편리성, 단열성으로 일상 및 여러 가지 산업분야에서 다양하게 활용되고 있고, 플라스틱의 사용량은 계속 증가하는 추세이다. 농업환경에서는 비닐하우스, 멀칭비닐 등의 형태로 플라스틱이 사용되고 있다. 사용 후 환경으로 유입된 플라스틱은 물리적, 화학적, 생물학적 작용으로 작은 단위로 분해된다. 이 중 입자 사이즈가 5 mm 이하인 플라스틱을 미세플라스틱이라 정의한다. 토양 중에 잔류하는 미세플라스틱은 표면적이 넓기 때문에 중금속을 포함한 다양한 오염물질을 흡착시켜 농경지 생태계에 영향을 줄 개연성이 있다. 본 연구에서는 농업환경에서 빈번하게 발생하는 미세플라스틱 필름의 납(Pb)과 카드뮴(Cd)의 흡착특성을 평가하고자 한다.
방법
본 연구에서는 농업환경에서 빈번하게 발생하는 미세플라스틱 필름의 Pb와 Cd 흡착특성을 평가하고자 한다. PVC (polyvinyl chloride) 필름 한 가지와 PE (polyethylene) 필름 두 가지를 5 mm × 5 mm 이하로 잘라 미세플라스틱을 준비한 후, Pb 용액 또는 Cd 용액에 넣어 72시간 동안 흡착 실험을 수행하였다. 흡착실험결과를 Langmuir, Freundlich, Temkin 등온 흡착 모델에 적용하였다.
결과 및 토의
등온 흡착 실험 결과를 Langmuir, Freundlich, Temkin 모델을 이용해 도식화한 결과, 전반적으로 Langmuir 및 Freundlich 모델에 잘 맞는 경향(R2>0.9)을 보였고, Temkin 모델은 상대적으로 잘 맞지 않는 경향을 보였다. 플라스틱 종류와 관계 없이, Pb에 대한 흡착친화도를 나타내는 Langmuir 상수(KL)의 값과 최대흡착에너지를 의미하는 Temkin 상수(AT)의 값이 Cd에 대한 값보다 더 높게 나왔고, 흡착강도와 관련 있는 Freundlich 상수(nF)는 Pb>Cd>1의 경향을 나타내었다. 이는 Cd보다 Pb의 PVC와 PE에 대한 흡착친화도가 크다는 것을 의미한다.
결론
본 연구는 토양 중 잔류하는 미세플라스틱 필름이 Cd와 Pb 같은 중금속을 흡착하고, 따라서 토양환경 중 중금속의 거동에 유의한 영향을 미칠 수 있음을 시사한다. 또한 폐플라스틱의 환경 문제가 사회적 이슈로 대두되고 있는 요즘, 다양한 폐플라스틱으로부터 발생할 수 있는 미세플라스틱의 지중환경 중 관리의 필요성에 대한 합리적 근거를 제공하고, 따라서 토양 환경 내 미세플라스틱에 대한 추가 연구가 이루어질 필요가 있다.
Trans Abstract
Objectives
Plastics are widely used in daily life and in various industrial fields due to their convenience and thermal insulation, and the use of plastics is continuing to increase. In agricultural environments, plastics are largely used for vinyl houses and mulching vinyl. Used plastics are degraded into small fragments through physical, chemical, and biological processes. Among these, plastics with a particle size of 5 mm or less are defined as microplastics. Since microplastics have a relatively large surface area, various pollutants including heavy metals can potentially be adsorbed and affect the agricultural ecosystem. The purpose of this study is to evaluate the Pb and Cd adsorption characteristics on microplastic films frequently generated in agricultural environments.
Methods
The Pb and Cd adsorption characteristics on microplastic films were studied with 3 different plastic films. Microplastic samples were prepared by cutting PVC (polyvinyl chloride) and PE (polyethylene) films to have the sizes of < 5 mm×5 mm. The prepared microplastic samples were placed in Pb or Cd solutions having a range of concentrations and shaken for 72 h for sorption tests. The experimental results were fitted to the Langmuir, Freundlich, and Temkin isothermal adsorption models.
Results and Discussion
The isothermal adsorption test results obtained fitted well to the Langmuir and Freundlich models (R2>0.9), but not the Temkin model. Regardless of the plastic type, the values of Langmuir constant (KL) and Temkin constant (AT) for Pb were larger than those for Cd, and the Freundlich constant (nF) showed a tendency of Pb>Cd>1, indicating the greater Pb sorption strength or affinity than Cd on PVC and PE.
Conclusions
This study shows that the microplastics in soil adsorb heavy metals like Cd and Pb affecting the heavy metal fate in the soil environment. With an increasing attention on the environmental problems due to plastic wastes, this study provides the basis for the need of management of soil environment. Therefore, further research on microplastics in soil environment is required.
1. 서 론
플라스틱은 편리성과 단열성으로 일상 및 여러 산업분야에서 다양하게 활용되고 있고, 그에 따라 플라스틱의 사용량은 계속 증가하는 추세에 있다[1]. 특히, 농업환경에서는 비닐하우스, 멀칭비닐 등의 형태로 플라스틱이 널리 사용되고 있다[2]. 사용 후 환경으로 유입된 플라스틱은 물리적, 화학적, 생물학적 작용을 통해 작은 단위로 분해된다[3]. 이 중 입자 사이즈가 5 mm 이하인 플라스틱을 미세플라스틱이라 정의한다[4]. 토양 중에 잔류하는 미세플라스틱은 일반 플라스틱에 비해 표면적이 넓기 때문에 중금속을 포함한 다양한 토양 환경 내 오염물질을 흡착 및 농축시켜 농경지 생태계에 영향을 줄 개연성이 있다[4]. 국내 영농폐비닐 발생량 자료에 따르면, 2018년도 기준 폐플라스틱비닐 발생량은 멀칭용 low density polyethylene (LDPE) 127,431톤(40.0%), high density polyethylene (HDPE) 112,909톤(35.4%), 하우스용 LDPE 68,758톤(21.6%), 기타(polyvinyl chloride (PVC), ethylene vinyl acetate (EVA) 등) 9,677톤(3.0%)으로 총 318,775톤이었고, polyethylene (PE) 재질 폐비닐이 주로 발생하는 것을 알 수 있다[5]. 또한 Kim과 Lee[2]의 농업환경 내 미세플라스틱 오염도 조사 결과에서도 PE 재질의 필름 발생량이 가장 높은 것으로 확인되었다.
Souza Machado et al. [6]에 의하면 미세플라스틱은 토양의 밀도(bulk density), 내수성 입단(water stable aggregate), 토양의 구조(soil structure)를 변화시켜 증발산(evapotranspiration)과 수분 포화도(water saturation)와 같은 물 역학(water dynamics)의 변화와 미생물 활성(microbial activity)의 변화를 초래한다. 또한 미세플라스틱은 궁극적으로 식물의 생물량, 식물 조직의 원소 조성 및 뿌리 특성(trait)에 가시적인 변화를 줄 수 있다[6]. 플라스틱으로부터 첨가제(additives), 가소제(plasticizers) 등이 침출되어 나올 수도 있는데, 이 중 프탈레이트(phthalate)와 비스페놀 A (bisphenol A)와 같은 첨가제는 척추동물(vertebrate)과 무척추동물(invertebrate)의 내분비계 교란(endocrine disruption)을 초래하며, 농업용수 수처리장 슬러지에서 비교적 높은 수준으로 검출되기도 하였다[7]. 또한 1 µm 이하의 난용성 생난분해성(biopersistent)의 미세플라스틱은 세포막, 세포 기관 등과 상호작용하여 막 투과성 변화, 산화 스트레스 유발과 같은 화학적 작용을 발현하기도 한다[7]. 이와 같이 토양 중 미세플라스틱은 토양의 물리적 및 화학적 특성 변화를 초래하고 나아가 토양 중 생물에게 유해한 영향을 줄 수 있다.
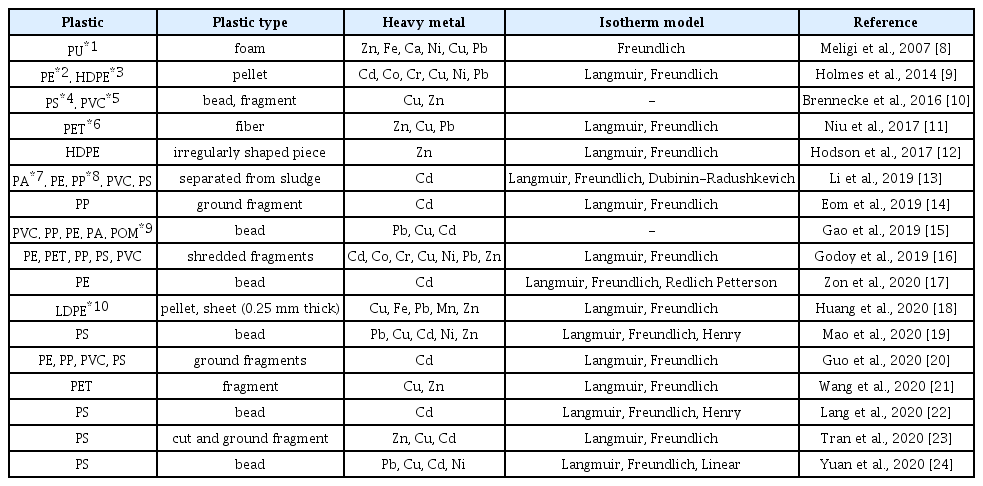
토양 중 미세플라스틱의 존재는 토양의 물리화학적 특성뿐 아니라 중금속과 같은 오염물질의 거동에 영향을 미칠 수 있다. 토양 내 중금속은 섭취, 접촉 및 흡입의 경로를 통해 인체로 유입되어 위해성(중추신경계 영향, 발암성, 기형성, 변이원성 등)을 나타내기도 하고, 대상 부지의 생태계에 노출되어 종 민감도에 따라 독성영향을 유발하기도 한다. 따라서 토양 내 중금속의 거동에 영향을 미칠 개연성이 있는 미세플라스틱과 중금속의 상호작용에 관한 연구가 필요하다. Table 1은 다양한 종류의 플라스틱에 대한 중금속 흡착 관련 연구를 보여 준다. 중금속의 흡착 특성을 평가하기 위해 다양한 등온 흡착 모델이 사용된 것을 볼 수 있다(Table 1). 일정한 온도에서 물질의 흡착특성을 평가하기 위해 Langmuir, Freundlich, Elovich, Dubinin-Radushkevich, Temkin, Sips, Henry, Redlich Petterson 등의 등온 흡착 모델들이 사용될 수 있다. 이 중 기존 연구에서는 플라스틱의 중금속 흡착을 평가하기 위해 주로 Freundlich 모델과 Langmuir 모델을 이용한 것을 알 수 있고, 그 외에도 Dubinin-Radushkevich, Henry, Redlich Petterson 모델들이 이용되었다(Table 1). 이들 연구는 비드(bead) 또는 펠릿(pellet) 형태의 미세플라스틱을 활용하여 수행되었다. 하지만 농업환경 중에는 필름 형태의 미세플라스틱이 잔류할 가능성이 더 크다.
본 연구에서는 농업환경에서 빈번하게 사용하는 PE, PVC 플라스틱 필름으로부터 유래한 미세플라스틱 필름의 특성을 확인하고, 납(Pb)과 카드뮴(Cd)에 대한 흡착특성을 Langmuir, Freundlich, Temkin 모델을 통해 정량화/평가하고자 한다.
2. 실험방법
2.1. 미세플라스틱 물성 분석
국내에서 유통되는 플라스틱 필름(PVC 1종(Hwashin Ind. Co., Seo-gu, Incheon, Korea), PE 2종(Hanjung Chemical, Geumsan-gun, Chungcheongnam-do, Korea (PE(1)), Seojin, Uiseong-gun, Gyeongsangbuk-do, Korea (PE(2))을 구매하여 면적 5 mm × 5 mm 이하의 미세플라스틱 필름을 준비하였다. PVC 및 PE(1)의 두께는 0.1 mm이고, PE(2)의 두께는 0.05 mm이다. 구매한 미세플라스틱의 물성은 attenuated total reflection-Fourier transform infrared spectroscopy (ATR-FTIR) (IRTracer-100, Shimadzu, Japan)로 분석하여 확인하였다. 별도의 시료 전처리 없이, 4 cm-1 분해능으로 4000-400 cm-1 영역에서 ATR-FTIR을 사용하여 투과도 및 흡수도를 측정하였다. 또한 Jung et al. [25]이 제시한 방법을 이용하여 두 가지 PE 필름의 밀도를 구분하였다. 이는 밀도 0.935 g mL-1의 에탄올 용액에 시료를 넣고 시료가 뜨는지, 가라앉는지 확인하여 밀도를 구분하는 방법이다.
2.2. 미세플라스틱의 Cd, Pb 등온 흡착 실험
CdCl2 (ACS reagent, Sigma-Aldrich)와 증류수를 이용하여 0.5-100 mg L-1의 용액을 제조하였다. 용액의 pH는 별도로 조절하지 않았고, pH는 5.83±0.15 정도였다. PbCl2 (99.0%, Junsei Chemical Co. Ltd.)와 증류수를 이용하여 0.5-100 mg L-1의 용액을 제조하였다. 용액의 pH는 질산(HNO3)을 이용하여 pH 5.39±0.14로 조절하였다. 50 mL 튜브에 제조된 Cd 용액 또는 Pb 용액 40 mL와 0.5 g의 PVC, PE(1), 또는 PE(2) 미세플라스틱 필름 시료를 각각 넣은 후 교반기(SH30L, FinePCR)를 이용하여 25℃에서 72시간 동안 60 rpm으로 교반하였다. 교반 후 용액을 0.45 µm 필터로 거른 후, inductively coupled plasma-atomic emission spectroscopy (ICP-AES, ThermoScientific, iCAP 7000 Series, USA)를 이용하여 잔류 Cd 또는 Pb 농도를 분석하였다.
중금속 흡착량은 식 (1)을 이용하여 계산하였다.
여기에서 qe (mg g-1): 플라스틱 필름에 흡착한 중금속의 농도 C0 (mg L-1): 초기 중금속 용액의 농도, Ce (mg L-1): 평형상태에서 중금속 용액의 농도, V (L): 중금속 용액의 부피, W (g): 사용된 플라스틱 필름의 무게이다.
2.3. 등온 흡착 모델을 이용한 모델링
본 연구에서는 Langmuir, Freundlich, Temkin 모델을 이용하여 등온 흡착 실험 결과를 모델링하였다. Sigmaplot (v 12.5, Systat Software Inc., USA)의 regression wizard 기능을 이용하여 모델링하였으며, Langmuir 모델에는 hyperbola-modified hyperbola I, Freundlich 모델에는 power-2 parameter, Temkin 모델에는 logarithm-2 parameter I을 사용하였다.
3. 결과 및 고찰
3.1. ATR-FTIR를 이용한 미세플라스틱 필름 분석 결과
Fig. 1에 ATR-FTIR을 이용한 PVC 필름 1종과 PE 필름 2종의 분석 결과를 나타내었다. PVC의 경우(Fig. 1(a)) 1427, 1331, 1255, 1099, 966, 616 cm-1에서 흡수띠가 확인되었고, PE와 LDPE의 경우(Fig. 1(b)와 1(c)) 2915, 2845, 1467, 1462, 739, 717 cm-1에서 공통적으로 흡수띠가 발견되었다. Jung et al. [25]은 ATR-FTIR 결과와 에탄올 용액을 이용한 밀도 분석 방법을 활용하여 LDPE, linear low density polyethylene (LLDPE), HDPE를 구분하는 방법을 제안하였다. Jung et al. [25]에 따르면 시료에 CH3 band가 존재할 경우 1377 cm-1에서 흡수가 발생하는데, 1377 cm-1에서 흡수띠가 인식되면 LDPE 또는 LLDPE가 확실하고, 인식되지 않을 경우 1377 cm-1의 띠와 1368 cm-1를 비교해 HDPE인지, LDPE인지, LLDPE인지를 확인할 수 있다고 하였다. 본 연구에서 사용한 PE 2종에 대한 ATR-FTIR 분석 결과에서는 1377 cm-1에서 흡수띠가 인식되지 않았다(Fig. 1(b)와 1(c)). 해당 범위를 확대하여 1377 cm-1에서의 띠와 1368 cm-1에서의 띠의 크기를 비교해 보아도, HDPE인지 LDPE인지 LLDPE인지 구분이 불분명하였다(Fig. 1(d)). 이럴 경우, 0.935 g mL-1의 에탄올 용액에 시료를 넣어 구분해 볼 수 있다[25]. 해당 용액에서 시료가 가라앉으면 HDPE이고, 뜨면 LDPE 또는 LLDPE로 구분할 수 있다[25]. 본 연구에서 사용한 PE 2종은 0.935 g mL-1의 용액에 모두 뜨는 것을 확인할 수 있었고, 이를 통해 본 연구에서 사용한 2종의 PE 시료가 LDPE라는 것을 확인할 수 있었다.
3.2. 등온 흡착 모델을 이용한 흡착 결과 모델링
본 연구에서는 Langmuir, Freundlich, Temkin 등온 흡착 모델을 이용하여 평형도달시간 경과 이후 Pb, Cd 농도에 따른 흡착량을 도식화하였다. Table 2에 본 연구에서 사용한 등온 흡착 모델식을 정리하였다. Langmuir 등온 흡착 모델은 단분자층 흡착(monolayer adsorption)을 가정하는 실증적 모델이다. 이 모델은 흡착이 균등한 흡착제 표면에서 일어나고, 흡착제 표면의 흡착질(sorbate) 분자간 입체장애(steric hindrance)와 측면 상호작용(lateral interaction)이 없다고 가정하고, 또한 흡착제 표면에 흡착이 균질(homogenous)하게 일어난다고 가정한다[26]. 한편 Freundlich 등온 흡착 모델은 가역적 흡착 및 비이상적 흡착을 표현하는데, Langmuir 등온 흡착 모델과 다르게, 다분자층 흡착(multilayer adsorption)을 가정한다[26]. 또한 이 모델은 흡착제 표면의 흡착열(adsorption heat)과 흡착친화도(adsorption affinity)가 흡착제의 불균질(heterogeneous)한 표면에 균등하지 않게 분포되는 것을 가정하고, 흡착층이 두꺼워짐에 따라 흡착 에너지가 지수적으로 감소한다는 것을 가정한다[26]. Temkin 등온 흡착 모델은 Freundlich 모델과 같이 다분자층 흡착을 가정하는데, 단 흡착층이 두꺼워짐에 따라 흡착 에너지가 선형으로 감소한다는 것을 가정한다. 또한 Temkin의 등온 흡착식은 흡착에너지가 균등하게 분포되어있다는 것을 함축하고 있다[26]. 본 연구에서는 서로 다른 가정을 가지고 있는 Langmuir, Freundlich, Temkin 모델을 이용하여 등온 흡착 실험 결과를 비교하였다.
3.2.1. Langmuir 등온 흡착식
Fig. 2는 본 연구의 등온 흡착 실험 결과에 대한 Langmuir 등온 흡착식의 적용 결과를 보여준다. Table 2에 있는 Langmuir 등온 흡착식을 이용하여 흡착제의 단분자층 최대흡착능을 나타내는 상수인 Qm값과 흡착세기(binding strength)를 나타내는 상수인 KL값을 구하였다. KL값이 클수록 흡착세기가 크다는 것을 의미한다[27]. 각 중금속 및 각 미세플라스틱 필름에 대한 이들 값들은 Table 3에 정리되어 있다.
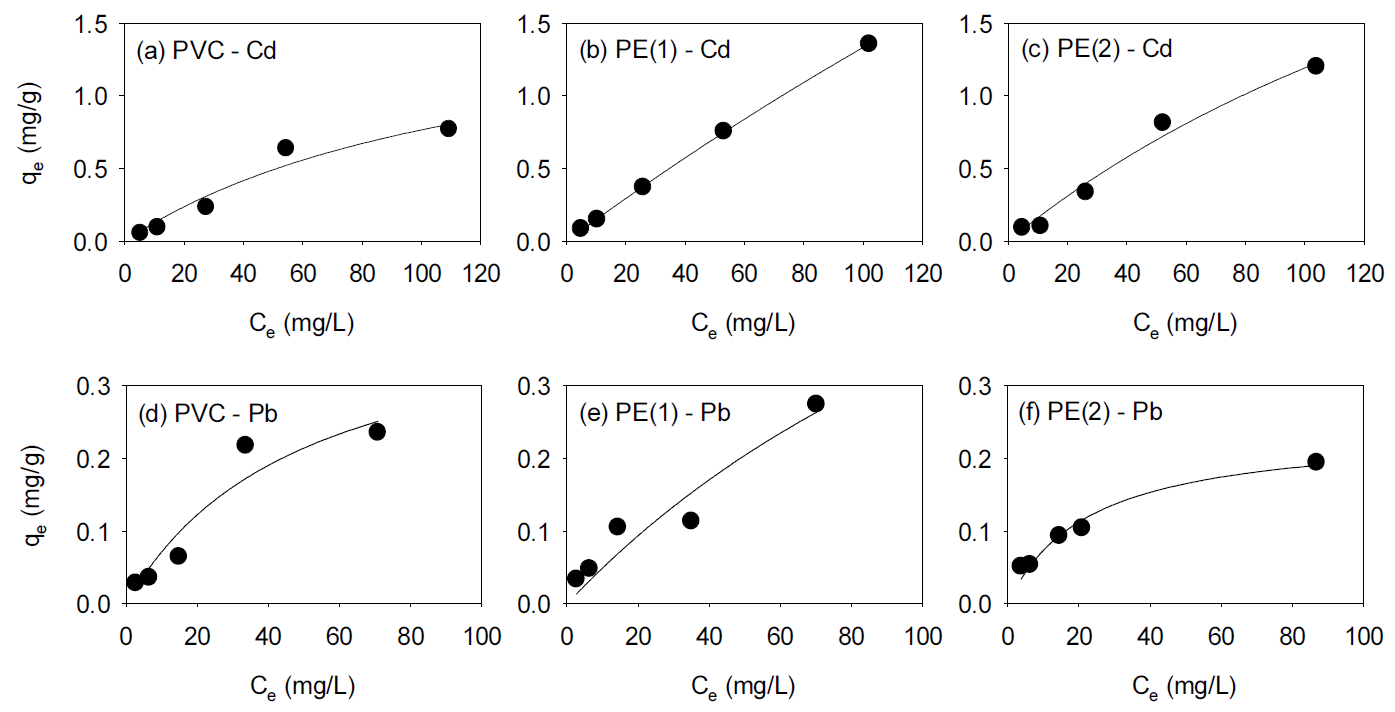
Langmuir isotherm of Cd adsorbed onto (a) PVC, (b) PE(1), and (c) PE(2), and Pb adsorbed onto (d) PVC, (e) PE(1), and (f) PE(2).
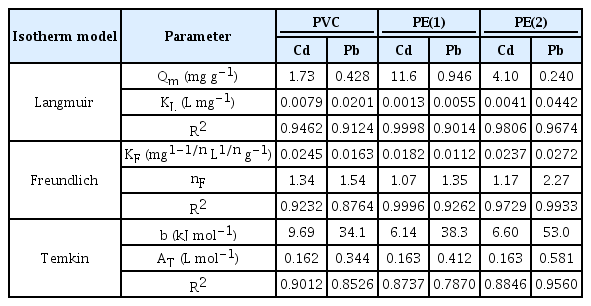
Isotherm parameters obtained from the Langmuir model, Freundlich model, and Temkin model for the adsorption of Cd and Pb onto PVC, PE(1), and PE(2).
플라스틱 종류와 관계없이, Cd의 Qm값(최대흡착능)이 Pb의 Qm값보다 크고, KL값의 경우, Cd의 KL값이 Pb의 값보다 작았다. PVC에 대한 Cd의 Qm값은 1.73 mg g-1, Pb에 대한 Qm값은 0.428 mg g-1이고, PE(1)에 대한 Cd의 Qm값은 11.6 mg g-1, Pb에 대한 Qm값은 0.946 mg g-1이고, PE(2)에 대한 Cd의 Qm값은 4.10 mg g-1, Pb에 대한 Qm값은 0.240 mg g-1이었다. 한편, PVC에 대한 Cd의 KL값(흡착친화도)은 0.0079 L mg-1, Pb에 대한 KL값은 0.0201 L mg-1이고, PE(1)에 대한 Cd의 KL값은 0.0013 L mg-1, Pb에 대한 KL값은 0.0055 L mg-1이고, PE(2)에 대한 Cd의 KL값은 0.0041 L mg-1, Pb에 대한 KL값은 0.0442 L mg-1이었다.
3.2.2. Freundlich 등온 흡착식
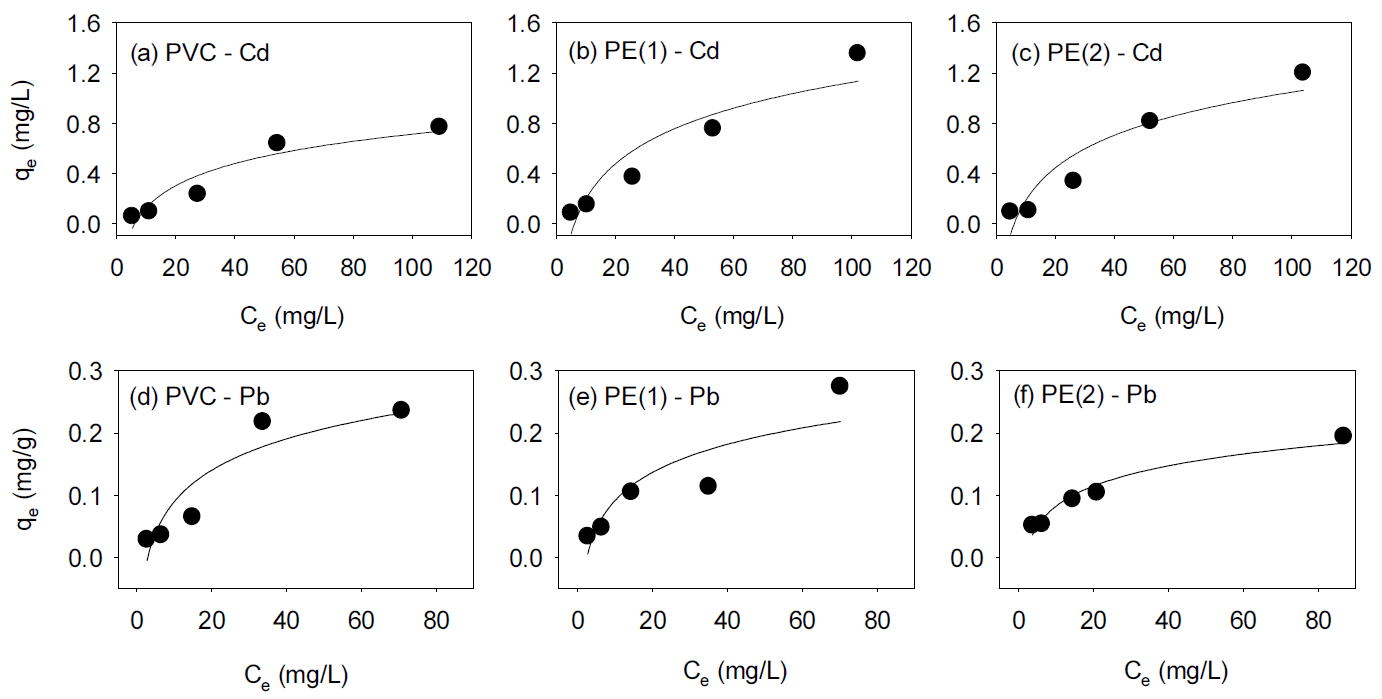
Table 2에 있는 등온 흡착식을 이용하여 Ce에 대한 qe값을 그래프로 그린 후, KF과 nF값을 도출하였다. KF는 흡착능과 관련된 상수, nF은 흡착강도와 관련된 상수이다. KF값이 클수록 흡착능이 크고, nF의 경우, nF<1이면 화학적 흡착이 일어난다고 하고, nF>1이면 물리적 흡착이 일어난다고 한다[28]. Fig. 3은 본 연구의 등온 흡착 실험 결과에 대한 Freundlich 등온 흡착식의 적용 결과를 보여준다.

Freundlich isotherm of Cd adsorbed onto (a) PVC, (b) PE(1), and (c) PE(2), and Pb adsorbed onto (d) PVC, (e) PE(1), and (f) PE(2).
PVC에 대한 Cd의 KF값은 0.0245 mg1-1/n L1/n g-1, Pb의 KF값은 0.0163 mg1-1/n L1/n g-1이고, PE(1)에 대한 Cd의 KF값은 0.0182 mg1-1/n L1/n g-1, Pb의 KF값은 0.0112 mg1-1/n L1/n g-1이고, PE(2)에 대한 Cd의 KF값은 0.0237 mg1-1/n L1/n g-1, Pb의 KF값은 0.0272 mg1-1/n L1/n g-1이었다. 한편 nF(흡착강도)값의 경우 플라스틱의 종류와 관계없이 플라스틱에 대한 Cd의 nF값이 Pb에 대한 nF값보다 작았고, 또한 모든 경우 모든 경우 nF>1으로, 물리적 결합이 선호되는 상태였다[28]. PVC에 대한 Cd의 nF값은 1.34, Pb에 대한 nF값은 1.54이고, PE(1)에 대한 Cd의 nF값은 1.07, Pb에 대한 nF값은 1.35이고, PE(2)에 대한 Cd의 nF값은 1.17, Pb에 대한 nF값은 2.27이었다.
3.2.3. Temkin 등온 흡착식
Table 2에 있는 Temkin 등온 흡착식을 이용하여 Ce에 대한 qe값을 그래프로 그린 후, b값과 AF값을 도출하였다. R (8.314 J mol-1 K-1)은 기체상수이고, T (K)는 절대온도, b (kJ mol-1)값은 흡착열과 관련된 값이고, AT(L g-1)은 최대흡착에너지를 의미하는 흡착평형 상수이다. Fig. 4는 본 연구의 등온 흡착 실험 결과에 대한 Temkin 등온 흡착식의 적용 결과를 보여준다.
Temkin isotherm of Cd adsorbed onto (a) PVC, (b) PE(1), and (c) PE(2), and Pb adsorbed onto (d) PVC, (e) PE(1), and (f) PE(2).
플라스틱의 종류와 관계없이, Cd에 대한 b값(흡착열과 관련된 값)이 Pb에 대한 b값보다 작았다. PVC에 대한 Cd의 b값은 9.69 kJ mol-1, Pb의 b값은 34.1 kJ mol-1, PE(1)에 대한 Cd의 b값은 6.14 kJ mol-1, Pb의 b값은 38.3 kJ mol-1, PE(2)에 대한 Cd의 b값은 6.60 kJ mol-1, Pb의 b값은 53.1 kJ mol-1이었다. 최대흡착에너지를 의미하는 AT값 또한 플라스틱의 종류와 관계 없이, Cd에 대한 AT값이 Pb에 대한 값보다 작았다. PVC에 대한 Cd의 AT값은 0.162 L mol-1, Pb의 값은 0.344 L mol-1, PE(1)에 대한 Cd의 b값은 0.163 L mol-1, Pb의 b값은 0.412 L mol-1, PE(2)에 대한 Cd의 b값은 0.163 L mol-1, Pb의 b값은 0.581 L mol-1이었다.
3.3. 미세플라스틱에 대한 중금속 등온 흡착 실험 결과에 대한 고찰
Table 3는 본 연구에서 수행한 등온 흡착 실험 결과에 Langmuir, Freundlich, Temkin 모델을 적용하여 도출한 상수 및 결정계수(R2)를 보여준다. 대체적으로 Langmuir, Freundlich 모델에 잘 맞는 경향(R2 > 0.9)을 보였고, Temkin 모델에는 잘 맞지 않는 경향을 보였다.
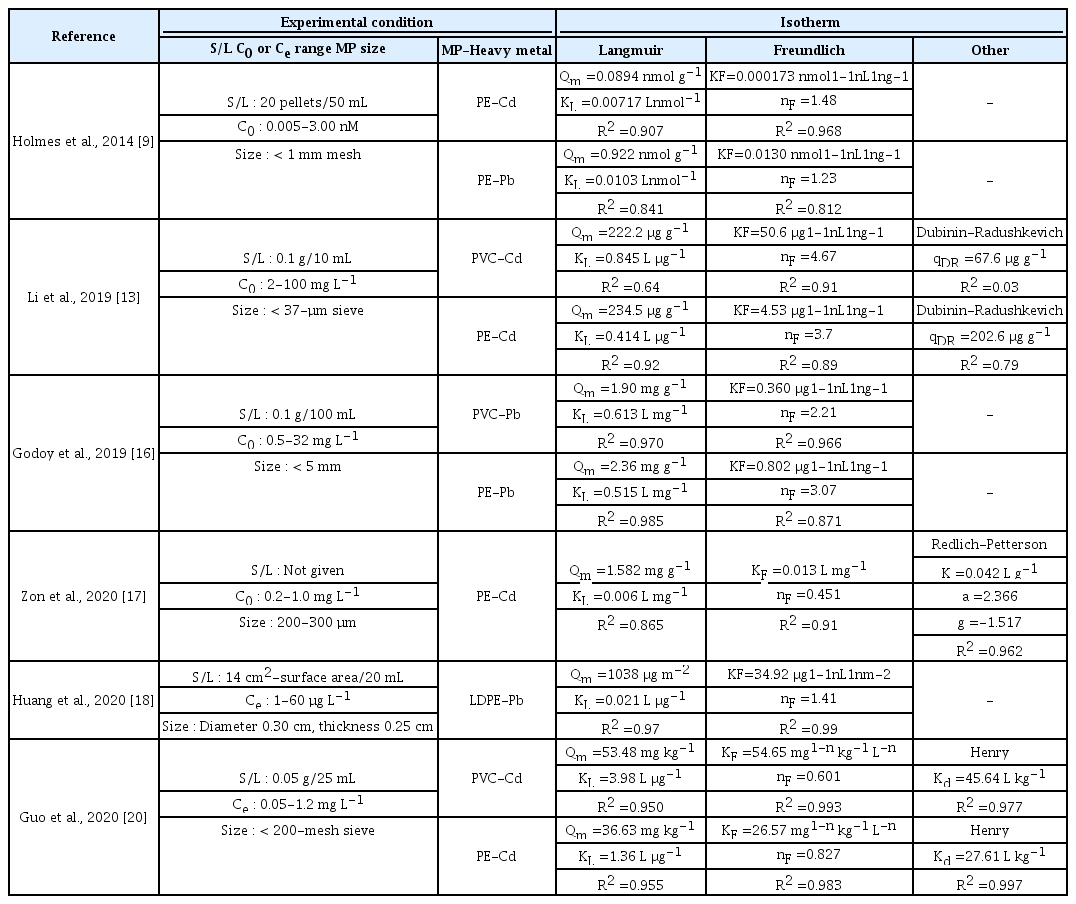
미세플라스틱과 Cd의 흡착에 관한 문헌연구를 수행한 결과 Li et al., [13] Zon et al., [17] Guo et al. [20]의 연구결과를 확인할 수 있었다. Li et al. [13]과 Guo et al. [20] 모두 PVC와 PE에 Cd에 대한 등온 흡착 실험을 수행하였는데(Table 4), Li et al. [13]연구의 초기농도(C0) 범위는 2-100 mg L-1로 본 연구와 비슷하였고, Guo et al. [20] 연구의 평형농도(Ce) 범위는 0.05-1.2 mg L-1로 본 연구와 농도 범위가 크게 달랐다. 농도 범위가 비슷한 Li et al. [13]연구의 결과와 비교한 결과, 본 연구와 같이 Langmuir 상수인 Qm 값의 경우 PVC의 값이 PE의 값보다 작고, KL 값의 경우 PVC의 값이 PE의 값보다 컸다. Freundlich 상수인 KF 값의 경우 PVC의 값이 PE보다 크고, nF 값의 경우 모두 1보다 컸다.
미세플라스틱과 Pb의 흡착에 관한 문헌연구를 수행한 결과 Godoy et al., [16] Huang et al. [18]의 연구결과를 확인할 수 있었다. Huang et al. [18]의 연구의 평형농도(Ce) 범위는 1-60 µg L-1로 본 연구와 범위가 크게 달라 비교가 불가능하였다. Godoy et al. [16]의 연구는 초기농도(C0) 범위가 0.5-32 mg L-1로 본 연구와 크게 다르지 않았고, 이에 따라 본 연구와 유사한 Qm 값이 도출되었다. 반면, KL 값은 PVC 0.163 L mg-1 및 PE 0.514 L mg-1로 보고하여 본 연구와 차이를 보였다. 1/nF는 본 연구와 Godoy et al. [16]의 연구 모두에서 1 보다 작은 값을 나타냈으며, KF는 PVC 0.360 mg1-1/n L1/n g-1 및 PE 0.802 mg1-1/n L1/n g-1로 보고하여 본 연구와 차이를 보였다. 도출된 Langmuir 및 Freundlich 모델 상수의 차이는 등온 흡착 실험의 조건(i.e., S/L ratio = 본 연구 1 g/80 mL, Godoy et al. [16]의 연구 1 g/1000 mL)에서 기인한 것으로 판단된다.
Holmes et al. [9]의 연구에서는 PE에 Cd와 Pb에 대한 등온 흡착 실험을 동시에 수행하였는데(Table 4), 등온 흡착 실험에 사용한 Cd와 Pb의 초기농도(C0) 범위가 미량으로(0.005-3.00 nM)로 본 연구에서 사용한 농도 범위와 크게 달라(Cd C0 44,468-889,363 nM, Pb C0 24,131-482,625 nM) 비교 불가능하였다.
플라스틱 종류와 관계없이, Cd의 흡착량이 Pb보다 크고, Pb의 흡착세기가 Cd보다 큰 경향을 보였다. 일반적으로 이온반경(ionic radius)이 클수록 전자배치(electron configuration)가 불안정(labile)하며, 금속 양이온이 하전된 표면 작용기의 전기장에 반응하여 분극화(polarization)되는 경향이 더 크다. 이는 다양한 결합을 형성할 수 있는 전자배치의 뒤틀림(distortion)으로 이어질 수 있으므로, 이온반경이 클수록 금속 양이온의 상대적 결합강도(affinity)가 강하다고 볼 수 있다[29]. Cd은 0.095 nm, Pb은 0.119 nm의 이온반경을 가지므로[29], Pb의 상대적 결합강도가 Cd에 비해 강한 것을 추정할 수 있다. 또한 원자가 전자를 끌어 당기는 능력을 일컫는[30] 전기음성도(electronegativity)는 폴링 척도(Pauling scale)에 따르면 Cd는 1.65, Pb는 1.96으로 Pb가 Cd보다 상대적으로 센 결합을 형성할 수 있는 것을 추정할 수 있다. Pb에 대한 Langmuir 상수(KL), Temkin 상수(AT)가 Cd의 것보다 더 크게 나왔으며, Freundlich 상수(nF)는 Pb > Cd > 1의 경향을 나타내어, 이온반경과 전기음성도에 따른 상대적 결합강도 차이로부터 기인한 것으로 추정해볼 수 있다. 이 경향성은 Zou et al.의 결과와도 일치하였다[31].
Labib와 Williams는 PE의 point of zero charge (PZC)를 2.5로 보고한 바 있고[32], Beneš와 Paulenová는 함유한 첨가제(additive)의 종류와 양에 따라 PZC가 달라지기는 하나, 대략 3.5의 PVC에 대한 PZC를 보고한 바 있다[33]. 이는 두 종류의 플라스틱 모두 본 연구의 실험 pH 영역인 5.4-5.8에서 음전하를 띄고 있음을 의미한다. 이와 유사하게, Zou et al.은 PVC와 PE가 담긴 용액의 pH가 증가함에 따라 PVC와 PE 표면의 작용기(functional group)가 탈수소화(deprotonation)하여 표면전하가 음의 방향으로 증가하는 것을 관찰하였다[31]. 또한 용액의 pH가 증가할수록 플라스틱과 2가 양이온(Pb, Cd) 사이에 정전기 인력(electrostatic attraction)이 증가하는 것을 확인하였다[31]. 미세플라스틱은 매우 넓은 비표면적을 지니므로 환경 중 노출로 인해, 전술한 정전기적 반응에 의해 중금속과 같은 오염물질을 표면에 흡착할 수 있는 개연성이 있음을 보여준다. 또한 PVC와 PE의 분자 구조의 차이도 중금속 흡착능에 차이를 유발할 수 있다. 예를 들어, PVC의 경우 분자 구조 중 염소가 포함되어 있어 극성의 작용기를 가지게 되고, 이로 인해 중금속 흡착에 더 용이할 수 있다[34].
토양 중 플라스틱은 저장(storage) 또는 지체(retention)된다는 견해가 대부분이라고 하나, 최근 지하수에 미량의 플라스틱이 검출되어 지중환경에서 미세플라스틱의 이동 가능성이 있다는 견해가 제기되고 있다[35]. 미세플라스틱은 그 자체로도 환경 중의 위협일 뿐만 아니라, 환경 중 중금속과 같은 오염물질을 흡착하여 이동할 수 있으며[35], 또한 환경 조건 변화에 따라 다시 환경으로 용출시킬 개연성이 있으므로, 환경 중 미세플라스틱의 관리는 매우 중요하다.
4. 결 론
PVC와 PE 필름을 미세플라스틱으로 정의되는 크기로 준비하여 Pb와 Cd 흡착 특성을 알아본 결과, 실험에 사용한 PVC에 대한 Cd의 최대흡착량이 Pb의 최대흡착량보다 약 4배 가량 높았고, PE에 대한 Cd의 최대흡착량이 Pb의 최대흡착량보다 약 12-17배 가량 높았다. 또한 Langmuir, Freundlich, Temkin 세 가지 모델 중 Langmuir 모델과 Freundlich 모델이 이러한 흡착 결과를 더 잘 표현하였다. PVC와 PE의 Cd와 Pb같은 중금속의 흡착능은 토양 환경 중 플라스틱 필름이 환경 중 중금속의 거동에 영향을 줄 수 있음을 의미한다. 흡착을 통해 중금속의 이동성을 낮출 수도 있지만, 흡착 및 농축된 중금속이 환경조건 변화에 따라 다시 환경으로 용출될 개연성이 있다. 따라서 농업환경 내 미세플라스틱 필름의 관리를 위한 연구가 필요하다. 또한 본 연구결과는, 마스크와 같은 일회용 폐플라스틱 발생량의 급격한 증가가 사회적 이슈로 대두되고 있는 요즘, 다양한 폐플라스틱으로부터 발생할 수 있는 미세플라스틱의 지중환경 중 관리의 필요성에 대한 합리적 근거를 제공한 데에 그 의의가 있다.
Acknowledgements
본 연구는 한국연구재단의 연구비 지원으로 수행되었습니다(과제번호: NRF-2018R1C1B6002702). 실험준비에 도움을 준 한국외국어대학교 안세인, 전어진, 김수현, 문영진, 조찬희, 김영홍 학생에게 감사드립니다.
References
Notes
Declaration of Competing Interest
The authors declare that they have no known competing financial interests or personal relationships that could have appeared to influence the work reported in this paper.