응집효율 개선을 위한 저염기도 알루미늄계 응집제의 개발
Development of Low Basicity Aluminum Coagulants for Improving Coagulation Efficiency
Article information
Abstract
과적인 응집효과를 위하여 PACl의 염기도를 변화시키고 철염 응집제를 첨가제로 사용하여 새로운 저염기도 PACl인 PAIC (polyaluminum iron chloride) 응집제를 개발하였다. 낮은 염기도로 제조된 PAIC에 대한 Al(Ⅲ)종 분포는 염기도가 낮을수록 monomeric Al(Ⅲ)종은 증가하고 polymeric Al(Ⅲ)종은 감소하는 것으로 나타났다. 또한, PAIC는 응집실험에서 탁도와 유기물(UV254) 제거에 높은 효율을 나타내었다. 이는 PAIC 제조 시 첨가되는 첨가제와 낮은 염기도를 유지함에 따라 모노머 종이 증가하게 되고, 적정 응집 pH를 유지함으로써 유기물(UV254)제거 효과를 나타난 것으로 판단된다.
Trans Abstract
In this study, we have developed a low basicity PACl coagulants containing iron by changing the basicity of the existing PACl and using iron salt coagulant as an additive for effective coagulation. The analysis of Al(Ⅲ) hydrolysis species with low basicity PAIC showed that monomeric Al species were increased while polymeric Al species were decreased for the low basicity PAIC. Also, PAIC (polyaluminumiron chloride) coagulant showed high coagulation efficiency for turbidity and organic matters (UV254) in coagulation experiments. Therefore, it was concluded that the addition of monomeric PAIC increases the removal efficiency of organic matters (UV254) by keeping the coagulation pH at the optimum level.
1. 서 론
최근 들어 지구 온난화로 인한 이상기온 현상으로 발생되는 강우 형태는 국지성 호우로 변하고 있으며, 장기간에 걸쳐 가뭄 형태가 빈번하게 발생되고 있다. 발생되는 국지성 호우 대부분은 폭우성 강우 형태로 상수원의 탁도 증가를 유발하고 있으며, 장기간에 걸친 가뭄은 녹조발생의 원인이 되고 있다. 빈번하게 발생되는 조류대 발생으로 인해 각 정수장에서는 높은 pH로 인한 pH 조절과 함께 유기물 처리에 있어 많은 애로사항을 겪고 있으며, 강우에 따른 주기적인 고탁도 발생으로 정수과정에 많은 애로사항을 겪고 있는 실정이다. 또한 원수 수질에 따라 전하중하에 필요한 응집제 주입율은 달라지며, 최적의 응집효과를 나타내기 위해서는 적정한 응집제 주입율이 요구된다[1]. 이에 따라 각 정수장에서는 고탁도 및 유기물 증가에 대처하기 위해 alum이나 고분자알루미늄계의 무기응집제인 PACl의 사용이 증가되고 있는 실정이다[2]. 그러나 PACl 응집제의 사용 증가는 정수공정 중 후속공정인 여과지 부하 증가의 원인이 되며, 잔류 알루미늄이 증가되는 등 정수장 운영에 많은 애로사항을 야기함에 따라, 적정 응집제 주입량의 사용으로 고탁도 및 유기물 처리의 적정성을 유지하는 응집효과를 일으킬 수 있는 고효율성의 응집제 개발에 대한 필요성이 대두되고 있다.
각 정수장에서 많이 사용되고 있는 고분자알루미늄계 응집제인 PACl은 일정량의 수산화알루미늄과 염산을 이용하여 고온․고압하에서 중합반응에 의해 제조되며, 주요 성분물질인 Al2O3의 농도에 맞게 물로 희석되어 최종 산물로 만들어 진다. 제조된 PACl은 고분자성 알루미늄 종을 함유하고 있기 때문에 응집효율 개선 및 동절기의 저수온에서도 응집효율을 높이는 특징을 지니고 있다. 그러나, PACl에 함유되어 있는 OH-이온과 Al3+이온에 대한 몰 농도비[(OH-added)/(AlT)]인 염기도는 35~45%로 거의 일정하게 유지하고 있으므로 응집효과에 있어 응집효율의 한계를 가지고 있다. 또한 응집제 내에서의 가수분해 지속성으로 인하여 저장기간에 따른 수산화알루미늄[Al(OH)3]의 석출물이 발생되어 약품 주입배관에 쌓여 약품 주입에 장애가 되는 등 제품의 안정성 결여에 따른 유지관리 어려움 등의 단점을 지니고 있다.
국내의 경우에 있어서 염기도를 조절하기 위한 알카리제를 이용하여 염기도가 높은 알루미늄계 응집제[3~6]와 산을 이용하여 낮은 염기도를 유지하는 알루미늄계 응집제를 제조하여 사용하는 경우[7]도 있으나, 염기도를 조절하기 위한 첨가제에 따른 응집제에 대한 물리․화학적 특성 및 응집에 미치는 영향에 대해서는 규명되어 있지 않은 상태로 각 정수장에서 사용되고 있는 실정이다. 사용하는 응집제에 대한 물리․화학적 특성을 정확히 파악함으로서 제조자의 경우 응집제의 제조에 있어서 제조된 응집제의 특성을 정확히 판명함에 따라 제품 품질의 향상에 기여할 수 있으며, 사용자 측면에 있어서는 사용하는 응집제의 특성 파악에 따라 원수수질의 변동에 바로 대처함으로서 안정적인 수처리의 운영을 기할 수 있을 것으로 기대된다[8].
이에 따라 본 연구에서는 효과적인 응집효과를 이루기 위하여 기존의 PACl이 가지는 염기도를 변화시키고 철염 응집제를 첨가제로 사용하여 철을 함유하는 저염기도 PACl을 개발하여 응집제가 가지고 있는 화학적 특성 및 응집성능 등의 응집제 특성을 파악하고, 탁도 및 유기물에 대한 응집효과를 향상시키고, 응집제 석출물이 발생되지 않는 등 응집제의 안정성을 확보하고자 하였다. 본 연구에서 첨가제로 철염 응집제를 사용한 것은 철염 응집제의 특징[9~11]인 응집 pH 폭이 넓으며(pH 4.0~11.0), 응집물의 침강성이 우수하고 유기물 제거효율 및 동절기의 저온에서도 응집의 우수성을 지니고 있는 철염 응집제의 장점을 이용하여 상승효과를 유지하고자 하였다.
본 연구를 통해 정수처리공정에 있어서 상수원수 수질에 적합한 새로운 응집제를 사용함에 따라 응집효율의 개선을 이룸으로써 원활한 후속처리공정의 운전을 유지하며, 잔류알루미늄에 대한 위해성을 배제할 수 있고, 장기 보관에 따른 안정성을 확보할 수 있음에 따라 정수공정 유지관리의 안정성을 확보할 수 있을 것이라 기대된다.
2. 재료 및 방법
2.1 고효율성 수처리제(PAIC (Polyaluminum Iron Chloride))
본 연구에서 적용하고자 하는 저염기도를 유지하는 응집제(PAIC (Polyaluminum Iron Chloride), 이하 PAIC-08, PAIC-11, PAIC-13이라 칭한다.)는 상용화되어 있는 PACl (폴리염화알루미늄)에 산(HCl)과 철염응집제인 염화제이철(FeCl3)을 첨가제로 사용하여 기존의 고염기도 PACl보다 염기도가 낮은 저염기도를 함유하고 있는 무기응집제이다. PAIC의 응집제 특성 실험은 착화합제와 반응율에 기초한 Ferron 분석법[8,12~15]과 FT-IR을 이용하여 PAIC에 함유되어 있는 Al(Ⅲ)종의 특성을 분석하였다. 착화합제와 반응율에 기초한 Ferron 분석법에 있어서 Ferron 시약과 Al(Ⅲ)종과의 반응은 (1) monomeric Al(Ⅲ)종은 Ferron 시약과의 반응이 빨리 이루어져 반응 즉시 흡광도가 일정하게 되며 (2) polymeric Al(Ⅲ)종은 Ferron시약과 반응시간 동안 일정한 반응속도로 반응하여 평형에 이르면 일정한 흡광도를 유지하게 된다. (3) precipitate Al(Ⅲ)종은 ferron 시약과 반응하지 않는다는 근거로 실험을 하였다. 그리고 FT-IR은 FT-IR Spectrophotometer [model: Spectrum X (Perkin elmer, U.S.A.)]를 이용하였으며, 분석시료는 동결건조기 [model: SFDSM24L (Samwon freeze eng., Korea)]를 사용하여 5×10-4 mbar의 진공압력하의 -90℃에서 건조된 것으로서 건조된 시료를 분쇄하여 시료 1 mg에 대한 KBr powder를 200 mg 투입하여 30초 동안 700 kgf/cm2의 압력을 가해 디스크화하여 응집제 내 성분변화에 대하여 분석을 하였다.
2.2. 응집실험
PAIC에 대한 응집성능을 파악하기 위하여 대조군으로 정수장에서 많이 사용하고 있는 PACl 11% (as Al2O3)와 PAC 17% (as Al2O3)를 사용하였으며, 제조된 PAIC에 정수용 응집제로 활용하기 위해 낙동강 상수원수를 이용하여 응집특성을 파악하였다. 응집특성을 파악하기 위해 사용된 시수로는 부산 D 정수장의 취수원인 M 취수장의 상수원수를 사용하였으며, 수질특성을 파악하기 위한 수질항목별 특성을 Table 1에 나타내었다. 본 연구에서 사용된 상수원수의 수질은 실험기간 중 비교적 안정한 양상을 나타내고 있었다.
응집실험에 사용된 Jar tester (Phipps & Bird사)는 6개의 교반장치를 갖춘 것으로 paddle (two-blade)의 크기는 2.5 W×7.5 L cm이다. Jar-test에서 사용된 Jar는 2 ℓ 용량의 사각형 Jar를 사용하였다. 응집 교반속도(rpm)는 급속혼화 250 rpm (G = 550 sec-1 at 20℃), 완속혼화 30 rpm (G = 22 sec-1 at 20℃)이며, 교반시간은 각각 1분, 30분으로 유지하였다. 이때 교반 조건은 충분한 예비실험을 거친 후 최적의 조건을 선정하였다. 교반 후 침전시간은 30분으로 하였으며 침전 후 수면아래 10 cm지점에 위치한 sampling tap을 통하여 채수한 다음 수질분석을 실시하였다.
3. 결과 및 고찰
3.1. PAIC (Polyaluminum Iron Chloride)의 특성
수처리제의 기준과 규격 및 표시기준[17]에 의한 폴리염화알루미늄(PACl)의 분석방법에 따라 PAIC의 주성분을 이루고 있는 Al2O3, pH, 염기도 및 3가철의 분석 결과와 응집성능을 파악하기 위하여 대조군으로 PACl 11%와 PACl 17%의 분석결과는 Table 3과 같이 나타났다.
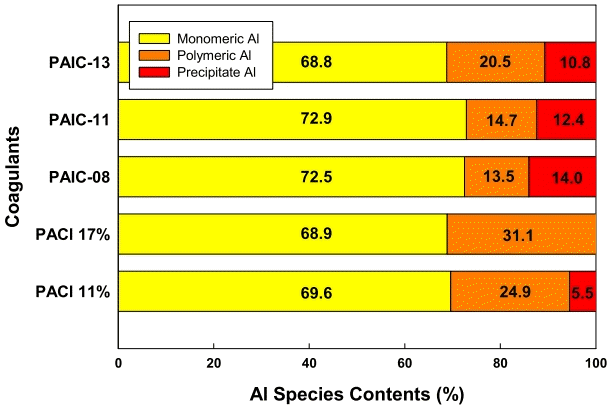
또한 수처리 현장에서 사용되고 있는 PACl 11%와 PACl 17% 및 제조된 저염기도 응집제인 PAIC-08, PAIC-11, PAIC-13에 대하여 Ferron 분석법에 의한 성분 특성결과는 Fig. 1과 같이 나타났다.
Fig. 1은 본 연구에 사용된 Al(Ⅲ)계 무기응집제 종류에 따른 알루미늄 종 분포를 나타낸 그림으로 PACl 11%의 경우 monomeric Al(Ⅲ)종은 69.6%, polymeric Al(Ⅲ)종은 24.9%, precipitate Al(Ⅲ)종은 5.5%로 나타났으며, PACl 17%는 monomeric Al(Ⅲ)종은 68.9%, polymeric Al(Ⅲ)종은 31.1%, precipitate Al(Ⅲ)종은 0%로 나타났다. PACl 11%의 경우 PACl 17% 보다 precipitate Al(Ⅲ)종이 많이 나타나고 있는데, 이는 응집제 내에 함유하고 있는 Al의 함량이 높은 것으로서 응집제 제조 시 Al 함량을 다량 함유하도록 제조함에 따라 monomeric Al(Ⅲ)종이 precipitate Al(Ⅲ)종으로 바로 전이가 일어난 것으로 판단된다.
저염기도 응집제인 PAIC에 대한 알루미늄 종 분포는, PAIC-08의 경우 monomeric Al(Ⅲ)종은 72.5%, polymeric Al(Ⅲ)종은 13.5%, precipitate Al(Ⅲ)종은 14.0%로 나타났으며, PAIC-11은 monomeric Al(Ⅲ)종은 72.9%, polymeric Al(Ⅲ)종은 14.7%, precipitate Al(Ⅲ)종은 12.4%로 나타났다. 그리고 PAIC-13의 경우에서는 monomeric Al(Ⅲ)종이 68.8%, polymeric Al(Ⅲ)종은 20.5%, precipitate Al(Ⅲ)종은 10.8%로 나타났다. PAIC의 경우에서는 저염기도 응집제 제조 시 첨가되는 산(HCl) 및 염화제이철의 첨가에 따라 저염기도를 유지하게 되고, 이에 따라 monomeric Al(Ⅲ)종이 증가되며, 이에 반해 polymeric Al(Ⅲ)이 줄어드는 것으로 나타났다. Han의 연구[8]에 의하면 Ferron 분석법과 Al-NMR 분석법에 따른 종의 분포를 비교한 결과 Ferron 분석법과 Al-NMR 분석법 모두 r 값의 증가에 따라 monomeric Al(Ⅲ)종은 감소하고, polymeric Al(Ⅲ)종과 precipitate Al(Ⅲ)종은 증가하는 것으로 나타났으나, 높은 r 값에 있어서 polymeric Al(Ⅲ)종은 감소하는 것으로 나타났다. 이는 형성된 polymeric Al(Ⅲ)종이 precipitate Al(Ⅲ)종으로 전이가 일어남에 따른 것이라 하였다. 이상의 결과 Ferron 분석법과 Al-NMR 분석법의 결과는 서로 유사한 경향을 나타내어, 분석에 따른 서로의 신뢰성은 유지되는 것으로 판단된다.
Fig. 2은 제조되는 응집제 내 알루미늄의 함량이 유사한 PACl 11%와 PAIC-11의 경우 FT-IR의 분석을 통해 응집제 내 성분의 변화에 대한 비교실험의 실시 결과를 나타낸 것이다. PACl 11%에 대한 FT-IR의 변화를 살펴보면 1,600, 2,500 및 3,300 cm-1의 영역에서 흡수 band가 형성되었으며, 2,500 cm-1에서의 흡수 band는 약하게 나타났다. 그런데 PAIC-11의 경우에서는 나타난 흡수 band는 1,300, 1,400, 1,600, 2,500 및 3,000 cm-1에서 나타났으며, PACl 11%에서 나타나지 않은 1,300과 1,400 cm-1에서 새로운 흡수 band가 나타났다. 또한 PACl 11%의 3,300 cm-1에서 나타난 흡수 band가 3,000 cm-1으로 이동되어 흡수 band를 형성시켜 나타났다. 이는 첨가제로 사용된 염화제이철의 철이 Fe-O의 형태로 응집제 내 가수분해에 따른 것으로 판단된다. 그리고 1600 cm-1의 영역에 있어서 나타나는 흡수 band는 물분자의 존재를 나타낸 것이다.
Ishikawa 등의 연구[18]에 의하면 FeCl3 용액에 NaOH를 첨가한 실험에서 r 값의 증가에 따라 FT-IR의 분석결과 monomeric Fe(Ⅲ)종은 감소하고 r=2.0 이상의 경우에서는 monomeric Fe(Ⅲ)종이 나타나지 않고 동시에 Fe3O4와 α-FeOOH가 나타난다고 하였는데, 이는 monomeric Fe(Ⅲ)종이 Fe3O4와 α-FeOOH로의 전이가 이루어져 나타났기 때문이라 하였다. 또한 Šarić 등[19]은 Fe(NO3)3를 이용하여 Fe(Ⅲ)종에 대한 FT-IR 분석 결과 800~892 cm-1의 영역에서 Fe-O-H의 구조를 나타내는 α-FeOOH의 흡수 band를 확인하였으며, 630 cm-1의 영역에서 Fe-O 구조의 Fe2O3 형태 흡수 band를 확인하였다.
현재 정수장에서 많이 사용되고 있는 PACl 11%와 PACl 17%의 경우 용액 내에서 저장기간의 경과에 따라 알루미늄의 가수분해 진행으로 인하여 precipitate Al(Ⅲ)종이 증가되어 고형물의 형태로 침전되어 배관 막힘의 원인으로 유지관리에 많은 문제점으로 제기되고 있다. 이에 반해 저염기도 응집제의 경우 제조 시 첨가물에 의해 monomeric Al(Ⅲ)종의 증가로 인하여 저장기간의 진행에 따라 용액 내 polymeric Al(Ⅲ)종으로 가수분해가 이루어져 고형물 형태의 precipitate Al(Ⅲ)종으로의 전이가 매우 느리게 이루어진다. 이에 따라 저염기도를 가진 PAIC 응집제의 경우 저장기간에 따른 안정성을 유지할 수가 있다. 첨가되는 염기의 OH-이온이 알루미늄 이온과의 착화합물 형성에 의한 고분자성 Al 성분으로 전이됨에 따른 결과로서, 초기 Al(Ⅲ)염에 대한 염기의 첨가량 및 첨가율은 고분자성 알루미늄 응집제의 제조에 있어 매우 중요한 인자라 알려져 있다[12,20,21].
Fig. 3은 응집제의 보관기간 중 응집제의 성분변화를 파악하기 위하여 제조된 저염기도 응집제인 PAIC-08, PAIC-11 및 PAIC-13 3종류에 대해 제조 후 Al(Ⅲ) 가수분해종의 분포와 제조 6개월 후의 Al(Ⅲ) 가수분해종의 분포를 비교하여 나타낸 것이다. Fig. 3에서와 같이 저염기도 응집제인 PAIC-08, PAIC-11 및 PAIC-13 3종류의 경우 Al(Ⅲ) 가수분해종의 변화는 monomeric Al(Ⅲ)종이 소량 줄어들고, polymeric Al(Ⅲ)종과 precipitate Al(Ⅲ)종이 소량 증가하는 것으로 나타나, 응집제의 저장기간에 따른 안정성의 확보가 용이할 것으로 판단된다. Al(Ⅲ) 용액의 중화정도(r)와 염기의 주입속도, 숙성과정 등을 적절히 제어할 수 있다면 다양한 형태의 안정성이 높은 Al(Ⅲ) polymer를 제조할 수 있으며 원수의 수질특성에 적합한 PACl의 제조 또한 가능할 것이다[22,23].
3.2. PAIC 응집특성
응집실험에 사용된 응집제는 제조된 저염기도 응집제인 PAIC-08, PAIC-11 및 PAIC-13 3종류와 대조군으로 정수장에서 많이 사용되고 있는 PACl 11%와 PACl 17%를 이용하였다. 그리고 응집실험은 응집제의 주성분인 알루미늄 함량의 유사성을 고려하여 PAIC-08, PAIC-11 와 PACl 11%를 상호 비교하였으며 또한 PAIC-13과 PACl 17%를 서로 비교하였다. 응집실험에 앞서 제조된 저염기도 응집제인 PAIC와 정수장에서 많이 사용하고 있는 PACl에 대한 응집 pH의 변화를 살펴보았다.
Fig. 4는 PAIC-08, PAIC-11과 PACl 11%에 대한 응집 pH 변화를 나타낸 것이고, Fig. 5은 PAIC-13과 PACl 17%에 대한 응집 pH 변화를 나타낸 것이다. PAIC-08, PAIC-11과 PACl 11%에 대한 응집 pH 변화를 나타낸 Fig. 4의 결과에서 나타난 바와 같이 동일한 Al2O3 함량을 유지하는 PAIC-11과 PACl 11%의 경우, 저염기도를 유지하고 있는 PAIC-11이 PACl 11% 보다 응집 pH에 민감한 것으로 나타났다. 또한 Al2O3 함량이 낮은 PAIC-08의 경우 PACl 11%와 응집 pH 변화폭이 유사한 결과를 나타내었다. pH 5.6~6.5의 응집 pH 조건에서 유기물의 응집효과가 높은 점을 감안할 때, 저염기도의 응집제의 경우에서 우수한 유기물 제거가 이루어질 수 있을 것으로 판단된다. Fig. 5의 PAIC-13과 PACl 17%에 대한 응집 pH 변화에서도 저염기도를 유지하는 PAIC-13의 경우 PACl 17%보다 응집 pH에 민감한 것으로 나타났으며, 이에 따라 유기물 제거에 저염기도 응집제인 PAIC의 경우에 있어서 다소 우수한 유기물 제거가 이루어질 수 있을 것으로 판단하였다[24~26]. 이와 같은 결론은 UV254를 통한 유기물에 대한 응집실험에서 확인할 수 있었다.
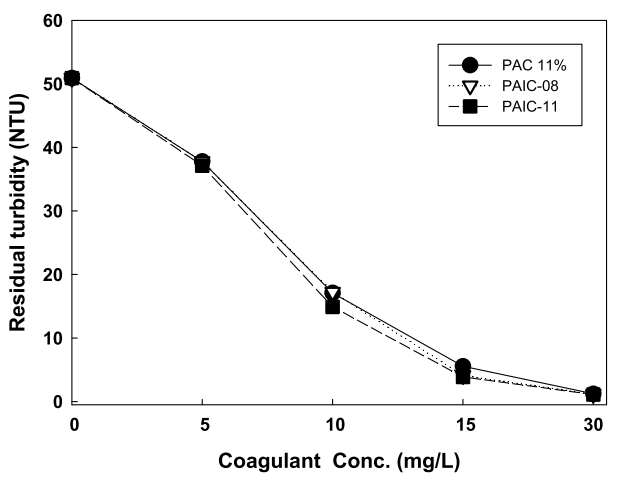
Fig. 6과 Fig. 7은 응집제 주입량에 따른 탁도의 변화를 나타낸 것으로서 응집실험 후 침전 상징액에 대한 탁도를 나타낸 것이다. Fig. 6은 PAIC-08, PAIC-11과 PACl 11%를 사용한 탁도 실험 결과로 PAIC-08의 경우 Al2O3 함량 8% 정도를 함유하고 있음에도 불구하고 Al2O3 함량이 11%를 함유하고 있는 PACl 11% 와 유사한 탁도 제거효율을 나타내고 있었다. 그리고 PACl 11%와 유사한 Al2O3 함량을 유지하고 있는 PAIC-11의 경우 PACl 11% 보다는 다소 높은 탁도 제거효율을 나타내었다. 이와 같이 Al2O3 함량이 낮음에도 불구하고 유사한 탁도 제거효과가 나타나고(PAIC-08), Al2O3 함량을 유사하게 유지하는 경우(PAIC-11) 우수한 탁도 제거 효과를 나타내는 것은 PAIC 제조 시 첨가되는 첨가제에 의한 저염기도의 유지에 따라 모노머 종의 증가하게 되고, 이로 인해 응집 시 전하중화 능력이 우수하게 작용하여 나타난 것으로 판단된다. 탁도의 경우 고분자성 Al종을 주종으로 하고 있는 PACl 응집제의 경우에서 효과적으로 나타났다. 이는 PACl 응집제에 함유된 고분자성 Al종이 가지는 높은 전하중화 능력에 의한 것으로 판단된다[27].
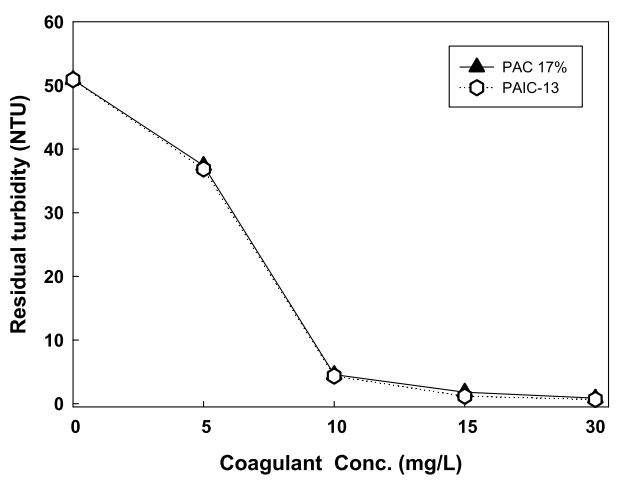
Fig. 7은 PAIC-13과 PACl 17%를 사용한 탁도 실험 결과로 Fig. 7에 나타난 바와 같이, PAIC-13의 경우 Al2O3 함량 13% 정도를 함유하고 있음에도 불구하고 Al2O3 함량이 17%를 함유하고 있는 PACl 17%의 탁도 제거효율과 유사하게 나타났다. 이는 Fig. 6의 실험결과에서와 같이 PAIC 제조 시 첨가되는 첨가제에 의한 저염기도의 유지에 따라 모노머 종의 증가하게 되고, 이로 인해 응집 시 전하중화 능력이 우수하게 작용하여 나타난 것으로 판단된다. 이에 따라 기존에 사용되고 있는 PACl에 대해 저염기도 응집제인 PAIC의 사용에 따라 응집 반응에서 작용하는 알루미늄의 저감으로 잔류알루미늄에 대한 위해성을 해소할 수 있으며, 안정적인 먹는물 관리가 이루어질 수 있을 것으로 판단된다.
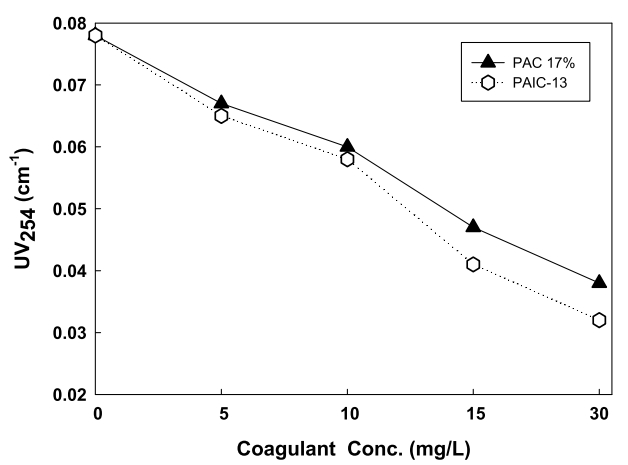
Fig. 8과 Fig. 9는 응집제 주입량에 따른 유기물농도(UV254)의 변화를 나타낸 것으로서 응집실험 후 침전 상징액에 대한 UV254 실험 결과를 나타낸 것이다. Fig. 8은 PAIC-08, PAIC-11과 PACl 11%를 사용한 유기물(UV254) 실험 결과로 Fig. 8에 나타난 바와 같이, PAIC-08, PAIC-11 모두 PACl 11%보다 우수한 유기물(UV254) 제거 효과를 나타내었다. 이는 PAIC 제조 시 첨가되는 첨가제에 의한 저염기도의 유지에 따라 모노머 종의 증가하게 되고, 이로 인해 응집 시 전하중화 능력이 우수한 응집작용을 나타내었으며, 응집제 주입에 따라 적정 응집 pH를 유지함에 따라 우수한 유기물(UV254) 제거효율이 나타난 것으로 판단된다. 또한 Fig. 9에서 나타난 바와 같이 PAIC-13과 PACl 17%를 사용한 유기물(UV254) 실험 결과에서도 저염기도 응집제인 PAIC 경우 Al2O3 함량 17%로 높게 유지하는 PACl 17% 보다 우수한 유기물(UV254) 제거효율을 나타내었다. 이에 따라 기존에 사용되고 있는 PACl에 대해 저염기도 응집제인 PAIC의 사용에 따라 응집 반응에서 작용하는 알루미늄의 저감으로 잔류알루미늄에 대한 위해성을 해소할 수 있으며, 안정적인 탁도 및 유기물(UV254) 제거 효과를 이룰 수 있을 것으로 판단된다.
4. 결 론
정수처리 시 응집효율의 증가와 응집제의 안정성 확보를 위하여 개발된 저염기도 응집제인 PAIC에 대한 연구를 수행한 결과 다음과 같은 결론을 도출할 수 있었다.
1. 저염기도 응집제인 PAIC에 대한 알루미늄 종 분포는, PAIC-08의 경우 monomeric Al(Ⅲ)종은 72.5%, polymeric Al(Ⅲ)종은 13.5%, precipitate Al(Ⅲ)종은 14.0%로 나타났으며, PAIC-11은 monomeric Al(Ⅲ)종은 72.9%, polymeric Al(Ⅲ)종은 14.7%, precipitate Al(Ⅲ)종은 12.4%로 나타났다. 그리고 PAIC-13의 경우에서는 monomeric Al(Ⅲ)종이 68.8%, polymeric Al(Ⅲ)종은 20.5%, precipitate Al(Ⅲ)종은 10.8%로 나타났다. PAIC 응집제 저염기도를 유지함으로써 monomeric Al(Ⅲ)종이 증가되며, 이에 반해 polymeric Al(Ⅲ)이 줄어드는 것으로 나타났다.
2. FT-IR의 분석을 통해 응집제 내 성분 변화에서 1,600, 2,500 및 3,300 cm-1의 영역에서 흡수 band가 형성된 PACl 11%에 대해 PAIC-11의 경우에서는 나타난 흡수 band는 1,300, 1,400, 1,600, 2,500 및 3,000 cm-1에서 나타났으며, PACl 11%에서 나타나지 않은 1,300과 1,400 cm-1에서 새로운 흡수 band가 나타났다. 또한 PACl 11%의 3,300 cm-1에서 나타난 흡수 band가 3,000 cm-1으로 이동되어 흡수 band를 형성시켜 나타났다. 이는 첨가제로 사용된 염화제이철의 철이 Fe-O의 형태로 응집제내 가수분해에 따른 것으로 판단된다.
3. 저염기도 응집제인 PAIC와 PACl에 대한 응집 pH 변화를 살펴본 결과, 저염기도를 유지하는 PAIC 응집제의 경우 응집 pH 변화에 민감하게 작용하는 것으로 나타났다. 또한, PAIC의 Al2O3 함량이 낮음에도 불구하고 PAIC와 PACl의 탁도 제거효과는 유사하게 나타났다. PAIC 제조 시 첨가되는 첨가제에 의한 저염기도의 유지에 따라 모노머 종의 증가하게 되고, 이로 인해 응집 시 전하중화 능력이 우수한 응집작용을 나타내었으며, 응집제 주입에 따라 적정 응집 pH를 유지함에 따라 우수한 유기물(UV254) 제거효율이 나타난 것으로 판단된다.
Acknowledgements
이 논문은 2017학년도 부경대학교 연구년[Ⅱ] 교수 지원사업에 의하여 연구되었음(C-D-2017-0976).