유기산, 산화음이온 및 금속 산화물 간의 근권 내 상호작용 연구를 위한 계산화학과 적외선 분광학에 관한 총설: 기본적인 원리와 스펙트럼 처리
Reviews in Infrared Spectroscopy and Computational Chemistry to Reveal Rhizospheric Interactions among Organic Acids, Oxyanions and Metal oxides: Fundamental Principles and Spectrum Processing
Article information
Abstract
이 총설은 근권에서 일어나는 유기산, 산화음이온, 그리고 금속 산화물 간의 상호작용을 이해하는데 활용하고 있는 적외선 분광학과 계산화학에 대한 기본적 원리, 역사, 적용 분야, 장점, 그리고 단점에 대해 최근 연구들을 바탕으로 요약하였다. 식물의 유기산과 금속 산화물은 토양 환경에서 산화음이온의 유효도와 이동성을 결정하기 때문에, 산화음이온의 환경내 거동을 이해하기 위해서는 계면에서 이들의 상호작용을 이해하는 것이 중요하다. 적외선 분광학의 감쇠 전반사 기법은 계면에서 일어나는 화학적인 반응을 측정하는 강력한 도구이지만, 광학적 특성들이 실험 설계와 대상에 따라 매우 다르게 나타날 수 있으므로 이를 이용한 측정은 까다롭다. 전반사에 의해 발생하는 소멸파의 침투 깊이가 가장 중요한 매개 변수인데, 침투 깊이는 적외선의 입사각과 대상 파장, 그리고 매질의 굴절률에 따라 결정된다. 또한, 적외선을 이용하여 계면에서의 화학반응을 분석할 때 겹쳐서 발생하는 스펙트럼을 해석하는 것 역시 큰 문제이기 때문에, 겹쳐 나타나는 스펙트럼을 해석하여 밴드를 검출하고, 이 스펙트럼을 deconvolution하는 것이 필수적이다. 본 총설에서는 적외선스펙트럼을 처리하는 기본적인 절차와, 밴드 검출에 사용하는 네가지 방법인 도함수 분광학과 이차 상관 분광학, multivariate curve resolution, 계산 화학을 액체상에 존재하는 인산염 종분화로 설명하였다. 스펙트럼 처리와 계산 화학을 조합하였을 때 간단한 계에서 측정한 겹쳐진 스펙트럼 결과는 해석할 수 있었지만, 자연과 같은 복잡계에서 측정한 겹쳐진 스펙트럼을 해석하는 것은 여전히 불가능한 상황이다. 그러나 향후 분석 및 신호 처리 기술 발달에 따라 복잡계뿐만 아니라 자연계에서 일어나는 계면 반응을 해석할 수 있을 것으로 기대한다.
Trans Abstract
This review summarizes advantage and limitation in infrared spectroscopy and computational chemistry to understand rhizospheric interaction among organic acids, oxyanions and metal oxides. Since organic acids and metal oxides determine dynamics of oxyanions in the soil environment, knowledge of fundamental mechanisms is a prerequisite for understanding the interactions at soil-water interface. Attenuated total reflectance-fourier transform infrared spectroscopy (ATR-FTIR) is a powerful tool to measure the interfacial reactions. However, the ATR-FTIR measurements are abstruse, because the optical characteristics for measurements are variable depending on the experimental setup. In addition, spectral overlapping is a primary obstacle to the analysis of the interfacial reaction; thus, it is essential to detect and to deconvolute bands for signal interpretation. In this review, we expained the fundamental principle for spectrum processing, and four band identification methods, such as derivative spectroscopy, two-dimension correlation spectroscopy, multivariate curve resolution, and computational chemistry with example of aqueous phosphate speciation. As a result, spectrum processing and computational chemistry improved interpretation and spectral deconvolution of overlapped spectra in relatively simple systems, but it was still unsatisfactory for the problems in more complexed system like nature. Nevertheless, we believed that our challenge would contribute practically to develop adequate analytical procedure, signal processing and protocols that could help to improve interpretation and to understand the interfacial interactions of oxyanions in natural systems.
1. 서 론
산화음이온(oxyanion)은 하나 이상의 산소를 포함하는 음이온을 통칭하는 용어로, 탄산염(carbonate), 질산염(nitrate), 인산염(phosphate), 규산염(silicate) 및 황산염(sulfate) 등이 대표적인 산화음이온이다. 비산염(arsenate). 안티몬산염(antimonate), 염소산염(chlorate), 셀렌산염(selenate), 텔레산염(tellurate) 등과 같이 미량 원소로 이루어진 산화음이온도 보고되었으며, 이들은 수소 이온, 전자, 그리고 산소 농도와 같은 환경 조건에 따라 다양한 형태로 종분화(speciation)한다[1,2]. 산화음이온으로 존재하는 여러 원소 중 질소는 질산염과 아질산염(nitrite), 두가지의 산화음이온으로 존재하는데, 토양환경에 따라 종분화가 일어나며, 이때 단순히 산화음이온의 구성성분만 바뀌는 것이 아니라 산화음이온의 안정도(stability)와 토양에 대한 친화도(affinity)에 영향을 주어 토양 환경 내 거동이 변화한다[3,4].
토양은 다양한 물질의 집합체로, 일반적으로 층상규산염 광물과 금속 산화물(metal oxide), 그리고 유기물로 이루어져 있다. Al, Fe 및 Mn 등은 금속 산화물의 주요 구성성분이며, 이들의 결정 형태에 따라 일반적으로 5 - 9.1의 영점전하를 가지기 때문에, 일반적인 토양의 pH 범위인 5.5 - 7.5에서는 표면이 양전하를 띄어 음전하를 갖는 산화음이온을 정전기적 인력에 의해 흡착한다[5~7]. 따라서 산화음이온은 이온 결합에 의해 토양입자에 흡착할 뿐만 아니라 다양한 양이온과 공유 결합하여 광물 형태로 침전되어 토양에 존재하는데, 이러한 반응들은 산화음이온이 생물에게 흡수되는 비율인, 생물유효도(bioavailability)를 결정한다[2,8]. 그 중에서 질소(N)와 인(P)은 대부분의 토양 환경에서 식물의 생장을 결정하는 제한요인으로, 이들의 유효도는 식물의 관점에서 토양 생물의 생활사를 결정한다.
식물은 뿌리를 통해 토양의 근권부(rhizosphere)에 존재하는 산화음이온을 특정 운반체(transporter)를 통하여 흡수하기 때문에, 토양에서 이들의 존재 형태에 따라 흡수할 수 있는 영양원소의 양이 결정된다[9,10]. 식물은 이러한 환경적 제약을 극복하기 위하여 다양한 흡수기작을 발달시켜왔는데, N은 질산성 질소뿐만 아니라 암모니아성 질소로 흡수하거나, 뿌리혹박테리아에 의한 질소고정 등 다양한 경로를 통하여 흡수한다[10,11]. 한편, P는 자연계에서의 순환에 따라 토양 환경 내로 이동되어 용액 상에서는 산화음이온 형태로 존재하지만, 다가 양이온과 쉽게 결합하여 침전되기 때문에(예를 들면 칼슘과 결합한 apatite, 철과 결합한 vivianite), 인의 유효도는 식물의 생장을 결정한다[2,12,13]. 다양한 속효성 화학 비료의 개발과 사용량이 증가하면서 N과 P의 부족은 더 이상 작물의 생장 제한요인이 아니기 때문에, 토양 연구 및 관리를 통하여 최적의 생물유효도를 유지하기보다 과다하게 많은 양의 비료를 투입하여, 작물의 성장에 필요한 양을 과다 충족시키는 방향으로 관행농업이 발전하였다[14,15]. 그 결과, 토양에 과량으로 존재하는 N과 P는 토양환경변화에 따라 수계로 유출되어 심각한 환경 문제를 야기하는 실정이다[15,16]. N은 암모니아휘산과 탈질 반응에 의해 기체로 대기에 배출되거나, 산화조건에서 질산염이나 아질산염과 같은 산화음이온으로 존재하는 반면, pH가 낮거나 혐기조건에서는 질소는 양이온인 암모니아 형태로 존재하는 등 다양한 경로를 통하여 이동한다[17]. 반면, P는 대부분이 산화음이온인 인산염 형태로 존재하거나 침전되어 결정형태로 존재하고, 토양수분의 이동에 따라 수계로 이동하여 부영양화와 같은 환경문제를 일으키는 주원인으로 밝혀지고 있다[18,19]. 이러한 환경 문제를 해결하기 위하여 N과 P의 적정 생물유효도를 유지하는 것은 매우 중요한 일이지만, 토양의 이질성(heterogeneity)에 의해 나타나는 복잡성은 이들에 대한 근본적인 이해를 어렵게 하고 있다.
최근 연구에서, 식물은 다양한 뿌리 삼출액을 분비하고, 뿌리 삼출액에 포함되어 있는 유기산은 금속산화물에 흡착되어 있는 산화음이온과 경쟁하여 탈착시키거나, 산화음이온이 포함되어 있는 광물을 해리시켜 생물유효도를 증가시킨다고 보고하고 있지만, 이에 대한 직접적인 증거를 제시하지 못하고 있다[20~22]. 그 원인은 크게 세가지로 제시할 수 있는데, 첫번째로는 기존의 토양분석은 건조시료를 바탕으로 이루어지기 때문이다. 생물이 쉽게 이용할 수 있는 인산염은 극히 소량으로 존재하며, 토양 건조 과정에서 다가 양이온과 결합하여 침전하거나 인산염이 결합할 수 있는 금속 산화물을 형성하기 때문에, 건조시료와 습윤시료 간에 인산염의 존재형태가 달라지게 된다[23,24]. 두번째로는 인산은 금속산화물에 대부분 흡착되어 있다고 알려져 있어, 토양의 이질성과 상대적으로 낮은 농도가 결합구조 분석을 매우 어렵게 하기 때문이다. 세번째로는 방사광을 이용하는 X선 흡수 미세구조 분광법(X-ray absorption fine structure spectroscopy)을 통한 결합 구조 측정이 있지만, X선은 유기산을 빠르게 분해시키기 때문에 유기산과 산화음이온의 금속 산화물에 대한 흡착과정에서 발생하는 현상을 관찰하기에는 이 역시 부적합하다. 이러한 이유로 유기산과 산화음이온 간 금속산화물 표면에서 일어나는 화학현상을 직접적으로 측정하는 것은 매우 어렵다.
X선을 이용한 분석의 한계를 극복하기 위하여 라만, 적외선, 전자 상자성 공명, 그리고 핵자기 공명 분광법 등의 분석법이 제시되었는데, 그 중에서 감쇠 전반사-퓨리에 변환 적외선 분광법(Attenuated total reflectance-fourier transformed infrared spectroscopy, 이하 ATR-FTIR)은 in situ에서 실시간으로 고체와 액체 계면에서 일어나는 진동에너지 변화를 측정할 수 있다[25,26]. 결합구조와 결합구조를 이루고 있는 원자의 질량에 따라 적외선 흡광이 나타나는데, 문제는 진동방식, 즉 시스템의 복잡성, 대상 물질의 유사성에 따라 흡광이 측정되는 밴드가 쉽게 겹쳐진다는 단점이 있다[27]. 과거에는 이렇게 겹쳐진 스펙트럼을 해석하는 것은 거의 불가능한 일이였으나, 이러한 단점을 극복하고자 동위원소를 이용하여 대상 원자의 질량을 변화시켜 흡광 파수를 조절하거나[28], 시스템의 복잡성을 단순화하는 방법을 통하여 계면에서의 결합 구조를 해석하는 방법이 시도되었지만, 여전히 겹쳐진 스펙트럼을 해석하기에는 문제점이 많았다.
그러나, 21세기에 들어오면서 고성능 컴퓨터 발달과 기존의 Schrödinger의 양자역학에 기초한 근사 계산 모델들이 제시되었고, 이는 복잡한 분자궤도함수를 이론적으로 계산할 수 있게 하였다. 최근에는 다양한 계산화학 소프트웨어가 무상으로 배포되거나 상업 목적으로 개발되어, 컴퓨터를 이용한 연산과 계산화학에 대한 기본적인 지식만으로도 쉽게 전자구조이론에 접근할 수 있게 되었으며, 이론적으로 물질이나 결합구조의 특징을 계산하는 것이 가능하게 되었다[29,30]. 이러한 계산화학의 발달은 ATR-FTIR을 이용한 결합구조 분석에 매우 중요하게 기여하였는데, 그 이유는 이론적인 계산을 통하여 결합구조의 분광학적 특성을 알 수 있기 때문이다. 그 결과로, 다양한 결합구조로 인해 겹쳐져 나타나는 적외선 흡광 스펙트럼의 여러 진동방식에 대한 정보를 이론적으로 구할 수 있게 되었다[29,31].
최근에는 적외선 분광학과 계산화학을 이용하여 계면에서의 결합구조를 해석하고자 하는 연구가 급증하고 있으며, 컴퓨터의 발달과 정교한 전자구조이론이 제시됨에 따라 수계의 부영양화를 일으키는 산화음이온의 토양 내 거동에 관한 기작 연구에 대한 필요성 역시 증가하고 있다. 따라서 본 총설에서는 계산화학과 ATR-FTIR를 이용하여 근권 내 상호작용 연구를 위한 기본적인 원리, 역사, 적용 분야, 장점, 그리고 단점에 대해서 광범위하게 고찰하였다. 특히, 겹쳐서 나타나는 스펙트럼을 해석하는 네가지 방법; 1)도함수 분광학, 2)이차 상관 분광학, 3) multivariate curve resolution, 4) 계산화학을 액체상에 존재하는 인산염 종분화를 예로 들어서 설명하였다.
2. 계산화학을 이용한 이론적 계산
2.1. 계산화학의 정의와 역사
계산화학은 이론화학의 한 분야로 컴퓨터 시물레이션을 이용하여 화학적 문제를 해결하는 학문이다. Heitler와 London이 1927년 최초로 이론적 계산을 수행한 이래, 1940년대에 컴퓨터 기술이 발전함에 따라 실제 적용 가능한 학문으로 발전하였다. 1956년 미국 MIT 대학에서 첫번째로 ab initio Hartree-Fock 방법을 이용한 계산을, 1964년에는 Hückel 방법에 따른 경험적인 계산을 수행하였으며, 1970년대부터 현재까지 계산 화학분야의 다양한 컴퓨터 프로그램이 개발 되고 있다. 1998년 노벨 화학상은 밀도 함수 이론과 양자 화학에서 계산 방법을 발달시킨 Kohn과 Pople에게 수여되었는데, 이는 계산화학이라는 분야가 하나의 학문으로 정착되었기 때문이다. 2013년에 복잡화학계에서 다중스케일 모델을 개발하고 발달시킨 공로로 Karplus와 Levitt, Warshel에게 노벨 화학상이 수여되었는데, 이는 계산화학이 주목받는 학문분야로 인식된 결과이다.
2.2. 계산화학의 종류 및 원리
Schrödinger의 방정식을 수학적으로 풀면, 다전자 시스템에서 전자의 파동성을 이해할 수 있는데, 이를 풀기위해서는 많은 연산과 여러 가지 근사 방법을 사용한다[32]. 이 때 사용하는 근사 방법에 따라 크게 ab initio 방법과 경험적(empirical) 방법으로 분류한다. 이 두 방법의 가장 큰 차이는 분자의 궤도함수(orbital)를 계산하는 식에서 경험적 또는 반경험적 매개변수를 사용하는가에 따라 달라지는데, 매개변수를 사용하지 않는 경우에는 ab initio 방법이라 부르고, 사용하는 경우에는 경험적 방법이라 부른다[33]. ab initio 방법에는 대표적으로 Hartree Fock 분자궤도이론(이하 HF)과 밀도범함수이론(이하 DFT) 등이 있는데, 모두 자가 모순없는 장(self-consistent field) 절차를 사용하여 계산한다. 예로 들면, 전자의 궤도함수를 가정한 다음 하나의 전자에 대한 퍼텐셜장을 계산하고, 그 계산을 바탕으로 다른 전자의 퍼텐셜장을 계산하며, 이를 계속 반복하여 이전의 계산 값과 새로운 계산 값이 일치할 경우 해로 취하는 방식이다[34]. HF는 ab initio 방법 중에서 가장 간단한 형태로, Hartree에 의해 제안되었으며, 그 후 Fock에 의해 Pauli의 배타 원리를 적용하여 수정되었다. HF는 전자와 전자가의 반발력을 다루지 않으며, 평균적인 영향만을 고려하는 방식이다[35]. 반면, DFT는 Fermi에 의해 제시되어 Kohn에 의해 발전된 이론으로, Born-Oppenheimer 근사를 통하여 핵을 고정하고 핵보다 몇천배 가벼운 전자를 핵에 의한 전자 운동이라는 가정을 이용해 계산에 필요한 부하를 획기적으로 줄이는 방법이다. 단순히 이야기 하면, 전자의 파동함수를 밀도함수로 대체함으로써 계산 부하를 줄이는 방식이다. 경험적 방법은 경험적 변수의 사용 정도에 따라 반경험적과 경험적 방법으로 나눠지는데, 이러한 방법은 대게 많은 원자로 이루어진 분자의 이론적인 계산 시간을 줄이기 위하여 사용한다[33,36]. 한편, 이외에도 매우 큰 분자를 가진 계의 경우, 양자역학 계산을 하지 않고 고전역학을 이용하는 분자역학도 존재한다.
2.3. 밀도범함수이론을 이용한 계산화학
Schrödinger 방정식을 수학적으로 풀기 위해서는 간단한 시스템이라 하더라도 수많은 연산을 수행하여야 하며, 연산을 줄이기 위한 다양한 근사 방법과 연산을 효율적으로 하기 위한 높은 수준의 연산 자원(computing resource)이 필요하다. DFT는 분자의 총에너지를 파동함수 대신에 전자밀도로 계산할 수 있다는 개념으로 다양한 근사법을 가지고 있다. 여러 근사 중에서도 가장 흔히 사용하는 방법은 1980년대 후반에 제안된 B3LYP (Becke, three-parameter, Lee-Yang-Parr) exchange correlation functional 방법으로[37,38], 기존의 HF에 비해 보다 진보된 방법이며, Post HF 기법보다 빠르게 비슷한 결과를 제시하는 것으로 밝혀졌다[36,38]. 이렇게 근사 방법을 적용하여 구한 해는 분자 구조, 진동 파수, 원자화와 이온화 에너지, 전기적 및 자기적 특성, 반응경로 등 다양한 분자의 성질을 예측하는데 사용할 수 있다[33,37,38]. 현재 계산화학을 구현할 수 있는 소프트웨어가 비상업용, 학술용, 또는 상업용으로 다양하게 개발되고 있다. 그중 ADF, GAMESS, Gaussian, NWchem, Spartan과 같은 소프트웨어가 대표적이다. 소프트웨어마다 라이센스, 적용되는 이론, 사용되는 근사법, 기저계 등이 상이하기 때문에, 연구 목적에 맞는 소프트웨어를 선택하는 것이 매우 중요하다.
3. ATR-FTIR을 이용한 실험적 측정
3.1. 액체와 고체 계면 분석의 중요성
액체-고체 계면에서 일어나는 화학반응은 토양 환경에서 오염물질이나 영양원소의 흡착과 거동을 이야기할 때 매우 중요하다[39,40]. 특히, 산화음이온은 토양 환경 내에서 흡착과 탈착, 화학종분화, 그리고 침전 등과 같은 다양한 화학반응을 거치며 토양계에서 수계로 이동한다[41,42]. 이러한 순환 과정에서 환경이 불가역적으로 변화할 경우, 전체의 순환 시스템에 영향을 줄 수 있으며, 이렇게 발생하는 순환 시스템의 문제는 궁극적으로 인류에게 영향을 미칠 수 있다. 그러므로, 액체-고체 계면에서 일어나는 화학반응을 이해하는 것은 매우 중요하며[25,39], 이를 밝히기 위해 다양한 분석 방법과 분석 기기들이 개발되고 있는 실정이다. 대표적으로, 원자간력현미경(AFM), 전자 에너지 손실 분광법(EELS), 전자 상자성 공명(EPR), 저속 전자선 회절(LEED), X선 흡수분광법(XAS) 및 X선 광전자 분광법(XPS)과 같은 다양하고 효과적인 분석 방법이 개발되었다[25,26,43]. 그러나 이러한 분석방법에는 몇가지 단점이 존재하는데, 전자를 사용하는 분석법의 경우에는 대게 높은 수준의 진공이 요구되기 때문에 액체-고체 계면 분석이 불가능하며, 건조나 응결과 같은 상변화 과정을 거쳐야만 분석이 가능하다는 단점이 있다. X선을 이용하는 분석 방법의 경우에는 세가지 문제가 존재하는데, 일반적으로 실험실에서 사용하는 X선의 세기(intensity)로는 계면분석을 수행할 경우 물에 흡수되어 감도가 매우 낮아진다는 단점이 있으며, 가속기(synchrotron)와 같이 높은 세기를 가진 X선을 이용할 경우에는 감도가 상대적으로 높게 나타나지만, 유기산과 같이 상대적으로 분해되기 쉬운 물질들이 분석과정에서 분해되어 버리는 단점이 있다[26,44]. 따라서 유기산을 분해하지 않으면서 계면 분석이 가능한 분석방법이 필요하게 되었다.
3.2. FTIR의 역사와 다양한 분석 기법들
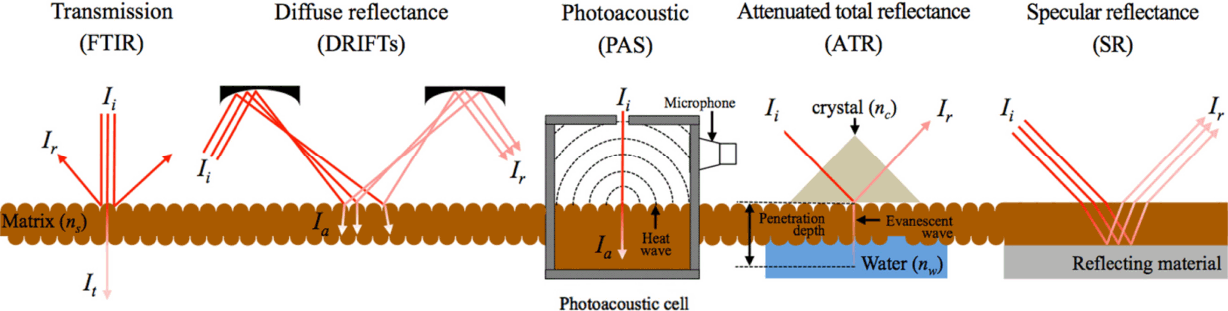
적외선을 이용한 분광학은 19세기 W. Herschel이 처음으로 제안하였는데, 초창기에 적외선 분광기(Infrared spectrophotometer, IR)는 프리즘이나 모노크로메이터를 사용하였다. 그러나 19세기 후반 Michelson에 의해 간섭계가 개발되면서, 현대 IR의 틀을 갖추게 되었다. 그러나 시역(timedomain)에서 측정한 인터페로그램(interferogram)을 진동수 도매인으로 변환하는 것이 문제였는데, 1949년 Peter Fellgett가 IR에 퓨리에 변환을 적용하면서 최초의 Fourier transform infrared spectroscopy (FTIR)를 개발하였고, 1960년대 본격적으로 상업적인 FTIR이 출시되어, 현재까지 반세기 동안 FTIR은 연구자들에게 매우 유용한 분석도구로 활용되고 있다. 따라서 FTIR을 이용한 다양한 분석 기법이 개발되고 발전되었는데, 가장 대표적인 것이 투과(transmission), 산란반사(diffuse reflectance), 광음향(photoacoustic), 감쇠전반사(attenuated total reflectance), 그리고 정반사(specular reflectance)방법이다(Fig. 1). 각각의 방법은 장단점을 가지는데, 투과법은 KBr을 이용한 고상 측정 방식과 액체를 투과하면서 측정하는 두 가지 방법이 있다. 고상 측정 방식은 계면분석이 불가능하고, 액체 투과 방식은 매우 작은 투과 두께가 필요하기 때문에 정량적인 분석이 거의 불가능하다는 단점을 가진다. 산란반사법은 시료에 적외선을 조사하고, 난반사되는 적외선을 집광하여 검출기에서 측정하기 때문에, 시료의 전처리가 필요없다는 장점을 가진다. 다만 물을 함유할 경우 물 분자에 의한 흡광 때문에 검출기로 도달하는 빛의 세기가 매우 약해진다는 단점 때문에 고체 시료를 측정하는데 적합하다. 광음향 분석법의 경우 적외선을 흡수하면서 발생하는 진동을 마이크로폰으로 측정하여 분석하는 방법으로 흡광도가 큰 물질을 측정하는데 장점이 있지만, 액체를 측정할 때는 공명기가 필요하다는 단점이 있다[45]. 정반사법은 적외선을 반사하는 물질 위에 시료를 놓아, 시료를 통과한 적외선이 전반사 후 다시 시료를 통과하여 나갈때 발생하는 적외선의 세기 차이를 바탕으로 분석하는 방법이다. 이는 금속 표면 위에 처리한 물질이나, 매끈한 표면으로 이루어진 피막 형태의 시료 측정에는 용의하지만, 반사매질의 굴절률과 표면의 평활도에 의존적인 방법이다[46]. 감쇠 전반사는 결정체 위에 시료를 적층하거나 압력으로 밀착한 뒤, 적외선을 결정체 내부로 투과시켜 전반사를 형성하면, 이때 발생하는 소멸파(evanescent wave)가 일정 침투 깊이(depth of penetration, 이하 dp)만큼 시료를 투과하면서 흡광이 일어나고 그 차이에 따라 분석하는 방법이다. 매우 작은 dp를 가지기 때문에 두께가 얇은 시료만 분석이 가능하지만, dp 범위 이내에 고체와 액체 계면을 형성한다면, 계면에서 일어나는 화학 반응에 대한 분석이 실시간으로 가능하다는 장점을 가진다.
3.3. ATR-FTIR의 원리 및 고려 사항
ATR-FTIR을 이용한 액체-고체 계면 측정의 기본 원리는 적외선을 결정체로 입사시켜 결정체와 시료 계면에서 전반사시킨 후, 이때 발생하는 수 μm 수준의 소멸파가 결정체 외부의 시료를 통과한 후 다시 결정체 내부로 들어가면서 나타나는 흡광 현상이다[39,47]. 따라서, ATR -FTIR 사용에서 가장 중요한 것은 전반사 형성이며, 이때 관여하는 변수는 Fig. 2와 같다. 본 실험 조건에서 적외선의 입사각(θi)과 결정체, 금속산화물, 그리고 물의 굴절률(각각 nc, ns, 그리고 nw)에 따라 적외선은 크게 세가지 형태로 전반사, 정반사 혹은 투과한다. 일반적으로 실험에서 온도, 압력, 그리고 θi은 일정하기 때문에, 결정체와 금속산화물의 굴절률의 비(ns/nc)가 임계각(θc)을 결정하게 된다. ns < nc 이고, θi > θc1이면 전반사가 일어나, 결정체와 금속산화물의 계면에서 소멸파가 발생한다. 이때 결정체와 금속산화물의 계면에서 소멸파가 발생하는 거리(dp,cs)는 식 (1)에 의해 계산한다[48,49].
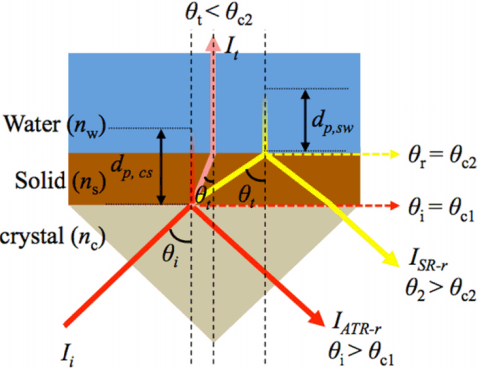
Schematic diagram showing optical pathway during internal reflection at solid-liquid interface measurement using in situ ATR-FTIR. nc, ns, and nw indicate refractive index of crystal, solid, and water, and θi and θt mean angle of incident from crystal to solid, and from solid to water. θc1 and θc2 show critical angle at crystal-solid and solid-water interface. Ii, IATR-r, IATR-r, ISR-r, and Ir indicate infrared intensity of initial, ATR refracted, SR refracted and transmitted. dp, cs and dp, sw mean depth of penetration at crystal-solid and solid-water interface, respectively.
식 (1)에 따르면 dp,cs는 파장(λ)이 길어질수록, θi가 감소할수록, 그리고 ns/nc가 커질수록 증가한다. 적외선 전반사에 의한 소멸파가 투과한 경로(path)에서 흡광이 일어나면, 전반사 후 세기(IATR-r)는 감소하여 검출기로 향하게 되고, 초기 적외선의 세기(Ii)와 IATR-r의 차이에 따라 흡광도를 계산한다.
ATR은 전반사의 횟수에 따라 단반사 ATR (single reflection ATR)과 다반사 ATR (multiple reflection ATR)로 구분한다. 단반사 ATR은 Fig. 2와 같이 작은 결정체를 이용하여 전반사를 1회만 발생시켜 정성 분석에 사용하거나 다이아몬드와 같은 결정체를 이용하여 극한 환경 조건에서 측정할 때 사용한다. 다반사 ATR은 막대 모양의 결정체를 이용하여 내부에서 연속적으로 전반사시켜 소멸파 발생횟수를 증가시키는데, 그 결과 단반사 ATR보다 긴 경로 길이를 가지기 때문에 정량 분석에 주로 사용한다. 다만, 상대적으로 큰 결정체를 필요로 하기 때문에 가격이 비싸지게 된다. 특히 토양과 같은 고체 시료를 측정할 경우 일반적으로 사용하는 ZnSe나 AMTIR의 경우 경도가 석영보다 낮기 때문에 압력을 가해 밀착하는 과정에서 결정체에 피해를 줘 난반사가 일어나는 문제가 흔히 발생한다.
Table 1은 결정체와 금속산화물에 따라 dp를 나타낸 것으로, 굴절률은 λ = 10 μm 조건에서 2.2-4.0이며[26], 본 총설에서 주로 다루는 금속산화물은 1.65-3.1 범위 안에 존재한다[5~7]. 결정체와 금속산화물의 굴절률이 비슷한 상태, 즉 nc≈ns, θi < θcs조건에서는 전반사가 일어나지 못하고 굴절되어 투과하는 현상이 발생한다. 이렇게 금속산화물 내부를 투과한 적외선은 다시 금속산화물과 물의 계면에 도달하게 되고, 이때 nw < ns, θr > θsw이면 전반사가 일어나고, 금속산화물과 물의 계면에서 소멸파가 발생한다. 이러한 현상은 Fig. 1에서 설명한 정반사법과 매우 유사하며, 물이 반사물질 역할을 하여 적외선은 결정체 위에 처리한 금속산화물을 투과하고, 금속산화물과 액체 계면에서 전반사되어 다시 금속산화물과 결정체를 거쳐 검출기로 향하게 된다. 뿐만 아니라, 금속산화물과 물 계면에서 발생하는 소멸파의 투과깊이(dp,sw)는 θi와 n에 따라 결정되며, 상대적으로 흡수성(absorbability)이 높은 물을 통과하기 때문에 적외선 흡광도가 증가한다. 이러한 이유로 정반사 후 세기(ISR-r)는 IATR-r과 비교하였을 때, 매우 감소하게 된다. 특히 λ가 증가하면서 dp는 급격히 감소하는데, 물에 의한 흡수성에 따라 검출기에서 검출되는 적외선의 세기가 매우 낮아 여러 문제를 발생시키기도 한다[47,50,51].
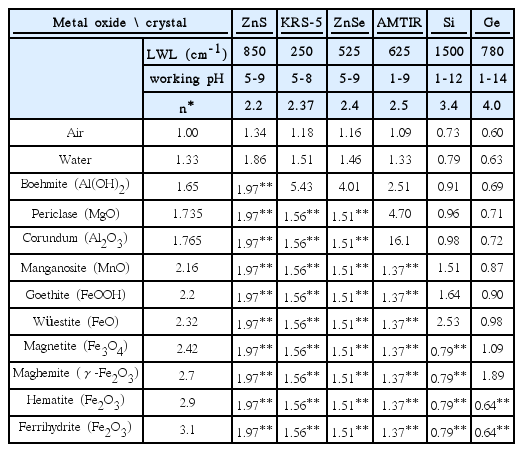
Penetration depth between crystal material and metal oxide (T=25℃, pressure=1 atm, nw=1.33, λ=10 μm, θi =45o)
Fig. 2에서 보면, IATR-r과 ISR-r의 위치 차이가 나타나는데, 이렇게 전반사의 횟수와 시료의 두께가 증가하면, 경로 길이의 차이는 크게 나타나고, 이때 전반사된 적외선이 검출기로 제대로 도달하지 못하는 현상이 발생할 수도 있다[48]. 그러나 일반적인 실험조건에서는 FTIR의 광학 장치를 조정하여 전반사나 정반사 모두 입사된 빛이 검출기로 돌아가도록 교정할 수 있기 때문에, 상대적으로 간단한 실험 매개변수 변경을 통하여 최적의 실험 조건을 도출해낼 수 있다. Fig. 2에서처럼, n3≈n2, θt < θc2인 조건에서 금속산화물과 물의 계면에 대한 θt가 작아지기 때문에, 적외선이 전반사 없이 투과하게 되어 소멸파가 발생하지 않는 경우도 발생한다. Table 1에 제시한 θi = 45o 조건에서는 결정체와 금속산화물 간에 투과가 발생하지 않지만, θi가 작아질수록 투과되는 경우가 발생하여, ATR 실험을 적용할 수 없는 경우가 발생할 수 있다.
실험 조건과 FTIR 기기 내부의 광학장치의 특성까지 ATR-FTIR측정에 영향을 미치는데, 가장 대표적인 예로 파수(wavenumber)와 금속산화물의 굴절률에 따른 dp를 들 수 있는데, 이를 이론적으로 계산하여 Fig. 3에 나타내었다. Fig. 3(a)는 장파장 차단(long wavelength cutoff) 지점 이상인 중적외선 영역(4,000 - 500 cm-1)에서 dp가 파수와 θi가 감소할수록 기하급수적으로 증가하는 것을 나타내는데, 이 때문에 ATR-FTIR에서 파수가 감소하면서 흡광도가 급격하게 증가하는 현상이 나타난다. 특히, θi가 낮을수록 dp는 급격하게 증가하고, 과도한 흡광에 따라 검출기에 도달하는 빛의 세기가 매우 낮아지는 현상이 주로 발생한다. 반면, θi가 높을수록 dp는 감소하기 때문에, 제작한 피막의 두께가 dp 이상이라면 계면에서 흡광이 일어나지 않아 계면 반응 정보를 얻을 수 없는 현상이 발생한다[25,43,52].
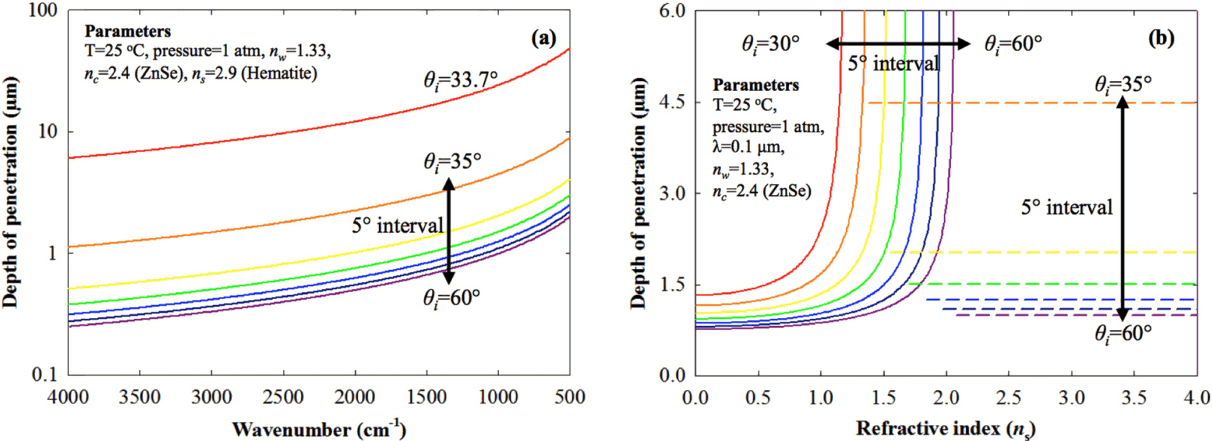
Theoretically calculated depth of penetration (dp) as function of wavenumber (a) and refractive index (b). The color difference means 5o interval at angle of incident (θi).
Fig. 3(b)는 파수 1,000 cm-1에서 ZnSe 결정체를 사용할 때, 시료의 굴절률에 따라 나타나는 dp 차이를 도식화한 것이다. 이 때 중요한 것이 실선으로 도식화한 ns 1-2 범위에서 나타나는 급격한 dp,cs 증가이다. 이는 소멸파 결합(evanescent wave coupling)이라 부르며, n이 높은 두 매질 사이에 두께가 얇은 n이 낮은 매질이 존재할 때, 소멸파가 다른 매질로 전달되는 현상이다. 이러한 소멸파 결합 때문에 소멸파는 다시 결정체 내부로 돌아가지 못하고 다른 매질로 이동하여 계면에서 흡광도 정보를 얻을 수 없게 된다[53]. θi가 낮은 경우에는 낮은 ns에서만 소멸파가 형성되기 때문에, ns > 1인 경우 일부가 소멸파 결합으로 다른 매질로 전달되거나 투과되어 소멸파를 형성하지 못한다. θi > 35o 조건에서는 ns가 증가하면서 소멸파 결합이 나타나서, dp,cs를 형성하지 못하고 dp,sw를 형성한다. 이때, 고체 매질을 통과하면서 입사각이 변하여 소멸파가 발생하기 때문에, ns의 증가와 관계없이 일정한 dp를 가지는 소멸파를 형성한다.
이와 같이 사용하는 매질의 n, 및 θi, λ에 따라 dp가 달라지고, 또 특정 조건에서는 소멸파가 발생하지 않기 때문에, 실험 대상 시료와 사용하는 결정체의 특성에 따라 적절한 실험 조건을 설정하는 것이 매우 중요하다[48]. 특히 물질은 λ에 따라 다양한 굴절률을 가지기 때문에, 이러한 특성까지 고려하여 실험 조건을 설정해야 하는데, ATR의 형성 원리와 dp에 대한 이해가 실험 설계보다 우선적으로 선행되어야 한다[26,43,54].
3.4. ATR-FTIR을 이용한 실험적 측정 방법
ATR 형성 원리를 이해하고 실험조건을 설정하였다면, 추가적으로 고려해야 하는 것은 금속산화물의 물리적인 특성이다. 대표적인 금속산화물인 철 산화물을 예로 든다면, 합성방법은 크게 6가지가 있다. Fe(III) 염화물 산성용액의 가수분해법, Fe(II) 염화물의 산화적 가수분해법, 상 변형법, Sol-Gel법, 열수 침전법, 그리고 금속 킬레이트 분해법이 있다[55]. 일반적으로 ATR-FTIR을 이용한 실험에서는 용액상에서 핵형성(nucleation)과 결정 성장(crystal growth)을 통하여 침전되는 철산화물을 주로 사용하는데, 주로 단분산 입자(monodispersed particle)를 형성하는 방법을 택한다. 그 이유는 입자의 크기와 형태에 따라 비표면적이 달라지고, 각각의 결정면 마다 흡착에 차이가 나타나기 때문에, 단분산 입자를 합성하는 것은 ATR-FTIR 실험에서 매우 중요하다[26,43,56].
일반적으로 철산화물은 주로 구형과 막대 모양이며, 마이크론에서 서브마이크론 정도의 입자크기를 가진다. 그러나 ATR-FTIR 실험에서 침투 깊이는 수 μm 이하로 나타나기 때문에, 입자 크기가 침투 깊이 보다 크면 소멸파가 계면을 통과하지 못하고 금속산화물 내부만 통과하여 표면 결합 구조에 대한 정보를 얻을 수 없다. 또한 계면 측정에서 흡착물인 금속산화물이 결정체 표면에 잘 접촉하는 것은 매우 중요한데, 입자 크기가 커질수록 물리적인 특성 때문에 응집(coagulation)이 일어나지 않아 피막 형성이 어렵게 된다[55,57]. 더욱이, 입자 크기가 클수록 입자 사이의 공극의 수는 감소하지만 공극의 크기는 증가하고, 이 공극에 공기나 물이 침투하여, 피막의 안정성을 저해하여, 결과적으로 ATR 결정체 표면에서 분리될 위험성이 있다. 다만 피막의 안전성에 영향을 주지 않는 범위 내에서 형성되는 공극은 nc≈ns 조건에서 결정체와 금속산화물 계면에서 소멸파를 발생시키는 역할을 하여 dp,cs가 발생한다. 그러나 만일 공극이 소멸파 결합이 일어나는 작은 크기로 존재한다면, dp,sw가 발생하거나 투과한다[26,48]. 그러므로, ATR-FTIR 실험을 위한 피막 제조방법은 단분산 입자를 합성하여 용매에 분산시키고, 이를 적정 농도로 희석하거나 농축하여 ATR 결정체 위에 도포하는 것이다[29,31]. 결정체 표면에 고르게 도포한 후 건조시키면 피막이 생기는데, 입자가 응집하는 특성에 따라 피막의 안전성이 달라진다. 따라서 pH 변화나 응집제 투입과 같이 환경 조건을 조절하여 형성 피막의 안전성을 증대시키는 것이 매우 중요하다.
피막이 제대로 형성되었다면, ATR 결정체 판(plate)을 반응 용기에 잘 고정시키고, 실험에 사용할 배경 용액을 투입하여 피막의 안전성과 배경 스펙트럼을 측정하는 것으로 계면 측정 실험 준비는 끝난다. 실험은 다양하게 할 수 있는데, 일반적으로 대상 물질을 용해한 뒤, 반응용기에 투입하여 피막과 반응시키고, 이 과정을 반응속도론 관점에서 시간 순서대로 측정한다[58~60]. 측정 환경을 변화시키거나, 흡착에 경쟁하는 물질 또는 물질을 분해하거나 변환시키는 물질을 투입하여 이들의 상호작용을 측정할 수 있을 뿐만 아니라[31,61~64], 장시간 반응시켜 평형 상태를 측정할 수도 있다[29,65,66]. 특히 최근에는 금속산화물 표면과 미생물과의 상호작용을 연구하는 시도까지도 이루어지고 있다[67].
4. 스펙트럼 해석
ZnSe를 사용한 실험에서 측정한 스펙트럼은 일반적으로 4,000 - 650 cm-1에서 다양한 진동에 관한 정보를 갖고 있다. 특히 1,200 - 600 cm-1 영역에서는 물질의 변각 진동(bending vibration)에 의한 특이적 흡광이 주로 나타나기 때문에, 이를 지문영역(fingerprint region)으로 부른다. 산소와 결합한 무기 분자의 경우 지문 영역에서 흡광을 나타내는 경우가 많다. 다만, λ가 증가하면서 물에 대한 dp가 증가하기 때문에, 800 cm-1이하의 정보는 얻기 힘들 뿐만 아니라, 설정한 실험계가 복잡할수록 흡광 밴드가 겹쳐지기 때문에 해석이 매우 어려워진다는 단점이 있다. 이러한 단점을 보완하기 위해, 실험적으로 중수소로 이루어진 물분자를 이용하여 지문영역에서 흡광 파수를 변화시키는 방법이나, 실험 조건을 변화시켜 물에 대한 dp를 조절하여 800 cm-1 이하의 스펙트럼을 구할 수 있다. 또, 실험에 의해 얻은 스펙트럼 밴드를 도함수 분광학(derivative spectroscopy), 이차원 상관 분광학(two-dimensional correlation spectroscopy) 및 multivariate curve resolution (MCR)을 이용하여 수학적으로 처리하는 방법과 계산화학을 이용하여 이론적으로 구하는 방법이 있다.
4.1. 스펙트럼 보정
스펙트럼을 해석하기 전에 측정한 스펙트럼에 대한 보정이 필요한데, FTIR 보정 방법은 두 가지로 구분할 수 있다. 첫째로는 FTIR 기기의 환경 요인 때문에 발생하는 잡음을 제거하는 방법으로 평활화(smoothing)를 수행하는 것인데[68], 이때 ATR-FTIR 측정에서 검출기로 도달하는 적외선의 세기가 매우 낮기 때문에 기기의 잡음 영향이 뚜렷하게 나타난다. 다른 방법으로는 ATR 보정이다. 파수가 감소할수록 dp는 급격히 증가하고, 이는 광로 길이를 늘어나게 한다(Fig. 3(a)) [26,54]. 그 결과로, 일정한 흡광이 일어난다 하더라도 검출기로 도달하는 적외선의 세기는 감소하게 된다. 이러한 이유로 동일한 시료를 투과와 ATR 방식으로 찍을 경우, ATR 방식에서 낮은 파수에서 더 높은 흡광도를 나타나게 된다. 이뿐만 아니라 흡광 밴드의 위치도 파수가 낮은쪽으로 이동하는 현상이 나타나는데, 이를 보정하는 방법이 Kramer-Kronig변환을 이용한 ATR보정(ATR correction)이다[69]. 이러한 현상은 매질의 n이 크게 차이가 나고, θi가 작을 때 심각하게 발생하며, 흔히 사용하는 ZnS (nc=2.4)와 θi = 45o 조건에서는 크게 나타나지 않는다.
4.2. 밴드 확인
보정을 마친 스펙트럼에서 진동 방식에 따른 흡수대(밴드위치)를 찾아야 하는데, 간단한 계일수록 겹쳐지는 밴드가 적기 때문에 쉽게 구분할 수 있지만, 복잡한 계의 경우 밴드중첩 현상도 증가하기 때문에 밴드를 구분하기 어려워진다. 이를 해결하기 위하여 사용하는 방법이 크게 네 가지인데, 도함수 분광학, 이차원 상관 분광학, 그리고 MCR을 이용하여 스펙트럼을 수학적으로 처리하여 밴드 위치를 확인하는 방법과 계산화학을 이용하여 이론적으로 밴드 위치를 계산하는 방법이 있다.
4.2.1. 도함수 분광학
도함수 분광학은 어떤 함수를 미분하여 밴드를 찾아내는 가장 기본적인 방법이다. 파장을 미분한 1차 도함수를 식 (2)와 같이 나타낼 수 있다[70,71].
이렇게 구한 1차 도함수를 계속 미분할 수 있는데, 미분 횟수(n)에 따라 n차 도함수라 하며 밴드 위치를 확인하는 것은 미분 횟수에 따라 달라진다. Fig. 4(a)는 용액상의 인산염을 pH 4.5와 7.0에서 ATR-FTIR을 이용하여 적외선 스펙트럼을 측정한 것으로, 이를 2차 도함수로 나타내었다. 그 결과, 두 pH 범위에서 총 5개의 밴드가 검출되었다. 이 방법은 단일 스펙트럼을 이용하여 밴드 위치를 쉽게 찾아낼 수 있다는 장점을 갖는 분광학에서 가장 기본적으로 사용하고 있는 밴드 검출 방법이지만, 매우 복잡한 계이거나 스펙트럼에 중첩이 심한 경우에는 밴드 검출이 어렵다는 단점이 있다. 특히, 시간이나 환경 변화에 따른 스펙트럼 변화를 개별적으로 모두 고려해야 하기 때문에, 처리 과정이 복잡하며, 계의 복잡도가 증가할수록 소요 시간이 기하급수적으로 증가한다는 단점도 있다.
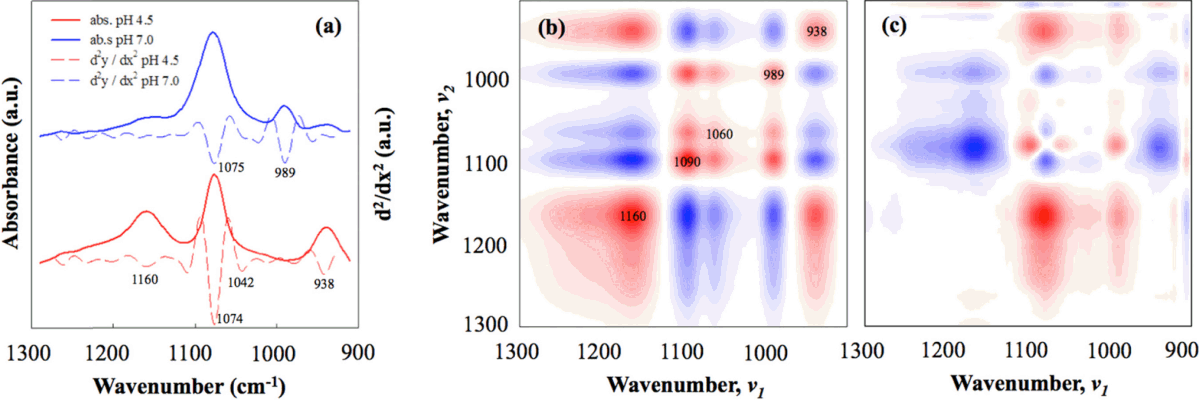
Example of peak identification in aqueous phosphate speciation measured by in situ ATR-FTIR using derivative spectroscopy under pH 5.5 and 8.0 (a) and synchronous (b) and asynchronous correlation spectrum (c) from pH 4.5 to pH 7.0 using two dimensions correlation spectroscopy. Solid and dotted line indicate absorbance and d2 /dx2 , respectively. Number indicates identified peak positions.
4.2.2. 이차원 상관 분광학
이차원 상관 분광학은 전자기파의 진동수, 파수, 파장과 같은 독립적인 분광 변수를 이용하여 분광 세기를 얻는 방법으로, 1980년대 NMR 연구에 처음 도입되었다. 이 방법은 계의 변화에 따라 나타나는 분광학적 신호의 유사성과 비유사성을 알 수 있게 해준다[72~75]. 이러한 신호 변동은 시료에 외부적인 섭동(pertubation)이나 물리적인 자극이 주어지면서 나타나는데, 이렇게 나타나는 신호 세기 변화를 상호상관 기법을 이용하여 체계적으로 분석해주는 것이 이차원 상관 분광학이다. 여기서 얻게 되는 상관 세기는 두개의 독립적인 스펙트럼 축에 의해 이차원적인 지도로 나타나는데, 이를 이차원 상관 스펙트럼이라고 부른다. 그 결과 크게 두가지 형태의 상관 스펙트럼을 얻게 되는데, 하나는 동기식(synchronous). 다른 하나는 비동기식(asynchronous) 스펙트럼이라 하고, 각각 식 (3)과 (4)와 같이 정의할 수 있다.
여기서 Φ와 ψ는 각각 동기식, 비동기식 스펙트럼,
Fig. 4(b)와 4(c)는 용액상의 인산염의 pH를 4.5에서 7.0으로 변화시켜 얻은 스펙트럼(Fig. 4(a))을 ATR-FTIR을 이용하여 측정한 결과이다. Fig. 4(b)는 동기식 스펙트럼을 나타냈으며, 이때 v1=v2인 지점(점선)에서 얻은 상관 값은 밴드의 유무를 나타낸다. 본 예시에서는 1,160, 1,090, 1,060, 989 및 938 cm-1에서 총 5개의 밴드를 확인하였다. 실험조건의 섭동에 의해 나타나는 밴드를 autopeak, 하나의 밴드가 증가할 때 감소하는 다른 밴드를 crosspeak이라고 부르며, 이들의 관계는 상관 정사각형(correlation square)을 그려보면 쉽게 알 수 있다. Φ(v1,v2)의 상관 값이 양수(그래프에서 적색 부분)일 때는 autopeak, 음수(청색 부분)일 때는 crosspeak이다. 예를 들면 1,160과 1,090 cm-1에서는 청색이므로 crosspeak, 1,160과 938 cm-1에서는 적색이므로 autopeak이다.
비동기식 스펙트럼은 autopeak을 나타내지 않고, crosspeak만을 나타내는데, 가장 큰 차이점은 대각선을 기점으로 동기식은 대칭이지만 비동기식은 비대칭으로 나타난다는 것이다. 비동기식 crosspeak은 v1과 v2에서 측정된 두 신호의 세기가 단계에 따라 변화할 때만 발생하기 때문에, 다른 지점에서 나타나 겹쳐지는 밴드를 구분하는데 매우 유용하다. 특히, 비동기식 crosspeak의 부호는 양수이거나 음수일 수 있는데, 이 부호는 신호 변화에서 순차를 결정하는데 사용한다. 섭동에 따라 Ψ(v1,v2)이 양수일 때에는 v1 밴드의 변화가 먼저 일어나고, 그 다음에 v2 밴드의 변화가 일어나지만, 반대로 음수일 때에는 v2 다음에 v1의 순서로 변화가 일어난다[72,74]. 예를 들면, Fig. 4(c)에서 Ψ(1160, 1090)이 청색, 즉 음수이기 때문에, 1,090 cm-1 밴드의 변화가 일어난 다음 1,160 cm-1 밴드의 변화가 그 다음에 일어난다. 이러한 방법을 통하여, 섭동에 의하여 연속적으로 나타나는 밴드를 검출할 수 있을 뿐만 아니라, 밴드 간 순서도 확인할 수 있다.
4.2.3. Multivariate curve resolution
MCR은 복잡한 구성요소들로 이루어진 신호의 집합에서 모델이나 시스템에 대한 사전적 정보 없이 하나의 신호만을 추출하는 것으로, 1971년 Lawton과 Sylvestre가 처음으로 제안하였다[76,77]. MCR법은 현존 모델이 없거나 모델에 대한 정보가 부족한 상황에서도 실험으로 얻어진 다양한 신호의 집합적 정보를 개별 신호에 관한 정보로 추출하는데 중점을 두고 있다. 그렇기 때문에, 실제 측정 결과 행렬만을 가지고도 MCR 분석을 수행할 수 있지만, 사전적 정보가 추가될 경우에는 최종 결과에 대한 정보를 보다 더 정확하게 얻을 수 있다는 장점이 있다[78].
MCR 분석의 이론적인 배경은 2차원 데이터 매트릭스, D(m × n)를 두개의 매트릭스, C(m × k)와 ST(k × n),로 분리하여, 알려지지 않은 혼합 신호에서 k에 대한 순수 스펙트럼과 농도 프로파일을 얻을 수 있다는 것이다[79]. MCR은 식 (5)와 같으며,
여기서 E(m × n)는 데이터의 잔존 변이(residual variation)를 포함하는 오차행렬이다. 현재 가장 잘 알려지고, 적용성이 높은 MCR방법은 1995년 Tauler가 제안한 alternating least squares(교대최소제곱)을 이용한 알고리즘(MCR-ALS)이다[79,80]. MCR 분석에서 가장 중요한 것 중 하나는 제한점(constraint)을 설정하는 것인데[79,80], 이는 데이터에 대한 기본적인 화학 및 물리학에 대한 이해에 근거하여 이루어져야 한다. 대표적인 제한점은 크게 네 가지로, Non-negativity, Unimodality, Closure, 그리고 Hard-modeling이 있다[77]. Non-negativity를 예로 들면, 시간에 따른 파장별 흡광도에 관한 행렬이 있고, 측정하는 물질이 자체 발광하지 않고, 외부로부터 빛이 추가적으로 들어오지 않는 조건일 경우, 흡광도는 음수가 될 수 없다는 것이다. 그러나 측정 과정에서 발생하는 오차로 인한 음수 값을 0으로 간주하여, MCR 분석을 실시하는 방법이다.
Fig. 5(a)는 pH 변화에 따른 용액 내 인산염의 종변화를 ATR-FTIR을 이용하여 측정한 결과로, Fig. 5에서 (b)와 (c)는 각각 MCR최적화 스펙트럼(MCR optimized spectra)과 MCR 최적화 농도(MCR optimized concentrations)를 나타낸다. MCR-ALS분석 프로토콜은 연속적으로 측정한 스펙트럼의 형렬을 배경선 보정과, 평활화, 그리고 정규화를 통하여 전처리를 하고, 이런 과정을 통하여 형성된 데이터집합을 이용하여 분석하는 것이다[81]. MCR-ALS분석에서 가장 우선적으로 수행하는 것은 초기추정치(initial estimates)를 설정하는 것인데, 특히 pH에 따른 스펙트럼 변화 안에 몇 개의 구성 요소(component)가 있는지 설정하는 것이 매우 중요하다. 이를 위하여 특이값분해(singular value decomposition, SVD)에 의해 초기추정치를 구하고, MCR-ALS 분석을 수행하여, 분석 결과로 MCR-ALS 최적화된 스펙트럼과 MCR-ALS 최적화된 농도를 얻을 수 있다.

Countour map of aqueous phosphate speciation measured by pH change using in situ ATR-FTIR (a), two identified spectrum and its experimental peak position calculated using DFT (b), pH versus concentration graph fitted by MCR-ALS (c). Red and blue bar in (b) indicate theoretically calculated peak position using DFT (B3LYP, 6-31G).
Fig. 5(b)는 SVD 수행 후, MCR-ALS를 이용하여 최종적으로 예측한 두 개의 구성 요소이다. 이 결과는 Fig. 4(a)와 매우 유사한데, 그 이유는 스펙트럼에 나타나는 밴드가 각각의 종에서 특징적으로 나타나는 autopeak이기 때문이다. Fig. 5(c)는 MCR-ALS 분석 후, pH 변화에 따른 두 구성요소의 농도 변화를 나타낸 것으로, pH 증가에 따라 종분화가 일어나는 현상과 각 구성요소의 농도를 의미한다. 이러한 분석으로, 복잡한 데이터집합에서 밴드를 구분하여 의미 있는 구성요소를 추출할 수 있다.
4.2.4. 계산화학
Fig. 5(b)에서 스펙트럼 아래의 적색과 청색 막대는 각각 DFT (B3LYP-D)를 이용하여 액체에서 얻은 H2PO4-와 HPO42-의 적외선 흡광밴드를 나타내는데[36], DFT 결과는 HPO42-의 va(PO-)에서 두 가지 밴드, 즉 1,090와 1,080 cm-1의 밴드가 겹쳐진 것으로 나타났다. 앞에서 언급하였던 세 가지 방법(도함수 분광학, 이차원 상관 분광학 및MCR-ALS)을 통해 검출한 밴드 대부분은 crosspeak로, 다른 비율로 변화하는 autopeak을 검출하기에 충분했지만, HPO42-의 1080 cm-1 va(PO-)에서 두 개의 밴드가 autopeak로 겹쳐서 나타나는 경우에는 이를 구분할 수 없다. 이러한 경우, 계산화학을 이용하여 이론적으로 적외선 스펙트럼을 계산하면, 매우 근접하여 발생하는 autopeak를 확인할 수 있었다[82,83]. Fig. 6(a)와 (b)는 pH 5.5와 8.0에서 측정한 스펙트럼을 각각 peak fitting하여 deconvolution하고, DFT를 이용하여 예측한 진동 방식을 나타낸 것이다. 한국과학기술정보연구원(KISTI)에서 제공하는 슈퍼컴퓨터(Tachyon)를 사용하여 계산화학 분석을 하였으며, 이 때 계산에 사용한 소프트웨어는 Gaussian 09 (Gaussian, USA)이며, 입력 파일은 Avogadro (USA)을 사용하여 작성하였다[84]. 분석 시, B3LYP, 6-31G(d,p) 조건을 사용하였고, 다음으로 구조최적화(geometry optimization)와 진동수(frequency)분석을 수행하였다[36]. 다섯 개의 물분자를 추가하여 계산하였지만[36], 이는 시인성을 위하여 나타내지 않았다. 녹색으로 표시한 화살표의 방향은 벡터를 의미하고, 화살표의 상대적인 길이는 그 진동의 크기를 의미한다. Fig. 6는 밴드가 특정 진동 방식에 배정되는 것을 나타낸 그림으로, 배정된 밴드가 pH에 따라서 변화하는 것을 나타낸다. 계산화학에 의한 결합 구조 계산은 지금까지 실험으로 측정한 결합 구조를 재검증할 수 있을 뿐만 아니라, 앞서 언급하였던 세 가지 방법으로 확인이 불가능하였던 중첩 autopeak의 유무도 확인할 수 있기에 매우 유용하다고 생각한다. 다만, 수퍼컴퓨터 계산을 최소화 하기 위하여 실험계를 최대한 단순화시킬 경우, 실제 실험값과 계산값이 일치하지 않는 경우가 발생할 수 있다[30,82,85,86].
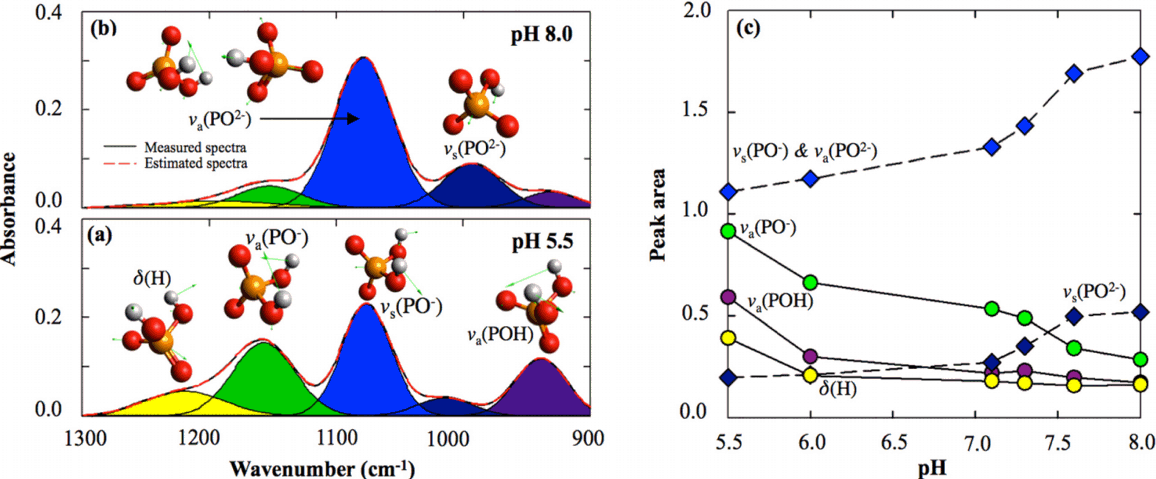
Peak deconvolution spectrum at pH 5.5 (a) and 8.0 (b), and the assigned vibrational mode for each deconvoluted peak, and deconvoluted peak area change as funtion of pH (c). Black solid and red dotted lines indicate measured spectra and estimated spectra for (a) and (b), and black solid and black dotted lines in (c) indicate spectrum of H2PO4- and HPO42-, respectively.
4.3. 결과 해석
이러한 접근 방법을 통하여 궁극적으로 얻고자 하는 것은 대상 물질의 환경 변화에 따른 구조 변화이다. Fig. 4(a)에서 나타나는 각 밴드별 흡광도와 Fig. 5(c)에서 나타나는 주성분의 pH에 따른 흡광도 변화, 마지막으로 Fig. 6(c)에서 나타나는 pH에 따른 각 밴드별 면적 변화는 모두 환경변화인 pH에 따라 대상물질인 인산염이 어떻게 종분화되는지에 대한 정보를 나타낸다. 앞에서 제시한 방법을 이용하여 복잡하게 겹쳐져 나타나는 스펙트럼을 각각의 밴드로 deconvolution하고, 밴드 각각의 면적을 구하여, 특정 진동 방식이 나타나는 정도를 구분한다. 결과적으로 특정 진동 방식의 세기를 알 수 있기 때문에, 특정 진동 방식이 환경 변화에 따라 어떠한 세기로 변화하는지 알 수 있다. 진동 방식의 변화는 결합 구조의 변화를 의미하기 때문에, 우리는 환경 변화에 따른 결합 구조 변화를 알 수 있다. 본 총설에 넣은 예시에서는 가장 간단한 용액 상에서 pH에 따라 변하는 인산염의 종분화만을 다루었지만, 여기에 금속산화물을 추가한다면, 우리는 pH 변화에 따라 금속산화물에 흡착한 인산염의 결합 구조와 존재비를 알 수 있다. 이는 곧 토양환경과 같은 복잡계에서 일어나는 유기산과의 경쟁이 인산염의 결합 구조와 존재비에 미치는 영향에 대한 실험을 수행할 수 있으며, 계면에서 일어나는 다면 반응의 기작을 이해하고 규명하는 데 기여하리라 생각한다.
5. 요 약
식물 유래 유기산과 산화음이온의 토양 내 거동 연구는 토양에서 영양염류의 이동성을 예측하고, 현재 수질 환경에서 발생하는 부영양화를 막기 위한 근본적인 해결책이다. 이러한 현상을 이해하기 위해서는 계면에서 일어나는 반응을 실시간으로 측정하는 것이 필요한데, ATR-FTIR은 계면 반응을 측정하기 위한 분석 방법 중 가장 유용한 도구 중 하나이다. 다만, ATR-FTIR을 이용한 연구를 수행함에 있어서 장점과 단점, 그리고 연구 설계 시 고려해야 할 사항들에 대한 기본적인 이해가 필수적이며, 특히 실험 조건에 따라 다른 형태의 전반사가 형성될 수도 있기 때문에, 주의가 요구된다. 적외선을 이용한 계면 분석은 많은 정보를 주지만, 그 정보들이 겹쳐짐으로 인하여, 해석이 매우 난해하여, 여러 신호 처리 방법들이 적용되고 있으며, 기본적인 도함수 분광학부터, 이차원 상관 분광학, MCR-ALS, 그리고 계산 화학까지 다양한 알고리즘을 이용하여 이러한 난해함을 해소하는 과정 중에 있다. 또한, ATR-FTIR은 현재 인위적이고, 간단하게 설계된 반응 시스템에서의 측정만 가능하기 때문에, 실제 자연 현상에서 일어나는 복잡한 반응에 대한 즉각적인 해답이 되지는 못한다. 그러나, 이러한 접근 방법을 이용하여, 상대적으로 간단한 계에서 나타나는 원리를 파악하고, 그 정보를 바탕으로 조금 더 복잡한 계를 해석한다면, 미래에 복잡한 자연 환경을 해석할 수 있는 중요한 접근 방법이 될 것이라 판단한다.
Acknowledgements
본 연구는 정부(교육부)의 재원으로 한국연구재단의 지원을 받은 기초연구사업(과제번호: NRF-2014R1A1A2059196), 글로벌박사양성사업(과제번호 : NRF-2015H1A2A1034068) 및 BK21 Plus 사업으로 수행하였습니다.