아크릴계 이온교환섬유를 이용한 수중 크롬(VI) 제거
Chromium(VI) Removal from Aqueous Solution using Acrylic Ion Exchange Fiber
Article information
Abstract
PAN 기반 아크릴계 섬유와 DETA 및 AlCl3・6H2O를 반응시켜 아민기(-NH2)를 가진 이온교환섬유 PADD를 합성하였 다. 개발된 섬유상 소재는 FT-IR과 SEM을 이용하여 그 특성을 확인해 보았다. 회분식 실험으로 수행된 PADD를 이용한 크롬 제거 실험 결과는 Langmuir 등온흡착모델에 잘 적용되었으며, 이때 계산된 이론적 최대흡착능 (Qmax)은 6.93 mmol/g으로 나 타났다. 한편 동적흡착실험은 Lagergren 유사이차속도모델에 잘 부합되었다. PADD의 크롬 흡착능은 pH 2에서 가장 높은 값 인 4.11 mmol/g을 나타내었고 pH 변화에 많은 영향을 받는 것으로 확인되었다. 또한, 인산과 비소(V)에 대한 공존이온 실험 을 통해 PADD가 크롬에 대한 높은 선택성을 갖고 있음을 확인할 수 있었다. 산-염기 역적정으로 구한 PADD의 총이온교환 능 (4.70 mmol/g)을 통해 소재의 선택적 제거 가능성을 검증하였다.
Trans Abstract
Ion exchange fiber, PADD was synthesized by the reaction between PAN based acrylic fiber and DETA with AlCl3・6H2O, and was analyzed by FT-IR and SEM to investigate its characteristics. The experimental results of Cr(VI) removal by PADD were better fitted with Langmuir adsorption isotherm, and the maximum uptake value (Qmax) was calculated to be 6.93 mmol/g. The kinetic data can be well described by Lagergen pseudo-second order rate model. The Cr(VI) adsorption capacity of PADD was 4.11 mmol/g at pH 2, which shows the effect of pH changes on the removal of Cr(VI). The adsorption selectivity of Cr(VI) was higher than phosphate and As(V). Total ion exchange capacity of PADD was 4.70 mmol/g, which was measured by acid-base back titration.
1. Introduction
크롬은 높은 내식성과 경도를 가지며, 도금, 스테인레스강 제조, 안료, 가죽 무두질 등의 산업에서 다양하게 사용된다[1,2]. 한편, 다양한 산화상태를 가지는 크롬은 수중에서 주로 3+, 6+의 산화수로 존재한다. 3가 크롬은 수용액 상에서 양이온으로 존재하며, 중성 pH에서는 낮은 수용성을 가지는 Cr(OH)3 형태로 나타낸다. 6가 크롬은 수용액 상에서 pH와 농도에 따라 HCrO4-, CrO42-, Cr2O72-의 형태를 가지며, 수용성과 이동성이 높아 3가 크롬에 비해 10~100배 이상 독성이 높다[1,2]. 6가 크롬은 체내 유입시 강한 산화력으로 간 및 신장손상, 체내 출혈, 호흡기 장애, 피부염 등을 발생시킬 수 있으며, 만성독성으로 발암성을 가진다[3]. 따라서 적절한 처리 없이 6가 크롬이 자연수계에 유입되면 환경을 오염시키고 동식물이나 미생물 등 생물체에 유해한 영향을 미칠 수 있다. 이러한 크롬의 독성을 고려하여 USEPA에서는 총 크롬에 대한 음용수 수질기준을 0.1 mg/L 이하, 한국에서는 0.05 mg/L로 규정하고 있다.
이러한 수중의 크롬을 제거하기 위해 개발된 기술에는 전기화학적 침전, 응집, 이온교환, 막분리, 용매추출, 흡착 등이 있다[3~5]. 화학적 침전 처리 방법은 장치가 단순하고 운전이 쉽다는 등의 장점을 갖고 있어 그동안 많이 사용되어 왔다. 그러나 이 방법은 6가 크롬을 3가로 환원시켜 제거해야 하는 추가적인 처리공정이 필요하며, 침전으로 인한 다량의 슬러지가 생성되고 처리 속도도 느리다는 단점을 가지고 있다[6]. 한편, 막분리 및 용매 추출법 역시 기술의 유지 관리 비용이 높고 불완전한 처리가 이루어지는 등 문제점들이 있다[7]. 이러한 단점을 극복하기 위한 대체 기술로 최근 각광받고 있는 것이 이온교환이다.
이온교환 기술은 처리 속도가 빠르고 슬러지가 발생하지 않는다는 장점을 지니며, 처리수의 수질이 높아 중금속 제거에 널리 이용되고 있다. 또한 유가 금속의 회수와 재생을 통한 반복 사용이 가능해 경제적인 측면에서 이점을 지닌다[8~10]. 현재 수처리 공정에서 통상적으로 사용되는 이온교환체는 입자상 이온교환수지이나, 또 다른 형태인 섬유상 이온교환체가 가지는 여러 가지 장점으로 인하여 최근 이온교환섬유에 대한 연구가 활발히 진행되고 있다. 이온교환섬유의 경우, 입자상에 비하여 상대적으로 표면적이 매우 크고, 용액 투과성이 높으며, 섬유의 특성상 다양한 밀도 및 형태로의 가공이 용이하다[11~13]. 또한 무기이온 형태의 중금속류를 처리하는데 있어 이온교환섬유 표면 기능기까지의 반응/확산거리가 가깝기 때문에 처리 속도도 매우 빠르다[14~16].
본 연구에서는 수중의 6가 크롬을 처리하기 위한 아크릴계 섬유의 표면개질을 통한 이온교환체를 합성하고, 이를 이용하여 크롬 제거 효율을 평가하고자 한다. 또한, 폐수 내 존재할 수 있는 공존 이온 및 유입 폐수의 성상에 따른 pH 변화가 처리 효율에 미치는 영향도 함께 고찰해 보았다.
2. Materials and Methods
2.1. 재료 및 시약
이온교환섬유를 합성하기 위한 원료섬유로는 ㈜동양/한일합섬의 아크릴계 섬유 HANILON을 사용하였다. 준비된 섬유를 에탄올을 이용하여 실온에서 하루 동안 세척하여 불순물을 제거한 후, 진공 건조하였다. Diethylenetriamine (DETA, Acros Organics Co., 98.5%)은 수분을 제거하기 위해 40℃에서 진공 건조하였다. Aluminium trichloride hexahydrate (AlCl3・6H2O, Junsei Chemical Co., 97%), potassium chromate (K2Cr2O7, Sigma-Aldrich Chemical Co., 99.5%), potassium dihydrogen phosphate (KH2PO4, Samchun Pure Chemical Co., 99.0%), sodium arsenate dibasic heptahydrate (Na2HAsO4・ 7H2O, Sigma-Aldrich Chemical Co., 98-102%), phenolphthalein (C20H14O4, Yakuri Pure Chemicals Co., Extra pure) 등은 별도의 정제 없이 사용하였다.
2.2. 아크릴계 이온교환섬유의 합성
HANILON 섬유 6 g과 DETA 500 g, AlCl3・6H2O 40 g을 둥근바닥 플라스크(1,000 mL)에 넣고 110℃의 oil bath에서 60분 간 교반하며 반응시켰다. 합성된 섬유는 증류수로 세척하고, 진공 오븐을 이용하여 40℃ (24 h)에서 건조하였다. 이온교환섬유 poly(acrylo-amidino diethylene diamine) (PADD) 합성과정의 화학적 구조는 Scheme 1에 나타내었다.
2.3. 6가 크롬 제거 실험
합성된 PADD를 이용한 수용액 상의 6가 크롬 제거는 회분식 실험으로 수행하였으며, 등온흡착 실험과 동적흡착 실험, pH에 따른 제거 실험 및 경쟁이온 실험, 총이온교환능 실험 등을 실시하여 흡착 특성 및 6가 크롬 처리를 위한 최적 조건을 알아보았다. 실험에 사용한 크롬(VI) 인공폐수는 K2Cr2O7으로 제조한 100 mmol/L 농도의 표준용액을 희석하여 준비하였다, 회분식 실험은 50 mL polypropylene 코니컬 튜브에 기 준비된 크롬 용액 40 mL와 0.2 g/L 용량의 PADD를 주입한 후 회전교반기를 이용하여 20 rpm의 속도로 2시간 동안 반응시켜 수행하였다. 반응 후에는 0.45 μm의 실린지 필터를 이용하여 시료 채취 후 용액 내 잔존 크롬 농도를 분석하였다. 등온흡착 실험에서는 초기 크롬 농도를 0.1, 0.4, 0.7, 1, 2, 5, 10 mmol/L로 제조하여 HCl 용액으로 pH 2로 조정한 후 PADD를 반응시켰다. 동적흡착 실험의 경우, 반응속도를 알아보기 위하여 초기 농도 1 mmol/L의 크롬 용액(pH 2)에 합성한 섬유를 주입하여기 정해진 시간(5, 10, 15, 20, 25, 30, 40, 60, 120분)에 시료를 채취하여 흡착능을 분석하였다.
pH 변화에 의한 크롬 제거 실험은 1 mmol/L 농도의 크롬 용액을 HCl과 NaOH 수용액을 이용하여 pH 2-10의 범위로 조절하여 흡착실험을 실시하였다. 동일한 방법으로 KH2PO4, Na2HAsO4・7H2O로 제조한 1 mmol/L 인산 수용액, 비소(V) 수용액의 pH에 따른 흡착 성능을 시험하였고, 크롬, 인산, 비소를 모두 용해시켜 각각의 농도가 1 mmol/L가 되도록 제조한 혼합 용액의 pH에 따른 흡착능을 실험을 통해 공존이온이 존재할 때 크롬의 흡착능 변화를 알아보았다.
PADD의 총이온교환능은 산-염기 역적정법으로 평가하였다. 0.1 mol/L HCl 수용액 20 mL에 0.01 g의 PADD를 주입하고 20 rpm으로 2시간 동안 회전 교반한 후 시료를 채취하였다. 실린지 필터를 이용하여 용액 10 mL를 취한 뒤 phenolphthalein 지시약을 넣고 0.1 M NaOH 표준용액으로 적정하여 용액 내 잔존 HCl의 양을 구하여 PADD의 총이온교환능을 계산하였다.
2.4. 측정 기기
Fourier transform infrared (FT-IR) spectroscopy (GX model, Perkin Elmer, USA)은 합성 후 섬유(PADD)의 구조 및 개질된 정도를 확인하기 위해 사용되었다. 섬유의 표면 형태는 Field emission scanning electron microscope (FESEM, Quanta 250 FEG, FEI, USA)을 통해 관찰하였으며, 흡착 후 섬유 표면의 크롬 이온은 Energy-dispersive X-ray spectroscopy (EDS) mapping을 통해 확인하였다. 크롬 제거 실험에서의 반응 전후 수용액 내 크롬 농도는 Inductively coupled plasma-optical emission spectrometry (ICP-OES, Prodigy ICP, Teledyne Leeman Labs, USA)로 분석하였다.
3. Results and Discussion
3.1. 합성된 PADD의 FT-IR 분석 및 FESEM 관찰
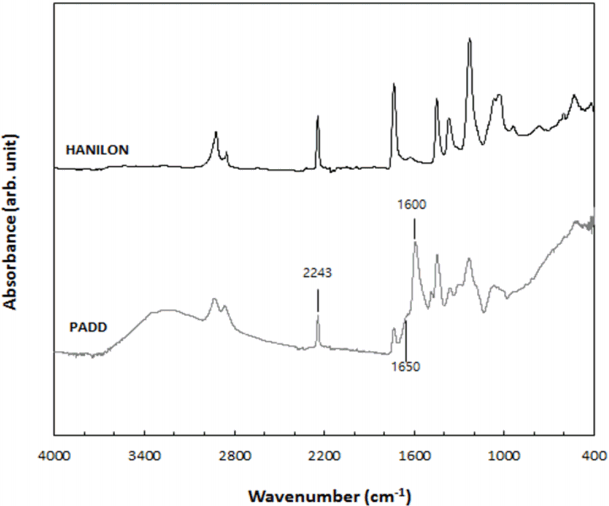
이온교환섬유 PADD는 polyacrylonitrile (PAN)을 주성분으로 하는 아크릴계 섬유(HANILON)에 단량체인 DETA와 함께 AlCl3・H2O를 넣고 grafting 과정을 통해 합성되었다. Fig. 1은 원료섬유 HANILON과 합성된 PADD 섬유의 FT-IR spectrum를 나타낸 것이다. 합성 전후의 spectrum에서 C≡N그룹 (nitrile, 2,243 cm-1)의 피크의 변화와 N-C=N (amidine group, 1,650 cm-1), NH2 (1,600 cm-1), amine그룹 (3,500~2,000 cm-1)의 피크가 나타나는 것을 확인할 수 있다[17]. 이러한 아민기 그룹이 크롬의 제거 효율을 향상시키는 기능기의 역할을 하는 것으로 판단된다.
합성 전 후 섬유의 형태 변화를 확인하기 위해 FESEM 이미지를 관찰 하였다. Fig. 2(a)는 원료섬유의 이미지이며, Fig. 2(b)는 합성 후 PADD의 것이다. 합성 전 30.98 ± 1.52 μm의 평균 직경을 나타내는 HANILON에 비하여 약 42.65 ± 4.00 μm 정도로 섬유의 평균 직경이 증가한 것을 확인할 수 있었으며, 섬유 표면에도 변화가 생긴 것을 관찰할 수 있었다. 이는 섬유 표면에 기능기의 grafting이 효과적으로 이루어졌음을 간접적으로 나타내는 결과라 할 수 있다. 또한 크롬(VI) 용액에서의 이온교환 실험 후 EDS-mapping을 통해 섬유 표면에 크롬 이온이 고르게 존재함을 확인하였다(Fig. 3).
3.2. 등온흡착 실험
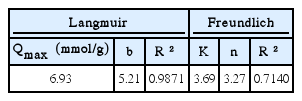
초기농도 0.1, 0.4, 0.7, 1, 2, 5, 10 mmol/L인 6가 크롬 수용액과 PADD를 반응시켜 평형 농도와 흡착능의 관계를 살펴보았다. Fig. 4는 실험 데이터를 각각 Langmiur 등온흡착모델과 Freundlich 등온흡착모델에 적용시켜 선형피팅한 그래프이다. 두 식을 통해 구한 parameter 수치는 Table 1에 나타냈다. Langmiur 등온흡착모델과 Freundlich 등온흡착모델은 각각 다음과 같이 표현된다.

Isotherm model analysis: (a) Langmiur (b) Freundlich isotherm model plot for Cr(VI) adsorption on PADD.
위 식에서 Qeq (mmol/g)는 흡착제 단위 중량당 흡착된 흡착질의 양, Qmax (mmol/g)는 최대흡착능, Ceq는 용액의 평형농도, b, n, K는 식으로부터 구한 상수값이다. 상관계수(R2)값은 Langmuir 모델 적용시 0.9871, Freundlich 모델 적용시 0.7140으로 나타나 단분자 흡착을 가정하는 Langmuir 모델이 PADD와 크롬의 흡착을 설명하는데에 더 부합한 것으로 확인되었다. Langmuir 등온흡착모델의 이론상 최대 흡착능인 Qmax값은 6.93 mmol/g으로 나타났다.
3.3. 동적흡착 실험
이온교환섬유 PADD와 크롬간에 반응하는 흡착속도를 알아보기 위하여 반응시간에 따른 흡착량을 알아보는 실험을 수행하였다. 120분 동안 반응했을 때의 시간에 따른 흡착량을 분석해 본 결과, 반응 시작과 동시에 빠른 흡착이 일어나고, 2차 흡착 단계에 진입하여 대부분의 흡착반응은 30분 내에 이루어지는 것을 확인할 수 있었다. 이 반응속도 실험 데이터를 Lagergren 유사일차 및 이차 속도식에 적용하여 선형피팅한 결과를 Fig. 5에 도시하였으며, 이로부터 구한 parameter 수치를 Table 2에 나타내었다. Lagergren 유사일차속도모델과 유사이차속도모델은 각각 아래와 같이 표현된다.
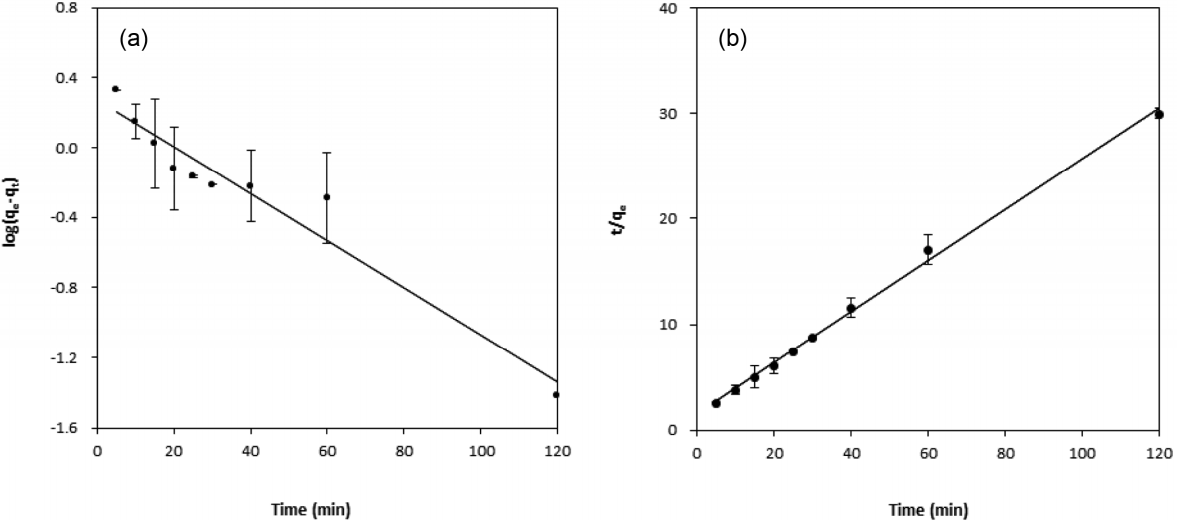
Kinetic model analysis: Lagergren (a) pseudo first-order (b) pseudo second-order plot for Cr(VI) adsorption on PADD.
이 식에서 t (min)는 반응 시간을, qe와 qt (mmol/g)는 각각 평형 상태와 시간 t에서의 흡착능을, k1 (/min)과 k2 (g/mmol・min)는 각각 Lagergren 유사일차속도모델과 유사이차속도모델의 흡착속도상수를 나타낸다. 유사일차속도모델과 유사이차속도모델에서 도출된 상관계수(R2) 값은 각각 0.9388과 0.9973으로, 결과를 유사이차모델에 적용시키는 것이 Cr(VI)과 PADD간의 반응속도를 보다 정확하게 산출할 수 있을 것으로 사료된다.
3.4. pH 및 경쟁이온의 영향
Cr(VI)은 수용액에서 pH에 따라 다양한 형태의 이온으로 존재하며, 이러한 이온 형태에 따라 제거율에 영향을 미치게 된다. 또한, 수용액 내 공존 이온에 의해서도 크롬 흡착능이 감소할 수 있다. 따라서 pH가 6가 크롬 및 공존 음이온의 흡착에 미치는 영향과 다른 음이온들이 크롬의 흡착에 미치는 영향을 조사해 보았다.
Fig. 6은 PADD의 인산, 크롬(VI), 비소(V) 음이온에 대한 각각의 흡착능이 초기 pH 2-10 범위에서 어떻게 변화하는지에 대한 결과를 나타낸 것이다. 크롬 흡착능은 용액의 pH가 2일 때 최대를 나타냈고, 인산은 pH 3에서, 비소는 pH 4에서 최대 흡착능을 보였다. 이것은 pH에 따라 각 이온의 화학종이 다르기 때문으로 해석할 수 있다. 우선 낮은 pH에서 PADD의 아민기(-NH2)는 -NH3+로 양전하를 띠게 되어 음이온과 반응하기에 보다 더 적합한 형태로 변하게 된다. 또한 pH 2에서 크롬(VI) 이온은 주로 HCrO4- 형태로 존재하고, 인산 이온은 pH 3에서 H2PO4-, 비소(V) 이온은 pH 4에서 H2AsO4-의 형태로 존재하는데, 이들 이온은 모두 -1가 형태로 PADD의 기능기와 반응하기에 좋은 조건을 가진 것이다.
Fig. 7은 인산, 크롬(VI), 비소(V)가 같은 농도(1 mmol/L)로 존재하는 경우에 PADD의 각 음이온에 대한 흡착능이 초기 pH 2-10 범위에서 어떻게 변화하는지에 대한 실험 결과이다. 세 음이온이 함께 존재할 때, 비소와 인산 흡착량은 전 pH 구간에서 0.5 mmol/g 미만으로, 최대흡착량이 3.73 mmol/g인 크롬에 비하여 현저히 낮았다. 크롬 역시 개별 흡착에서 확인된 최대흡착량 4.11 mmol/g와 비교하면 흡착량의 저하가 나타났지만, 전체적인 pH 변화에 따라 큰 차이는 없는 것으로 확인되었다. 또한, PADD가 다른 공존이온에 비하여 크롬에 대한 선택도를 가지고 있음을 나타내는 결과이기도 하다.
3.5 총이온교환능
이온교환섬유 PADD의 총이온교환능은 산-염기 역적정법을 이용하여 구하였다. 0.1 mol/L의 HCl 용액과 섬유를 반응시켜 흡착된 양을 0.1 mol/L의 NaOH로 적정하여 구하였을 때의 흡착량은 4.7 mmol/g으로 나타났다. 이 결과로 볼때, 본 연구를 통해 개발된 PADD는 크롬에 대한 선택성을 가지는 이온교환섬유이며(총 이온교환능 4.7 mmol/g 중 크롬 흡착능이 4.11 mmol/g), 공존이온에 대한 효율 저감도 크지 않음을 확인할 수 있었다.
4. Conclusion
아크릴계 섬유를 DETA와 AlCl3・6H2O를 이용하여 화학적으로 개질한 이온교환섬유 PADD를 수용액 내 6가 크롬 제거에 적용하여 등온흡착 및 동적흡착 특성과 pH 및 공존음이온의 영향을 확인한 결과 다음과 같은 결론을 얻을 수 있었다.
1) 원료섬유와 합성된 이온교환섬유를 FT-IR로 분석한 결과, 합성 후 섬유의 C≡N (nitrile)기 피크가 작아짐을 확인할 수 있었고, 합성 이후 섬유의 평균 직경이 증가하였다. 산-염기 역적정법을 통해 구한 PADD의 총이온교환능은 4.70 mmol/g으로 비교적 높은 수치임을 확인할 수 있었다.
2) Cr(VI) 제거 등온흡착실험 결과 Langmuir 등온흡착모델이 Freundlich 모델보다 더 적합한 것으로 나타나 단분자 흡착을 통한 이온교환 반응이라는 것을 확인하였다. Langmuir 모델로부터 도출된 PADD의 크롬 최대 흡착량은 6.93 mmol/g이었다.
3) Cr(VI) 제거 동적흡착실험 결과를 Lagergren 유사일차 및 유사이차 속도모델에 적용한 결과 유사이차속도모델에 더 잘 모사되었으며, 반응 초기 빠른 흡착을 통해 대부분의 흡착이 이루어짐을 알 수 있었다.
4) Cr(VI), 인산, As(V) 이온의 pH 변화에 의한 제거실험을 통해 pH에 따른 이온의 화학종 변화가 PADD의 음이온교환능에 영향을 미치는 것을 확인하였으며, 다른 두 음이온에 비해 Cr(VI)의 선택성이 높게 나타났다. 상기 결과를 종합해 볼 때 본 연구에서 개발한 PADD 소재는 Cr(VI) 제거에 높은 성능이 있음을 확인할 수 있었으며, 향후 재생실험, 연속흐름실험 및 현장폐수와의 적용성실험을 통해 그 효율 및 특성을 파악하고 최적 조건을 설계하여 실제 크롬 폐수 처리 공정에서 PADD의 활용 가능성을 확인해 볼 필요성이 있다.
Acknowledgements
본 연구는 “특화전문대학원 연계 학연협력 지원사업”과 환경부 “환경산업선진화기술개발사업(과제번호: 201400015-0018)”에서 지원받았으며, 이에 감사드립니다.