|
The Korean text of this paper can be translated into multiple languages on the website of http://jksee.or.kr through Google Translator.
AbstractObjectivesAs the variety and quantity of recalcitrant pollutants such as pharmaceuticals, pesticides, endocrine disruptors, and cosmetic products discharged into water bodies steadily increase, the need for AOPs following biological wastewater treatment processes is growing. In this study, we compared the Total Organic Carbon (TOC) removal capabilities of conventional AOPs, ultrasound, hydrogen peroxide, and persulfate-based multiple AOPs on the final effluent of S wastewater treatment plant. The study also evaluated the feasibility of wastewater reuse by examining the optimal operating conditions of the applied AOPs.
MethodsThe removal characteristics of TOC were investigated based on reaction time, US frequency, and oxidant dosage for the following conditions: ultrasound (US) alone, individual treatments with hydrogen peroxide (H2O2) and persulfate (PS) as oxidants, combined US/H2O2 and US/PS dual AOPs, and a US/PS/H2O2 multi-AOPs system.
Results and DiscussionOnly US oxidation treatment at 80 kHz for 60 minutes resulted in a 14.4% TOC removal efficiency. Individual treatment with H2O2 at 174 mM showed 69.2% removal efficiency, while persulfate oxidation treatment at 43.5 mM showed 13.8%. The PS/H2O2 oxidation treatment showed 68.5% removal efficiency at 174 mM H2O2 and 0.52 mM PS, and an 85.3% removal efficiency at 2.08 mM PS and 350 mM H2O2 conditions. Under the same 80 kHz ultrasound conditions, the combined US and other oxidant treatment resulted in an increased TOC removal efficiency: 87.8% for US/H2O2 at 174 mM H2O2, and 81.9% for US/PS at 43.5 mM PS. Additionally, the multi-treatment with US, PS, and H2O2 showed a removal efficiency of 87.0% at 2.08 mM PS and 350 mM H2O2, and 91.1% at 174 mM H2O2 and 0.52 mM PS conditions.
ConclusionIn this study, among the AOPs, the oxidation treatment with US/PS/H2O2 exhibited the highest TOC removal efficiency at 91.1%. The integration of chemical oxidants with US demonstrated significant improvement in TOC removal capabilities, with PS showing superior performance at the same concentration conditions among the utilized chemical oxidants in the multi-AOPs. Although H2O2 also displayed commendable TOC removal abilities, its oxidation efficiency was lower at low concentration injections, whereas higher concentrations of H2O2 injections proved to be more effective in oxidation.
요약목적수계로 배출되는 의약품, 살충제, 내분비계 교란물질, 미용용품 등 난분해성 오염물질의 종류와 양이 점차 증가함에 따라 생물학적 수처리 공정 후 AOPs의 필요성이 증가하고 있다. 본 연구에서는 기존의 AOPs와 초음파, 과산화수소 그리고 과황산염을 이용한 다중 AOPs에 대하여 S 하수처리장 최종방류수를 대상으로 TOC 제거능을 비교하고 적용된 AOPs의 최적 운전 조건 검토를 통해 하수처리수 재이용 가능성을 조사하였다.
방법초음파(Ultrasound, US) 단일 처리, 산화제로 사용된 과산화수소(H2O2) 및 과황산염(Persulfate, PS)의 단일 처리, US와 H2O2, PS를 융합한 US/H2O2, US/PS 이중 AOPs 그리고 US/PS/H2O2 다중 AOPs의 처리시간, 초음파 주파수 및 산화제 주입량에 따른 TOC 제거 특성을 조사하였다.
결과 및 토의80 kHz, 60 min 조건에서 US 단일 산화처리한 결과 14.4%의 TOC 제거율을 나타냈고 174 mM 조건에서 H2O2 단일 산화처리는 69.2%, PS 단일 산화처리는 43.5 mM 조건에서 13.8%를 나타냈으며 PS/H2O2 처리는 H2O2 174 mM 및 PS 0.52 mM 조건에서 68.5%, PS 2.08 mM 및 H2O2 350 mM 조건에서 85.3%를 나타냈다. 동일한 80 kHz 초음파 조건에서 US와 산화제 융합 시 US/H2O2는 H2O2 174 mM 조건에서 87.8%, US/PS는 PS 2.08 mM 조건에서 71.4%로 증가하였다. 또한 US, PS 및 H2O2와의 다중 처리 시 PS 2.08 mM 및 H2O2 350 mM 조건에서 87.0%, H2O2 174 mM 및 PS 0.52 mM 조건에서 91.1%의 TOC 제거율을 나타냈다.
1. 서 론1.1. 연구의 목적수역으로 배출되는 의약품, 살충제, 내분비계 교란물질, 미용용품 등 난분해성 오염물질의 종류와 양이 점차 증가함에 따라 기존의 생물학적 처리공정만으로는 하수처리수의 효율적인 처리에 어려움이 있어 AOPs를 이용한 3차 처리를 필요로 한다. 또한 기후온난화로 인한 강우의 불확실성이 증가함에 따라 수질의 안정적인 확보의 어려움은 커지고 있어 하수 처리수 재이용에 대한 요구가 증가하고 있다[1].
국내의 공공하수처리시설의 하수처리수 재이용량은 2000년 기준 167백만톤/년(재이용율 2.9%)에서 2008년 712백만톤/년(10.8%), 2015년 1,027백만톤/년(14.7%) 그리고 2022년 기준 1,137백만톤/년(15.4%)으로 점차 증가하고 있다[2,3]. 그러나 하수처리수를 산업용수나 생활용수로 재이용하기 위해서는 처리수 중에 잔류하는 생물학적 난분해성 물질에 대한 제거가 필수적이므로 하수처리수 내의 생물학적 난분해성 유기물질을 대표하는 총유기탄소(Total Organic Carbon, TOC)의 효과적인 제거가 필요하다. 기존의 유기물질 측정지표였던 CODMn는 하・폐수 중 총 유기물질의 30~60% 내외만이 측정 가능하다는 문제가 있어 하수처리 방류수 내 난분해성 유기물을 충분히 대표하지 못한다. 또한 산업의 고도화에 따른 신규 화학물질이 매년 증가하고 PFAS나 PFOA와 같은 난분해성 물질 처리의 중요성이 증가하고 있고 2021년부터 CODMn에서 TOC로 폐수 및 공공폐수처리의 방류수 수질기준 및 배출수 수질기준이 변경되었다. 현재 공공폐수처리시설의 방류수 수질기준은 I, II 지역 기준으로 TOC 15 mg/L 이하로 설정되었고 향후 2026년부터 10 mg/L 이하로 강화될 것으로 검토 및 추진 중에 있다[4]. 또한 환경부는 낙동강 수계에 TOC 수질오염총량관리제의 도입을 목적으로 TOC 총량관리 시범 계획에 대하여 밝힌 바가 있다. 이처럼 TOC 관리의 중요성이 증가함에 따라 현재와 미래의 수질관리의 주요 지표로서 TOC의 의미가 증가할 것으로 판단된다.
AOPs는 기존의 일반적인 공정보다 ∙OH와 같은 강력한 산화제의 발생을 유도하여 오염물질을 산화분해시켜 최종산물인 CO2, H2O 등 무기화합물로 전환시키는 기술이다. 가장 대표적으로 사용되는 화학종은 ∙OH로 높은 표준산화환원전위(Eo(∙OH/OH-) = 2.8 VNHE)와 108~1010 M-1s-1의 이차반응속도 상수의 특성을 띠어 다양한 유기화합물과 빠른 속도로 반응한다[5]. AOPs는 주로 O3, UV, H2O2의 조합을 기본으로 하여 초음파, 광촉매, 전기분해 등과 조합한 여러 가지 기술이 존재한다[6]. O3와 H2O2 조합공정은 H2O2가 이온화되어 생성된 HO2-에 의한 개시반응을 시작으로 O3과 반응하여 생성되는 ∙OH, ∙O2- 등의 라디칼 산화 반응을 이용한다[7]. Peroxone이라고 명명하여 국내 정수장에 활용되고 있는 기술 중 하나이지만 O3 생성을 위한 설비와 대기로 방출되는 O3을 처리하기 위한 설비 등이 필요하다. Fe(II)과 H2O2 조합공정은 최초 발견자 H. J. H. Fenton의 이름을 따서 fenton 반응으로 명명되는데, 2가 철염과 H2O2가 섞여 있을 때 보라색 계열을 띠면서 유기물질을 산화시키는 전통적인 AOPs이다[8]. 펜톤 반응은 추가적인 에너지 공급 없이 비교적 우수한 유기물 제거 특성을 보이지만, pH가 중성에 가까워지면 Fe(OH)3 형태로 침전되면서 다량의 슬러지 발생하며 색도 처리에 대한 문제점을 지니고 있어 추가적인 처리가 필요하다. UV와 H2O2의 조합공정은 H2O2 기반의 기본적인 AOPs로 자외선의 에너지에 의해 H2O2의 산소 원자 간 공유결합이 끊기면서 생성되는 ∙OH의 산화 반응을 이용한다[5]. UV/H2O2 공정은 잔류 부산물을 생성하지 않지만 O3 기반 공정에 비해 많은 H2O2 주입을 요구하며, 질산염과 같은 화합물에 의해 자외선 효과가 저하될 수 있다[9]. 이와 달리 초음파 공정은 비교적 단순하고 슬러지와 같은 부산물을 발생시키지 않고 무해하며 주로 O3, H2O2, 광촉매 등과 조합하여 사용되어 유기물질의 처리 효과를 높일 수 있다[10,11]. Son 등(1996)은 난분해성 유기물인 TCE, benzene, 2,4-DCP에 대한 제거실험을 한 결과 TCE 20 mg/L, 반응시간 60 min 조건에서 90% 이상의 TCE 제거율, benzene 20 mg/L, 반응시간 80 min 조건에서 75% 이상의 benzene 제거율, 그리고 2,4-DCP 20 mg/L, 반응시간 120 min 조건에서 80% 이상의 2,4-DCP 제거율을 보였다[12]. Wang 등(2009)은 US와 H2O2를 조합하여 rhodamine B 분해에 대한 연구를 한 결과 용액의 온도 50℃, pH 3.0, 압력 0.6 Mpa, H2O2 100 mg/L, 반응시간 180 min 조건에서 rhodamine B 농도 50 mg/L에서 63.4%, 10 ppm에서 98.9%의 제거율을 보였다[13]. 반면, Lastre-Acosta 등(2014)에 따르면 US와 H2O2를 조합함으로써 H2O2가 radical scavenger로 작용할 수 있음을 보이기도 했다. US/H2O2 조합 공정을 통해 반응시간 120 min, US 주파수 및 출력 580 KHz・22 W, SDZ 25 mg/L, 온도 30℃, 초기 pH 5.5 조건에서 sulfadiazine (SDZ) 제거실험을 한 결과, H2O2가 없는 조건에서 90%의 제거율을 나타냈고, SDZ 25 mg/L 완전 산화에 필요한 H2O2의 이론적 화학반응량 기준으로 단위 H2O2 주입 조건에서 약 82%의 제거율을, 25배의 H2O2 주입 조건에서 약 73%의 제거율을 나타내어 최소 8%에서 최대 17%의 제거율 감소를 나타냈다[14]. Siddique 등(2014)은 US와 광촉매(TiO2)를 결합하여 Reactive Blue 19 분해에 대한 연구를 하였다. US 및 TiO2 단일 처리는 염료 농도 100 mg/Lm, 반응시간 120분 조건에서 각각 7.2%(출력 240 W)와 10.18%의 TOC 제거율을 보였지만, US/TiO2 처리는 염료 농도 100 mg/L, 반응시간 120분, 초음파 출력 240 W, TiO2 농도 300 mg/L 조건에서 55.0%의 TOC 제거율을 보였다[15]. Zhang 등(2022)은 금 제련 폐수를 대상으로 시안화물의 제거와 구리의 회수를 목적으로 US/O3 조합 공정에 대한 연구를 하였다. O3 유속 80 L/h, 온도 25℃, 반응시간 15 min 및 US 출력 밀도 80 W/L의 조건에서 99.96%의 시안화물 제거율과 99.3%의 구리 회수율을 보였다.16) 한편, 유기물질로 파과된 활성탄 재생을 위해서 초음파가 사용된 바도 있는데, Joo 등(2023)은 활성탄 재생을 목적으로 초기 재생능의 30% 이하로 파과된 입상활성탄에 US/fenton 조합 공정을 적용하여 재생시켰다. 그 결과 Fe2+ 10 mmol/L, H2O2 1,000 mmol/L, 반응시간 120 min, US 주파수 40 kHz 조건에서 68.5%의 재생효율을 보였다[17]. 근래에 들어, 산화제로 H2O2 및 O3뿐만 아니라 과황산염을 활용한 연구도 다수 진행되고 있는데, Lee 등(2021)은 35 KHz 초음파 반응기와 활성화된 PS를 조합하여 ibuprofen (IBP)의 분해에 대한 연구를 하였다. 그 결과 IBP 24 μM, PS 0.8 mM, US 주파수 35 KHz, calorimetric power density (CPD) 76W/L, pH 4.9, 반응시간 60 min, 교반속도 400 rpm 조건에서 수돗물과 하천수의 IBP 제거율은 각각 90.4%와 85.3%이었다[18]. Kim 등(2012)은 난분해성 산업폐수처리를 위하여 UF/Ozone/UV/Catalyst 다중 AOPs를 이용하여 초기 CODCr 78.0 mg/L 조건에서 약 90%, 초기 CODMn 27.0 mg/L 조건에서 약 90% 제거율을 보였다[19]. Chung 등(2021)은 하수처리 방류수의 3차처리를 위하여 O3/H2O2. O3/UV, O3/GAC 공정을 이용하였다. O3/H2O2 공정의 경우 O3주입농도 7.0 mg/L, H2O2와 O3 주입비(H2O2/O3) 0.43/1.0, 유입 TOC가 5.6 mg/L 조건에서 62%의 제거율을, O3/UV 공정의 경우 유입 TOC 5.6 mg/L 조건에서 61.0%의 TOC 제거율을, O3/GAC 공정의 경우 GAC 공상체류시간 20 min, 초기 TOC 5.6 mg/L 조건에서 TOC의 제거율은 58.9%의 제거율을 보였다[20]. Pourgholi 등(2018)은 섬유 폐수의 COD 및 색도 제거를 위해 UV/H2O2/O3 공정을 이용하였다. pH 6, 10 g O3/L, 그리고 10 g H2O2/L・hr 조건에서 89.2%의 색도 제거율과 76.7%의 COD 제거율을 보였다[21]. 위와 같이 다중 AOPs를 적용한 사례에서 기존의 AOPs 공정에서 처리수 제거능의 향상을 도모하였다. 그러나 하수처리수나 산업폐수와 같이 난분해성 유기물이 포함된 경우 O3/H2O2, UV/H2O2 등 일반적인 AOPs 공정만으로는 농업 용수 및 산업용수에 이용 가능하도록 처리하기는 충분치 못하다는 한계점이 존재하여 다양한 산화제를 융합한 다중 AOPs에 대한 연구가 필요하다.
본 연구에서는 범용성 있는 하수처리수 재이용을 위하여 실하수처리장 방류수를 대상으로 US와 산화제인 H2O2 및 PS를 이용한 US/H2O2, US/PS, US/PS/H2O2 다중 AOPs에 대한 연구를 하여, 하수처리 방류수 내 잔류 TOC의 효과적인 제거를 통해 TOC 제거 효율 향상을 목적으로 처리시간, US 주파수 및 산화제 주입량에 대하여 조사하여 TOC 제거를 비교・평가하였다.
1.2. 이론적 배경1.2.1. 초음파화학액상에 20 kHz 이상의 초음파를 조사하였을 때 초음파 캐비테이션 현상(cavitation effect)이 나타나 압력 변화로 인한 수축과 팽창의 과정을 거쳐 공동화 기포(cavitation bubble)가 발생하는데, 기포 속 고온고압의 에너지에 의해 수증기가 해리되어 H· (hydrogen radical)과 ·OH (hyderoxyl radical)이 생성된다[22,23]. Fig. 1(b)는 이러한 캐비테이션 현상을 도식화하여 나타낸 것이다. 수용액에 US 조사 시 용존 산소가 있는 조건에서 라디칼 및 산화제의 생성은 다음 식(1)~(16)과 같은 메커니즘을 따르는 것으로 알려져 있다[24,25]. 이 반응은 US 주파수 및 출력, 반응기 용적, 용액의 온도 및 압력, 용해 가스의 종류 및 농도, 용해 이온의 종류 및 농도, 용매의 특성 등에 의해 라디칼 및 산화제의 생성 속도에 영향을 받을 수 있고, 이러한 US화학 메커니즘으로부터 하수처리수 내의 제거 대상 물질이 고온고압의 충격파에 의한 열분해 또는 라디칼 반응으로 산화분해될 수 있다.
H2O + US⦖ → H∙ + ∙OH (1)
O2 → 2O∙ (2)
∙OH + ∙OH → H2O + O∙ (3)
∙OH + ∙OH → H2 + O2 (4)
∙OH + ∙OH → H2O2 (5)
∙OH + H2O → H2O2 + H∙ (6)
H∙ + ∙OH → H2O (7)
H∙ + H∙ → H2 (8)
O∙ + O∙ → O2 (9)
O∙ + H2O → 2∙OH (10)
O2 → O∙ + O∙ (11)
O2 + O∙ → O3 (12)
H∙ + O2 → HO2∙ (13)
HO2∙ + H∙ → H2O2 (14)
H2O∙ + H2O∙ → H2O2 + H2 (15)
2H2O∙ → 2∙OH + H2 (16)
이때, 식(17)과 같이 초음파 조사 시 산화제로 H2O2를 첨가하면, H2O2는 산화 환원 전위가 낮은 반응성 종인 ∙O2- 및 1O2와 함께 ∙OH로 분해될 수 있다. 반면에 H2O2는 식 (18)과 같이 ∙OH과 반응할 수 있어 과량의 H2O2는 ∙OH를 소비하는 scavenger로 작용할 수 있다[26].
H2O2 +US⦖ → 2∙OH (17)
∙OH + H2O2 → H2O + O2 (18)
1.2.2. 초음파/과황산염(US/PS)과황산염(Persulfate, PS)은 황산염(Sulfate)과 퍼옥소기(Peroxo group)가 결합된 형태의 화합물로 일과황산염(Peroxymonosulfate, PMS; HSO5-)과 이과황산염(Peroxydisulfate, PDS; S2O82-)을 의미한다. PS의 경우 비교적 최근에 적용되고 있는 산화제로 황산 라디칼은 과산화수소와 유사한 라디칼 산화력을 지니고 있으며(E0(SO4-∙) = 2.4~3.1 VNHE) 광범위한 활성화 기법, 높은 라디칼 전환율, 낮은 자가분해율, 처리 대상물질에 도달하기까지 소모가 적은 특성 등의 장점을 지니고 있다. 그러나 과황산염은 대부분의 유기물질과 반응성이 낮아 PS에 의한 직접 산화분해 효과는 기대하기 어려워 화학적 활성이 필요하다[27,28,29]. PS 기반 AOPs는 다음 Fig. 2와 같이 균일계와 불균일계 방식으로 구분할 수 있다. PS의 균일계(Homogeneous) 활성은 다시 에너지를 인가하는 방식과 전이 금속을 이용한 전자 전달 방식으로 구분되고, 불균일계(Heterogeneous) 활성은 촉매의 종류에 따라 금속 기반과 탄소 기반 촉매로 구분된다. 대표적으로 식(17)과 같이 에너지 인가를 통한 열 또는 자외선에 의해 활성화될 수 있고, 식(18)과 같이 전이 금속을 이용한 전자 전달 방식에 의해 활성화될 수 있다[30,31].
S2O82- + Heat/UV → 2SO4-∙ (17)
S2O82- + Mn+ → SO4-∙ + SO42- + M(n+1)+ (18)
PS와 US와의 반응은 다음 식 (19)~(29)와 같은 메커니즘을 따르는 것으로 알려져 있다[32]. 이러한 반응을 통해 여러 종류의 라디칼 및 산화제가 생성 및 분해되는 과정에서 수중 유기 물질과 반응하여 산화분해시킬 수 있다.
S2O82-+ US⦖ → 2SO4-∙ (19)
H2O + US⦖ → ∙OH + ∙H (20)
H2O + 2SO4-∙ → H+ + 2SO42- + ∙OH (21)
SO4-∙ + SO4-∙ → S2O82- (22)
∙OH + ∙OH → H2O2 (23)
∙OH + SO4-∙ → HSO5- (24)
SO4-∙ + HSO5- → HSO4- + SO5-∙ (25)
∙OH + HSO5- → SO5-∙ + H2O (26)
2SO5-∙ → S2O82- + O2 (27)
S2O82- + SO4-∙ → SO42- + S2O8-∙ (28)
S2O82- + ∙OH → OH- + S2O8-∙ (29)
2. 재료 및 방법2.1. 시약 및 재료본 연구에서 사용된 시료는 천안시 S 공공하수처리장 최종 방류수로, S 하수처리장은 DNR 및 DeNiPho 및 BIONAD 공법과 총인처리 및 자외선 소독 등의 공법으로 처리되고 있고 시료는 최종방류수를 수질오염공정시험기준에 의거하여 2 L 무균 채수병에 채취하였다. 방류수는 실험 전 시료의 균질성을 확보하기 위하여 Whatman사의 GF/C(1.2 μm) 유리섬유 여과지를 사용하여 감압여과장치를 통해 잔류 부유물질을 제거하였다. 또한 산화제로서 hydrogen peroxide (34.5%)와 potassium persulfate (98~102%)는 SAMCHUN사의 제품을 사용하였다. TOC 분석을 위한 UV/VIS Spectrophotometer는 HACH사의 DR 5000 모델을 사용하였고, TOC 분석의 표준물질로는 글루코스(glucose) 용액을 제조하여 사용하였는데 이때 분석된 오차율은 ± 2%였다.
2.2. 초음파 발생 장치 구성본 연구에서 사용한 초음파 발생 장치와 발생원리를 Fig. 1(a), (b)에 나타내었다. 초음파는 16 kHz 이상의 진동수를 갖는 음파로서 진동수가 낮은 초음파가 액상의 매질에 조사될 때 공동이 일어나고 공동이 파괴되는 과정에서 10,000 K에 달하는 국부적인 고온 영역이 발생하여 입자의 물리화학적 변화를 촉진시킨다.
초음파 발생 장치는 ㈜고도기연사의 NXGC-4F 모델과 ㈜경일MEGASONIC사의 MW-0609AP-06-750K 모델을 사용하였다. 각 장치는 Ultrasound oscillator, Ultrasound reactor 및 Connecter로 구성되어 있고, NXGC-4F 모델의 크기는 250(W) × 300(L) × 200(H) mm이며 작동 주파수는 40, 80, 132, 164 kHz, MW-0609AP-06-750K 모델의 크기는 320(W) × 460(L) × 165(H) mm이며 작동 주파수는 750 kHz이다.
2.3. 산화제 주입에 따른 AOPs의 TOC 제거 특성효과적인 초음파 처리를 위해서는 ∙OH, SO4-∙등과 같은 강력한 산화력을 가진 라디칼의 생성이 중요하다. 이를 위해 산화제로 H2O2와 PS를 이용하여 하수처리수 내 TOC 제거를 위한 최적 주입 조건을 산출하고자 하였다. 먼저 초음파 단일 처리로부터 최적의 접촉시간과 주파수에 대한 조건을 산출한 후 US와 H2O2를 융합하여 H2O2의 주입량을 변수로 87, 174, 343, 567 mM 주입하였고(US/H2O2 이중 처리), 같은 방법으로 최적 초음파 처리 조건에서 PS를 융합하여 PS의 주입량을 변수로 0.52, 2.08, 3.12, 10, 20, 43.5 mM 주입하였다(US/PS 이중 처리). 또한, 앞선 US/PS의 최적 조건에서 H2O2를 융합하여 H2O2를 변수로 50, 100, 150, 200, 250, 300, 350 mM 주입하였고(US/PS/H2O2 다중 처리), 앞선 US/H2O2의 최적 조건에서 PS를 융합하여 PS를 변수로 0.52, 2.08, 4.16, 6.24 mM 주입하였다(US/PS/H2O2 다중 처리). 초음파 내부 반응기의 수위는 반응기 내부에 놓은 500 mL 비커 내 처리수와 동일 수위로 하여 수돗물로 채웠다. 또한 초음파 반응 진행 시 반응기 내부 액상의 온도는 초기 약 24~27℃에서 30분 경과 시 약 54~57℃, 60분 경과 시 약 67~70℃였다.
본 연구에서 실험기간 동안 사용된 하수처리수의 성상은 다음 Table 1과 같다. TOC는 평균 8.7 mg/L, T-N은 평균 6.1 mg/L, T-P는 평균 0.30 mg/L, pH는 평균 6.96, SS는 평균 4.0 mg/L, 수온은 평균 21.4℃로 나타났다. 성분 분석값이 조금씩 다른 이유는 강우의 영향으로 보이며 강우 시 T-N 6~7 mg/L, T-P 0.1~0.2 mg/L로 화창한 날 대비 대략 T-N 2 mg/L, T-P 0.2 mg/L정도 낮은 수준으로 측정되었고, SS 4.0~6.0 mg/L로 화창한 날 대비 대략 1.5 mg/L정도 높은 수준으로 측정되었다.
3. 결과 및 고찰3.1. US 단일 산화처리US 단일 산화처리에서 주파수별 영향을 조사하기 위하여 주파수 40~750 kHz 조건에서 산화실험을 진행하였고 처리 전 초기 TOC 농도는 10.4 mg/L이었다. Fig. 3(a)는 하수처리장 최종방류수 250 mL, US 접촉시간 60 min 조건에서 US 주파수를 변수로 하여(40, 80, 132, 168, 720 kHz) 주파수에 따른 TOC 제거율을 나타낸 그래프이다. 그 결과 주파수 80 kHz 조건에서 14.4%로 가장 우수한 TOC 제거 특성을 보였다. 일반적으로 세정과 추출 등 초음파 물리적 효과(Sonophysical effects)는 미세 기포의 크기와 내부 에너지가 상대적으로 크기 때문에 20-40 kHz의 낮은 주파수 조건에서 효율적인 것으로 알려져 있고, 오염물질의 분해와 물질의 합성 등 초음파 화학적 효과(Sonochemical effects)는 작은 크기의 기포가 더 많이 발생하고, 빠른 주기로 생성 및 성장 그리고 폭발을 반복하면서 더 빠르게 라디칼이 생성되기 때문에 비교적 높은 주파수 조건에서 효율적인 것으로 알려져 있다[33]. 본 연구에서는 US 단일 처리 시 주파수에 따른 TOC 제거능이 가장 우수한 80 kHz (400 W) 조건으로 실험을 진행하였다. 각 실험 별 처리 전 초기 TOC의 농도가 조금씩 다른 이유는 강우의 영향 및 여러 번 샘플링 하였기 때문이다.
US 단일 산화처리에서 반응시간별 영향을 조사하기 위하여 30~120 min 조건에서 산화실험을 진행하였고 처리 전 초기 TOC 농도는 9.7 mg/L이었다. Fig. 3(b)는 Fig. 3(a)와 동일한 방류수와 80 KHz US 조건에서 US 접촉시간을 변수로 하여 (30, 60, 90, 120 min) TOC 제거능을 나타낸 그래프이다. 실험마다 최종방류수의 미미한 TOC의 변동이 있어 TOC 제거량(mg/L)으로부터 TOC 제거율(%)을 산출하였다. 그 결과 US 접촉시간 60 min 조건에서 13.4%로 가장 우수한 TOC 제거 특성을 보였다. 따라서 US 단일 처리만으로는 하수처리수 내 난분해성 물질을 효과적으로 처리하기에 어려움이 있는 것으로 나타났다.
3.2. 단일 및 이중 산화제 산화 처리비교하수처리장 최종방류수의 잔류 TOC 제거에 있어 US와 산화제의 융합 공정이 US와 산화제 각 단일 산화처리의 제거능보다 효과적인지를 판단하기 위하여 PS 단일 처리, H2O2 단일 처리, PS/H2O2 처리 실험을 하였다. 예비실험에서 진행한 US와의 융합 공정에서 최대 TOC 제거능을 보인 산화제 주입량을 기준으로 최종방류수 250 mL, 100 rpm 조건하에서 Jar-tester를 이용하여 진행하였다. 그 결과 PS 단일 처리는 43.5 mM 조건에서 13.8%, H2O2 단일 처리는 174 mM 조건에서 69.2%, PS/H2O2 처리결과 PS 주입량 변수 시 H2O2 174 mM 및 PS 0.52 mM 조건에서 68.5%, H2O2 주입량 변수 시 PS 2.08 mM 및 H2O2, 350 mM 조건에서 85.3%를 나타냈다. PS/H2O2 처리를 제외한 각 단일 처리에 대한 이론적 제거율 합산 결과 97.4%(14.4+13.8+69.2)로 나타났고 이를 Fig. 4에 나타내었다. 단일 산화처리의 경우 174 mM H2O2가 가장 우수한 TOC 제거 특성을 나타내었고 동일 농도를 기준으로 평가해도 단일 처리시는 H2O2가 유기물의 산화능이 우수한 것으로 나타났다.
3.3. 초음파 결합 다중산화공정3.3.1. 초음파/과산화수소(US/H2O2)다중 산화공정에서 H2O2 주입의 영향을 조사하기 위하여 87~567 mM H2O2 조건에서 실험을 진행하였고 시료의 초기 TOC 농도는 8.2 mg/L이었다. Fig. 5(a)는 동일한 80 kHz 초음파와 접촉시간 60 min 에서 H2O2 주입량을 독립변수로(43.5, 87, 174, 343, 567 mM) TOC 제거능을 나타낸 그래프이다. 실험 결과 H2O2 174 mM 주입 조건에서 87.8%로 가장 우수한 TOC 제거 특성을 보였다. 일정량의 H2O2 주입은 TOC 처리능을 개선시킬 수 있지만 PS와 비교하여 저농도 조건에서 상대적으로 효과가 저조하였고, 174 mM H2O2를 초과하여 주입하는 경우도 TOC 제거량이 감소하였다. 이는 식 (18), (31)과 같이 H2O2가 과량 존재할 시 ∙OH을 소비하여 유기물질의 산화 효과를 저해시킨 것으로 판단된다.34)
∙OH + H2O2 → HO2 + H2O (31)
3.3.2. 초음파/과황산염(US/PS)이번에는 동일한 초음파 조건에서 PS 주입의 영향을 조사하기 위하여 2.08~43.5 mM PS 조건에서 실험을 진행하였고 산화처리 전 초기 TOC 농도는 7.7 mg/L이었다. Fig. 5(b)는 Fig. 5(a)와 동일한 조건에서 PS 주입량만을 독립변수로 하여 (0.52, 2.08, 3.12, 10, 20, 43.5 mM) TOC 제거능을 나타낸 그래프이다. 그 결과 PS 43.5 mM 주입 조건에서 81.9%로 가장 우수한 TOC 제거 특성을 보였다 PS의 경우 US와 융합처리 시 상승효과가 발생하는 것으로 판단된다. H2O2 주입량과 비교하였을 때 저농도에서도 H2O2보다 상대적으로 양호한 TOC 제거 특성을 띠었다. 이는 92 kJ mol-1 퍼옥소결합의 해리 에너지를 갖는 대칭성 구조의 이과황산염(Peroxydisulfate, PDS; S2O82-)은 일과황산염(Peroxymonosulfate, PMS; HSO5-)보다 열 혹은 빛과 같은 에너지에 의해 비교적 쉽게 활성화될 수 있는데, US 열에너지에 의해 PS가 빠르게 활성화되어 생성된 황산라디칼이 유기물질의 산화를 촉진시킨 것으로 판단된다[5,27]. 이때 H2O2와 같은 맥락으로 다음의 식(32)에 따라 과황산칼륨의 적정 주입량보다 높은 농도로 주입하면 과황산이온이 황산 라디칼의 scavenger로 작용하여 더 이상 효과가 미미하거나 역효과를 낼 수 있으므로 최적 주입량을 확인하는 것이 바람직하다[18].
S2O82− + SO4−∙ → SO42− + S2O8 −∙ (32)
3.3.3. 초음파/과황산염/과산화수소(US/PS/H2O2)일정한 2.08 mM PS 주입하에 H2O2 주입의 영향을 조사하기 위하여 50~350 mM 조건에서 산화실험을 진행하였고 처리 전 초기 TOC 농도는 9.5 mg/L이었다. Fig. 5(c)는 Fig. 5(a)의 동일한 방류수, 초음파 및 접촉시간 하에 PS 2.08 mM 조건에서 H2O2 주입량을 변수로 하여(50, 100, 150, 200, 250, 300, 350 mM) TOC 제거능을 나타낸 그래프이다. 그 결과 H2O2 주입량이 증가할수록 TOC 제거율이 증가하는 경향을 보였고 H2O2 350 mM 주입 조건에서 87.0%로 가장 우수한 TOC 제거 특성을 보였다. US/PS/H2O2 다중 처리가 US/PS 다중 처리보다는 더 높은 TOC 제거능을 나타냈지만 높은 농도의 H2O2 주입을 필요로 하며 최종 TOC 제거능은 US/H2O2와 유사한 처리 효율을 나타냈다. Fig. 5(c)와 Fig. 5(a)를 함께 비교하였을 때 PS 주입량이 US/H2O2 산화반응에 영향을 주는 것으로 보인다.
일정한 174 mM H2O2 주입하에 PS 주입의 영향을 조사하기 위하여 0.52~6.24 mM 조건에서 산화실험을 진행하였고 처리 전 초기 TOC 농도는 10.4 mg/L이었다. Fig. 5(d)는 Fig. 5(a)의 동일한 방류수, 초음파 및 접촉시간 하에 H2O2 174 mM 조건에서 PS 주입량을 변수로 하여(0.52, 2.08, 4.16, 6.24 mM) TOC 제거능을 나타낸 그래프이다. 그 결과 PS 0.52 mM 주입 조건에서 91.1%로 가장 우수한 TOC 제거 특성을 보였다. 일정량의 PS 주입은 추가적인 유기물질 산화에 효과적이었지만 과량의 PS 농도는 US/PS/H2O2 다중 처리에서 scavenger로 작용하여 TOC 제거능을 저하시키는 것으로 나타났다. Fig. 6에는 융합 AOPs의 최대 TOC 제거율을 막대그래프로 비교하여 나타내었다.
3.4. AOPs 공정의 상호작용
Table 2에 단일, 이중 및 다중 AOPs의 최대 TOC 제거율과 산화 조건을 표로 정리하여 나타내었다. US/H2O2 이중 처리는 80 kHz, 174 mM H2O2 조건에서 87.8%를 나타내 US 단일 처리(14.4%)와 H2O2 단일 처리(69.2%)의 합(14.4%+69.2%) 보다 4.2% 높았다. US/PS 이중 처리는 80 kHz, 43.5 mM PS 조건에서 81.9%를 나타내 US 단일 처리(14.4%)와 PS 단일 처리(13.8%)의 합(14.4%+13.8%)보다 53.7% 높게 나와 multi-AOPs의 상승효과를 나타내었다. US/PS/H2O2 다중 처리는 80 kHz, 0.52 mM PS, 174 mM H2O2 조건에서 91.1%를 나타내 US 단일 처리(14.4%)와 PS/H2O2 이중처리(68.5%)의 합(14.4%+68.5%)보다 8.2% 높았으며, 80 kHz, 2.08 mM PS, 350 mM H2O2 조건에서는 87.0%를 나타내 US 단일 처리(14.4%)와 PS/H2O2 처리(85.3%)의 합(14.4% +85.3%)보다 12.7% 낮았지만 총괄적으로 다중 AOPs 처리는 단일 산화처리의 합보다 처리효율이 높은 상승효과를 나타냈고 다중 AOPs에서 AOP들의 상호작용은 화학적 산화제의 종류에 따라 효과가 다를 수 있어 상호작용에 대한 해석을 보다 다양한 실험을 통한 후속 연구가 필요하다. 본 실험에서 US와 화학적 산화제를 조합함으로써 하수처리수 내 잔류 TOC 제거에 가장 큰 TOC 제거 효율을 나타내는 AOPs는 US/PS/ H2O2가 91.1%로 최고의 결과를 나타냈고, US와의 다중산화처리공정에서 TOC 제거능에 가장 큰 상승효과와 높은 민감도를 나타내는 화학적 산화제는 PS로 나타났다.
4. 결 론1) 40~720 kHz 범위의 주파수에 대하여 US 단일 처리한 결과 80 kHz에서 14.4%로 최대 TOC 제거능을 보였고 사용된 주파수 범위에서 고주파수보다는 저주파수가 TOC 처리능이 우수한 것으로 나타났다. 80 kHz 조건에서 반응시간을 변수로 하여 US 단일 처리한 결과 60 min에서 13.4%로 최대 TOC 제거능을 나타내었고 이를 초과한 초음파 조사시간은 TOC 처리능에 저해를 주었다.
2) 초음파 단일 산화처리한 결과 80 kHz, 60 min 조건에서 14.4%의 TOC 제거율을 나타냈고 H2O2와 PS로 단일 처리한 결과 H2O2 단일 처리는 174 mM 조건에서 69.2%, PS 단일 처리는 43.5 mM 조건에서 13.8%를 나타냈으며, 두 가지 산화제를 융합한 PS/H2O2 처리는 174 mM H2O2 및 0.52 mM PS 조건에서 68.5%, 2.08 mM PS 및 350 mM H2O2 조건에서 85.3%를 나타냈다.
3) US와 화학적 산화제 융합 시 US/H2O2는 174 mM 조건에서 87.8%, US/PS는 43.5 mM 조건에서 81.9%로 증가하였다. 또한 US와 PS 및 H2O2와의 다중 처리 시 2.08 mM PS 및 350 mM H2O2 조건에서 87.0%, 각각 174 mM 및 0.52 mM 조건에서 91.1%의 제거율을 나타냈다.
4) PS는 US와의 융합 처리한 US/PS는 각각 단일 처리의 합보다 큰 상승효과를 내었으며, US/H2O2와 US/PS/H2O2는 산화제 단일 처리와 비교 시 TOC 제거율이 소폭 상승하였는 데 이는 융합처리 시 사용한 H2O2가 유기물질의 산화능이 우수하여 총 제거율의 변화가 상대적으로 작게 나타났기 때문으로 판단된다.
5) PS의 경우에는 US와 융합 시 TOC 제거능이 크게 증가하는 상승효과를 나타냈으며 이때 US와 융합 시 처리수의 pH가 주입 농도에 따라 강하될 수 있어 PS를 이용한 AOPs에서 고려해야 할 사항이다. US/PS와 US/H2O2에서 산화제의 주입 농도를 43.5 mM로 동일하게 적용하였을 때 US/PS는 TOC 제거율 81.9%, US/H2O2는 22.8%를 나타내어 US와 융합한 이중 처리 시 동일 농도에 대한 TOC 제거능은 PS가 H2O2보다 더 우수한 것으로 나타났다.
6) US/PS/H2O2는 본 실험에서 가장 우수한 TOC 제거능을 나타냈지만 효과적인 다중 AOPs를 선택할 때는 개별 산화 처리들의 상호작용이 중요하고 US의 융합 여부, 화학적 산화제의 종류 및 처리수의 pH 등을 고려하여 공정을 선정해야 한다.
7) 부영양화 원인물질이며 공공하수처리시설 방류수 수질 기준 항목인 T-N, T-P는 하수처리수를 하천유지용수로 사용 시 TOC와 더불어 추가적으로 제거가 필요한 인자이며 T-N은 향후 방류수질기준이 강화될 수 있다. 본 연구는 PS, H2O2 및 US의 융합처리 공정에 대한 평가이지만 향후 nano ZVI나 펜톤과 같은 AOPs가 추가되는 경우 Heterogeneous catalysis 반응 효과에 의해 T-P나 T-N의 제거 효과를 추가적으로 기대할 수 있다.
NotesDeclaration of Competing Interest The authors declare that they have no known competing interests or personal relationships that could have appeared to influence the work reported in this paper. Fig. 4.US, PS, H2O2, alone treatment and PS/H2O2 treatment and sum of US+PS+H2O2 TOC removal(%) (US : 80 kHz, PS : 43.5 mM, H2O2 : 174 mM). 
Fig. 5.Comparison of multiple AOPs at sewage treatment effluent(Frequency 80 kHz, exposure time 60 min). 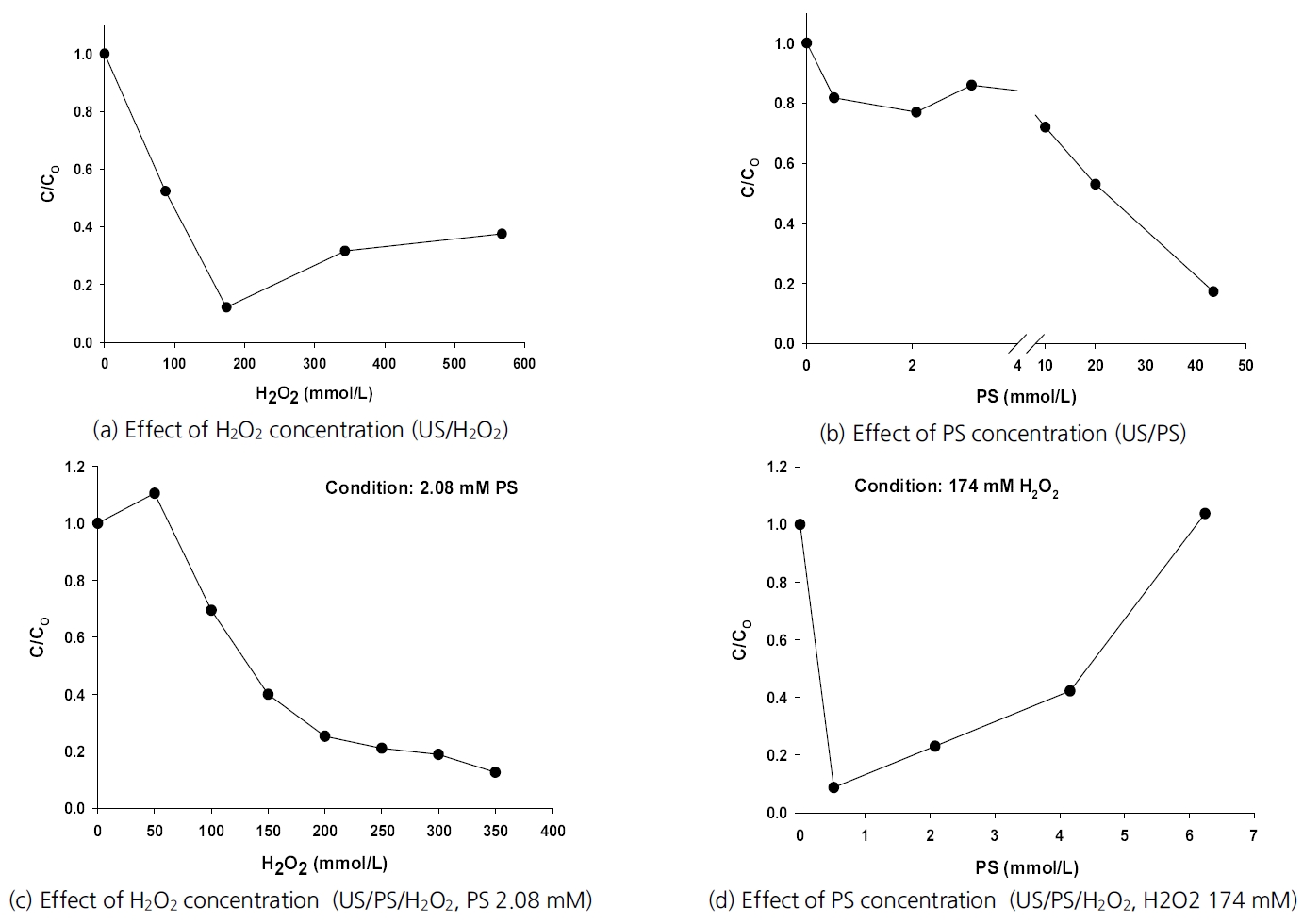
Table 1.Effluent water quality of treated sewage during experiment periods. Table 2.Comparison of maximum TOC removal according to AOPs. References1. E. H. Chung, J. T. Jung, S. Y. Han, A Study on the Application of Advanced Oxidation Process(AOP) for the Tertiary Treatment of Municipal Wastewater, KSWST J. Wat. Treat., 29(5), 39-45(2021).
3. Y. M. Par k, C. H. Par k, Evaluation of P r essur ed UF Membr ane in UF/RO P r ocess for Wastewater Reuse, J. Kor ean Soc. Ur ban. Environ., 19(2), 65-75(2019).
5. M. S. Kim, H. I. Kim, J. D. Shin, J. H. Lim, Oxidant-based advanced oxidation processes (AOPs) for the treatment and reuse of water, Korean Society on Water Environment Water 4 Future City., 7, 1-16(2022).
6. J. O. Tijani, O. O. Fatoba, G. Madzivire, L. F. Petrik, Air, & Soil Pollution., 225, 1-30(2014).
7. B. Langlais, D. Reckhow, D. Brink, Ozone in Water Treatment: Application and Engineering, Lewis Publishers., (1991).
8. H. Lim, K. C. Namkung, J. Yoon, Theoretical understanding of Fenton chemistry, J. Ind. Eng. Chem., 16(1), 9-14(2005).
9. M. Brienza, I. A. Katsoyiannis, Sulfate radical technologies as tertiary treatment for the removal of emerging contaminants from wastewater, Sustainability., 9(9), 1604(2017).
10. N. Pokhrel, P. K. Vabbina, N. Pala, Sonochemistry: science and engineering, Ultrasonics sonochemistry., 29, 104-128(2016).
11. Y. Segura, F. Martínez, J. A. Melero, R. Molina, R. Chand, D. H. Bremner, Enhancement of the advanced Fenton process (Fe0/H2O2) by ultrasound for the mineralization of phenol, Applied Catalysis B: Environmental., 113, 100-106(2012).
12. J. R. Sohn, S. Y. Mo, Characteristics of TCE, Benzene & 2, 4 Dichlorophenol Degradation in Aqueous solution by Ultrasonic Irraditation, Korean J. Sanitation., 11(2), 33-41(1996).
13. X. Wang, J. Wang, P. Guo, W. Guo, C. Wang, Degradation of rhodamine B in aqueous solution by using swirling jet-induced cavitation combined with H2O2, Journal of Hazardous Materials., 169(1-3), 486-491(2009).
14. A. M. Lastre-Acosta, G. Cruz-González, L. Nuevas-Paz, U. J. Jáuregui-Haza, A. C. S. C. Teixeira, Ultrasonic degradation of sulfadiazine in aqueous solutions, Environmental Science and Pollution Research., 22, 918-925(2015).
15. M. Siddique, R. Khan, A. F. Khan, R. Farooq, Improved Photocatalytic Activity of TiO2 Coupling Ultrasound for Reactive Blue 19 Degradation, Journal of the Chemical Society of Pakistan., 36(1), 37-43(2014).
16. H. Zhang, Y. Zhang, T. Qiao, S. Hu, J. Liu, R. Zhu, K. Yang, S. Li, L. Zhang, Study on ultrasonic enhanced ozone oxidation of cyanide-containing wastewater, Separation and Purification Technology., 303, 122258(2022).
17. J. S. Joo, S. M. Lee, H. J. Kim, I. T. Shim, H. J. Kim, Spent-GAC regeneration using variable frequency sono-fenton oxidation, J. Korean Soc. Urban. Environ., 43(4), 449-458(2023).
18. Y. H. Lee, S. J. Lee, M. C. Cui, J. G. Kim, J. J. Ma, Z.C. Han, J. H. Khim, Improving sono-activated persulfate oxidation using mechanical mixing in a 35-kHz ultrasonic reactor: Persulfate activation mechanism and its application, Ultrasonics Sonochemistry., 72, 105412(2021).
19. S. J. Kim, M. J. Jin, Y. T. Jeon, T. S. Jeong, Y. K. Park, C. H. Won, The Study of Ultra-filtration and AOP Processes for Reuse of Nonbiodegrable Industrial Wastewater, J. Korean. Soc. Environ. Tech., 13(1), 1-8(2012).
20. E. H. Chung, J. T. Jung, S. Y. Han, A Study on t he A pplication of Advanced Oxidation Process(AOP) for the Tertiary Treatment of Municipal Wastewater, J. Wat. Treat., 29(5), 39-45(2021).
21. M. Pourgholi, R. M. Jahandizi, M. Miranzadeh, O. H. Beigi, S. Dehghan, Removal of Dye and COD from Textile Wastewater Using AOP(UV/O3, UV/H2O2, O3/H2O2 and UV/H2O2/O3), O3/H2O2 and UV/H2O2/O3)., J. Environ. Health and Sustainable Development, 621-629(2018).
22. S. Y. Mo, H. K. Chang, K. J. Lee, G. E. Jang, J. R. Sohn, Measurement of the quantity hydrogen peroxide produced in ultrasound-irradiated aqueous solution of organic compounds, Korean J. Environ. Eng., 22(1), 61-71(1999).
23. D. Y. Lee, Y. G. Son, Sonochemical and sonophysical effects in heterogeneous systems, J. Korean Soc. Water Environ., 35(2), 115-122(2019).
24. M. Mohajerani, M. Mehrvar, F. Ein-Mozaffari, F. Ein-Mozaffari, Recent achievements in combination of ultrasonolysis and other advanced oxidation processes for wastewater treatment., International Journal of Chemical Reactor Engineering, 8(1).
25. Y. G. Adewuyi, Sonochemistry: environmental science and engineering applications, Industrial & Engineering Chemistry Research., 40(22), 4681-4715(2001).
26. R. Bendjelloul, A. Bensmaili, M. Berkani, T. M. Aminabhavi, Y. Vasseghian, D. Appasamy, Y. Kadmi, Efficient H2O2-sonochemical treatment of Penicillin G in water: Optimization, modeling, DI-HRMS ultra-trace by-products analysis, and degradation pathways, Process Safety and Environmental Protection., 2024.
27. H. Zhang, H. W. Kwon, J. H. Choi, Y. H. Kim, Oxidation of Chloroethenes by Heat-Activated Persulfate, J. Environ. Sci. Int., 26(11), 1201-1208(2017).
28. B. G. Jun, Study of persulfate activation by ultrasonic cavitation phenomenon: effects of frequency and temperature, Domestic Master's Thesis Kumho National University of Technology Graduate School., 2023.
29. R. L. Johnson, P. G. Tratnyek, R. O. B. Johnson, Persulfatepersistence under thermal activation conditions, Environmental science & technology., 42(24), 9350-9356(2008).
30. C. Tan, N. Gao, Y. Deng, N. An, J. Deng, Heat-activated persulfate oxidation of diuron in water, Chemical Eng. J., 203, 294-300(2012).
31. W. S. Chen, Y. C. Su, Removal of dinitrotoluenes in wastewater by sono-activated persulfate, Ultrasonics sonochemistry., 19(4), 921-927(2012).
32. S. Wang, N. Zhou, Removal of carbamazepine from aqueous solution using sono-activated persulfate process, Ultrasonics Sonochemistry., 29, 156-162(2016).
33. Y. G. Son, The Analysis of Acoustic Emission Spectra in a 36 kHz Sonoreactor, J. Soil Groundw. Environ., 21(6), 128-134(2016).
34. D. Y. Ha, S. H. Cho, Y. S. Choi, G. S. Kyung, D. H. Kim, Degradation Characteristics of Oxalic Acid and Citric Acid by UV/H2O2 Oxidation, J. Korean. Soc. Environ. Eng., 22(7), 1307-1318(2000).
|
|
|||||||||||||||||||||||||||||||||||