|
The Korean text of this paper can be translated into multiple languages on the website of http://jksee.or.kr through Google Translator.
AbstractIn this study, a lab-scale sequencing batch reactor of effective volume 3.5 L was used to evalute the performance of mircopollutants removal by 2 Stage PAC-AGS process. It consisted of raw water tank, 1st AGS reactor, 2nd PAC-AGS reactor, reservoir, effluent tank. AGS has superior precipitation of SVI30 58 mL/g and high EPS concentration. For combination AGS with PAC, PAC was evenly distributed by attaching to AGS surface. The result of operating, BOD, TOC, SS, T-N, T-P of 2nd PAC-AGS effluent was 1.2 mg/L, 6.0 mg/L, 1.9 mg/L, 15.5 mg/L, 0.13 mg/L. SUVA of influent, 1st AGS effluent, 2nd PAC-AGS effluent was 0.97 L/mg/m-1, 1.30 L/mg/m-1, 2.03 L/mg/m-1 respectively. It means that hydrophilic and small-molecule compounds was mainly removed of DOC. The 14 species of micropollutants was detected in influent from A STP. Micopollutants concentration of influent, effluent of bioreactor from A STP was 68,016.3 ng/L, 710.4 ng/L respectively and the micopollutants concentration of effluent from 2 Stage PAC-AGS process was 18.1 ng/L. It shows that 2 Stage PAC-AGS process has superior performance for micropollutants removal than bioreactor from A STP in operation. Specially, Diclofenac acid, Carbamazepine were known for high RQ(Risk Quotient) was not detected in effluent from 2 Stage PAC-AGS process.
요약본 연구에서는 2 Stage PAC-AGS 공정을 이용한 미량오염물질의 처리 성능을 평가하고자 하였다. 2 Stage PAC-AGS 공정은 원수조, 1st AGS, 저류조, 2nd PAC-AGS, 방류수조로 구성되며 유효용량 3.5 L 원통형의 두 반응조는 연속 회분식으로 운전되었다. 실험에 사용된 AGS는 SVI30 58 mL/g으로 침강성이 우수하며 EPS 농도가 높게 나타났고 AGS와 PAC 간의 물리적 결합을 유도하여 AGS 표면에 PAC가 고르게 부착되어 분포하는 것으로 나타났다. 2 Stage PAC-AGS 공정 운전결과, 2nd PAC-AGS 유출수의 BOD, TOC, SS, T-N, T-P 농도는 각각 1.2 mg/L, 6.0 mg/L, 1.9 mg/L, 15.5 mg/L, 0.13 mg/L 이었고 SUVA는 유입수 0.97 L/mg/m-1, 1st AGS 유출수 1.30 L/mg/m-1, 2nd PAC-AGS 유출수 2.03 L/mg/m-1으로 증가하며 DOC 중 친수성의 저분자 물질이 주로 제거되는 것으로 나타났다. A하수처리장 유입 하수에서 총 14종의 미량오염물질이 검출되었으며, 미량오염물질 총 농도는 A하수처리장의 유입수 및 유출수 각각 68,016.3 ng/L, 710.4 ng/L로 나타났고, 2 Stage PAC-AGS 공정 유출수는 18.1 ng/L으로 나타나 현재 운영중인 A하수처리장 생물반응조 보다 미량오염물질 제거성능이 우수한 것으로 확인되었다. 특히, 위해성이 높은 물질로 알려진 Diclofenac acid, Carbamazepine은 2 Stage PAC-AGS 공정에서 제거율이 매우 높은 것으로 나타났다.
1. 서 론산업의 고도화 및 생활환경의 변화에 따라 의료업, 산업, 농업 등 여러 분야에서 매우 다앙한 종류의 오염물질이 배출되고 있으며 분석기술의 발달로 기존에 검출되지 않았던 수계에 존재하는 미량오염물질의 확인이 가능해졌다. 이러한 미량오염물질은 난분해성, 독성 등의 특성을 가진 경우가 많고 특히, 항생제, 진통제 등 대부분의 의약물질은 신진대사에 완전히 활용되지 못하고 배출되며 생분해도가 낮아 하수처리장에서 제거가 어렵고[1] 하천이나 강으로 유입되어 아주 적은 농도로 생태계 및 인체에 영향을 미출 수 있다.
최근까지 국내 하수처리 공법은 A2O공정, 막여과 공정을 이용한 고도처리기반의 기술개발이 중점적으로 추진되었으며 활성슬러지를 이용한 생물학적 처리와 응집, 여과의 물리적 처리는 미량오염물질을 제거하기 어렵고 흡착, 광분해, 열분해, 오존 산화 등의 기술이 연구되었으나 경제성 측면에서 효과적이지 못하다.
흡착기술은 다공성 물질을 활용하여 수중 미량오염물질을 제거하는 방법으로 미량오염물질을 효과적으로 처리할 수 있는 것으로 알려져 있으며 대표적인 흡착제는 활성탄, 제올라이트, 점토, 탄소튜브 등이 있고 흡착제의 종류에 따라 제거성능이 달라지는 특성이 있다[2].
활성슬러지를 활용한 SBR(Sequencing Batch Reactor)은 하수 고도처리 방법 중 하나로 일반적인 SBR공정과 비교했을 때, 호기성 그래뉼 슬러지(Aerobic Granular Sludge, AGS) 적용 기술은 고효율 생물흡착, 높은 미생물농도, 빠른 침전속도와 같은 장점이 있으며[3] AGS는 수처리 과정에서 미생물의 서로 다른 역할 수행으로 유기물, 질소, 인을 동시에 제거 가능하다[4].
활성탄은 다량의 미세공극이 형성되어 높은 흡착성으로 용존성 유기물질 제거에 효과적인 것으로 알려져 있다[5]. 생물활성탄(Biological Activated Carbon, BAC)은 활성탄 표면에 미생물이 성장하여 생물막을 형성함으로써 유기물의 생분해와 흡착이 가능하며 2가 양이온, 분말활성탄, Ceramsite와 같은 무기물질을 핵으로 사용하면 미생물의 응집을 촉진하고 과립 강도를 높여 안정성 향상에 도움이 되는 것으로 보고되었다[6].
이전 연구에서 AGS는 높은 유기물 농도 및 독성물질을 함유한 수처리에 매우 유망하다는 것을 보여주었고[7] 구조적 안정성이 높은 AGS와 분말활성탄(Powder Activated Carbon, PAC)의 결합을 통해 PAC-AGS를 형성하여 흡착성능을 향상시킴으로 오염물질을 효과적으로 제거할 수 있을 것으로 판단된다.
미량오염물질 처리에 관한 연구가 대부분 오존, 염소 소독, 활성탄 등을 활용하였으나 오존에 의한 산화 부산물 및 소독 부산물 생성, 폐활성탄의 분리와 폐기에 대한 대책이 요구되며 AGS를 이용한 미량오염물질 제거에 관한 연구는 정보가 부족한 실정이다.
따라서, 본 연구에서는 다량의 미생물을 포함한 AGS 생물반응조와 PAC-AGS 생물반응조를 연계처리 함으로써 2 Stage PAC-AGS 하수처리공정의 미량오염물질 제거 성능을 평가하고자 하였다.
2. 연구 방법2.1. 실험장치1st AGS와 2nd PAC-AGS를 연계한 2 Stage PAC-AGS 공정에 사용된 장치는 Fig. 1과 같다. 2 Stage PAC-AGS 공정은 원수조, 1st AGS, 저류조, 2nd PAC-AGS, 방류수조로 구성되며 두 반응조는 연속 회분식 반응조로 부피 3.5 L의 원통형으로 높이 37 cm, 직경 11 cm 이었고 유출수는 반응조의 중간 위치에서 밸브에 의해 외부로 배출되었다.
2.2. 운전조건본 실험에서 유입수는 충청북도 소재 A하수처리장의 1차 침전지에서 발생한 유출수를 이용하였고 운전조건은 Table 1과 같다. 안정화 상태에서 수리학적 체류시간(Hydraulic Retention Time, HRT)은 각각 4 hr, 6 hr 이었고 1st AGS는 회(Cycle)당 120분(유입/무산소 40분, 포기 70분, 침전/유출 10분) 연속 운전하였고, 2nd PAC-AGS는 회(Cycle)당 144분(유입/무산소 85분, 포기 50분, 침전/유출 9분) 연속 운전하였다. 포기공정에서 공기 공급유량은 2.0~4.0 L/min, 용존산소(Dissolved oxygen) 농도는 6.0~8.0 mg/L 이었고, 반응조 pH는 6.8~8.2를 유지하였다.
2.3 분석항목 및 방법공정의 처리성능을 확인하기 위해 TOC(Total Organic Carbon), DOC(Dissolved Organic Carbon), 생물학적 산소요구량(Biochemical Oxygen Demand, BOD), 부유물질(Suspended Solid, SS), 총질소(T-N), 총인(T-P), UV254 농도를 수질오염공정시험법으로 측정하였고 호기성 그래뉼 슬러지의 특성을 평가하기 위해 MLSS(Mixed Liquor Suspended Solid), MLVSS(Mixed Liquor Volatile Suspended Solid), SVI(Sludge Volume Index), 광학현미경(Optical microscope), 주사현미경(SEM) 분석을 수행하였다.
미량오염물질 정량분석을 위해 4종의 충진재(HLB, ENV+, Strate-X-AW, Strate-X-CW)로 구성된 multi-layer 카트리지을 이용한 고상추출법(SPE)으로 시료를 전처리 하였다. 채취된 시료는 glass microfiber filter(GF5, 0.7 μm)로 여과 후 내부표준물질 100 ng/L을 첨가하고 mulity-layer 카트리지에 시료 1L를 주입 후 질소조건 하에서 건조하였다. 건조된 카트리지에서 acidic solution(ethanol/ethyl acetate 1:1, 1.7% formic acid)과 alkaline solution(ethanol/ethyl acetate 1:1, 0.5% ammonium acetate)이 혼합된 추출용매를 이용하여 시료를 용출하였고 용출액은 질소농축기로 농축시켜 cellulose acetate filter(0.45 ㎛)로 여과 후 vial에 옮겨 닮아 HPLC(High Performance Liquid Chromatography, Ultimate 3000) 기기분석 전까지 냉장(4℃) 보관하였다.
3. 결과 및 고찰3.1. 호기성 그래뉼 슬러지(AGS)3.1.1. 호기성 그래뉼 슬러지(AGS) 형태본 실험에서는 충청북도 소재 A하수처리장 생물반응조의 활성슬러지를 이용하여 연속 회분식 반응조에서 AGS를 배양하였고 운전시간에 따른 AGS 형태를 관찰한 결과는 Fig. 2와 같다. Fig. 2에서 보는바와 같이 14일 이후 미세한 입자가 감소하며 floc의 크기가 증가하였고 36일 이후부터 크기 0.2 mm 이상의 그래뉼이 관찰 되었으며 98일 이후 그래뉼이 조밀하고 안정적인 형태를 나타내었다. 반응조 내부의 낮은 산소농도와 이용가능한 기질의 존재는 Filamentous 성장을 유도하며[8] 실하수를 이용한 입상화 과정에서 짧은 체류시간으로 인한 잔류 유기물에 의해 AGS표면에서 Filamentous bacteria의 성장이 관찰되었다.
3.1.2 호기성 그래뉼 슬러지(AGS) 특성AGS는 자가고정화 방식으로 형성된 미생물 군집체로 운전 시간에 따른 MLSS 농도 변화는 Fig. 3과 같다. 운전초기 짧은 침전시간에 의한 강한 선별강도에 의해 MLSS 농도는 1,000 mg/L까지 감소하였으나 이후 침전성이 향상되면서 2,000 mg/L 이상을 안정적으로 유지하였고 미생물 양 증가와 함께 MLSS 농도는 4,800 mg/L까지 상승하였다.
3.1.3. EPS본 실험에서 형성된 AGS와 일반 활성슬러지(AS)의 EPS (Extracellular Polymeric Substance) 농도 분석결과는 Fig. 5와 같다. AGS의 다당류(Polysaccharide, PS)와 단백질(Protein, PN) 농도는 각각 131.8 mg PS/g MLVSS, 4.7 mg PN/g MLVSS으로 PS/PN비는 28.0이었고, 활성슬러지의 PS와 PN 농도는 각각 63.4 mg PS/g MLVSS, 3.4 mg PN/g MLVSS으로 PS/PN비는 18.6으로 나타나 AGS의 PS/PN비는 활성슬러지에 비해 약 1.5배 높았으며 PS 증가 폭이 더 큰 것으로 확인되었다. PN은 그래뉼 전체에 분포하며 표면전하를 감소시켜 미생물 집합체 형성을 촉진시키고 PS는 주로 그래뉼의 외층에 존재하며 높은 점도로 미생물 간의 상호작용을 유지하며 그래뉼의 안정성을 유지하는데 중요한 역할을 하는 것으로 보고되었다[10].
3.2. PAC-AGS본 실험에서는 AGS와 PAC의 물리적 결합으로 PAC-AGS 입상화를 유도하였고 PAC와 미생물 간의 상호작용을 통해 흡착평형에 이르는 파과시간을 증가시키고자 하였다. 사용된 PAC는 석탄을 기본으로 한 것으로 직경 50~250 μm, 밀도 1.06 g/cm3이었고 500 mg/L 농도로 주입되어 연속 회분식 반응조에서 AGS와 결합시켰다.
PAC-AGS의 광학현미경과 SEM 분석 결과는 Fig. 7과 같다. Fig. 7의 (a)는 PAC와 결합하지 않은 AGS의 광학현미경 이미지이고 (b)는 AGS와 PAC가 결합된 PAC-AGS의 광학현미경 이미지로 AGS 표면에 PAC가 표면에 고르게 분포된 것을 알 수 있으며 (c)는 PAC-AGS의 SEM 분석결과로 슬러지 표면에 결합된 PAC를 관찰 할 수 있다.
AGS는 유체역학적 전단력과 EPS에 의해 형성된 생물막(Bio-film)의 구조와 기능에 영향을 받으며 미생물의 부착과 탈착이 지속적으로 발생한다고 알려져 있으며[11] 이러한 과정에서 PAC가 AGS표면에 부착되어 고르게 분포된 것으로 판단된다.
3.3 2. Stage PAC-AGS 공정3.3.1. 유기물 및 영양염류국가공인시험기관에서 2회 수질분석을 실시하였고 유입수, 1st AGS 유출수, 2nd PAC-AGS 유출수의 BOD, TOC, SS, T-N, T-P 농도는 Table 2와 같다. 1회 분석 결과, 2nd PAC-AGS 유출수는 총인 제거를 위한 약품주입 없이 T-P 농도는 2.07 mg/L을 보였고, 유입수의 비교적 낮은 질소 농도와 1st AGS에서 동시 질산화・탈질에 의해 T-N 농도는 3.9 mg/L으로 매우 낮게 나타난 것으로 판단된다. AGS는 산소 농도 구배에 의해 호기조건에서도 저장된 기질이 무산소 영역에서 소비되고 탈질반응이 활성화 된다고 보고되었다[12].
2회 분석 결과, 2nd PAC-AGS 유출수는 총인 제거를 위한 약품 처리를 실시하였고 모든 항목에서 공공하수처리시설의 Ⅰ지역 방류수질 기준을 안정적으로 만족하는 것으로 나타났다.
3.3.2. TOC, DOC, SUVA유입수, 1st AGS 유출수, 2nd PAC-AGS 유출수의 TOC, DOC, UV254, SUVA(Specific UV Absorbance)는 Table 3과 같다. DOC/TOC(%)는 유입수 53.3%, 1st AGS 유출수 92.9%, 2nd PAC-AGS 유출수 94.9%으로 2nd PAC-AGS 유출수의 TOC 중 대부분은 DOC로 나타났고 UV254 분석 결과, 유입수 대비 1st AGS 유출수에서 크게 감소하는 것으로 보아 AGS에 의해 소수성의 Humic substances가 주로 제거되는 것으로 판단된다.
공정에 따른 DOC 농도와 SUVA 변화는 Fig. 8과 같다. SUVA는 유입수 0.97 L/mg/m-1, 1st AGS 유출수 1.30 L/mg/m-1, 2nd PAC-AGS 유출수 2.03 L/mg/m-1으로 공정을 거치면서 증가하는 경향을 나타냈고 특히, 2nd PAC-AGS 유출수에서 SUVA가 크게 증가하는 것으로 보아PAC-AGS에 의해 친수성의 저분자 물질이 주로 제거 되는 것으로 판단된다. SUVA 4~5 L/mg/m-1 에서 유기물은 비교적 소수성의 Humic substances으로 구성되며, SUVA 3 L/mg/m-1 이하에서 유기물은 친수성이며 저분자 물질로 구성된다고 보고되었다[13].
3.4. 미량오염물질본 실험에서 사용된 유입수는 충청북도 소재 A하수처리장의 생물반응조 유입 관로에서 채수한 것으로 A하수처리장 생물반응조의 유입수 및 유출수, 1st AGS 유출수, 2nd PAC-AGS 유출수의 미량오염물질 농도는 Table 4와 같다.
총 14종의 미량오염물질이 유입수에서 11종, A하수처리장 생물반응조 유출수 및 1st AGS 유출수에서 3종이 추가로 검출되었으며 이는 유입수에서 다른 물질과 결합한 상태로 존재하던 미량오염물질이 포기조에서 단일 형태로 분해되어 유입수에서 검출되지 않았던 물질이 유출수에서 검출되거나 또는 농도가 증가하는 것으로 판단된다. 미생물은 농약 및 의약물질을 분해하는 과정에서 변환물질(Transformation porducts, TPs) 및 대사체(Metabolites)를 생성하며 독성을 저감시키는 것으로 알려져있다[14].
A하수처리장의 생물반응조 유출수와 1st AGS 유출수에서 검출된 미량오염물질 종류 및 농도는 유사하게 나타났으며 2nd PAC-AGS 유출수에서는 Metoxuron을 제외한 모든 미량오염물질이 제거되었다. 이러한 결과는 1st AGS에서 흡착제에 친화력이 높은 물질이 대부분 생물분해 및 흡착에 의해 제거되고 2nd PAC-AGS에서 낮은 친화력을 갖는 미량오염물질의 흡착이 효과적으로 발생한 것으로 판단된다. 다성분의 흡착에서 친화력이 높은 물질이 우선적으로 흡착점을 점유하고 이미 흡착되어 있는 낮은 친화력을 갖는 물질을 치환하여 낮은 친화력을 갖는 물질은 주입농도보다 배출농도가 높게 된다고 보고되었다[15].
A하수처리장 생물반응조의 유입수 및 유출수, 1st AGS 유출수, 2nd PAC-AGS 유출수의 미량오염물질 농도 합은 Fig. 9와 같다.
A하수처리장 생물반응조 유입수, 유출수의 미량오염물질 합은 각각 68,016.3 ng/L, 710.4 ng/L 이었고, 1st AGS 유출수, 2nd PAC-AGS 유출수의 미량오염물질 농도 합은 각각 1,170.3 ng/L, 18.1 ng/L으로 2nd PAC-AGS에서 생물분해 및 활성탄 흡착에 의해 대부분의 미량오염물질이 제거되어 A하수처리장 생물반응조 대비 미량오염물질 제거율은 97.5% 개선되었다. 특히, 하수에서 검출빈도(Detection Frequency, DF)가 높고 예측무영향농도(Predicted No Effect Concentration, PNEC) 낮아 위해성이 높은 물질로 알려진 Diclofenac acid, Carbamazepine은 2 Stage PAC-AGS 공정에서 제거효율이 매우 높은 것으로 나타났으며 이러한 결과는 1st AGS에서 PAC에 친화력이 높은 물질이 우선 제거되고 2nd PAC-AGS에서 잔류하는 난분해성 저분자의 미량오염물질이 효과적으로 제거된 것으로 판단된다.
4. 결 론2 Stage PAC-AGS 공정을 이용한 미량오염물질의 처리 성능을 분석한 결과 다음과 같은 결론을 도출하였다.
1) AGS는 고농도 미생물 군집체로 SVI30는 58 mL/g으로 침강성이 매우 우수하며 EPS의 농도가 높고 주성분인 다당류(Polysaccharide)는 미생물 간의 결합을 위한 가교 역할을 한다.
2) AGS와 PAC 간의 물리적 결합을 유도한 결과, EPS에 의해 AGS로부터 미생물의 탈부착이 지속적으로 발생하는 과정에서 PAC가 AGS 표면에 고르게 분포하는 것으로 나타났다.
3) 2 Stage PAC-AGS공정은 1st AGS와 2nd PAC-AGS로 구성되며 HRT는 각각 4시간, 6시간으로 운전하였다. 최종 처리수의 BOD, TOC, SS, T-N, T-P 농도는 각각 1.2 mg/L, TOC 6.0 mg/L, SS 1.9 mg/L, T-N 15.5 mg/L, T-P 0.13 mg/L로 나타났으며, Ⅰ지역 방류수질 기준을 안정적으로 만족하였다.
4) 공정에 따른 TOC, DOC, SUVA 변화를 살펴보면, DOC/TOC(%)는 유입수 53.3%, 1st AGS와 2nd PAC-AGS를 거치면서 각각 92.9%, 94.9%으로 증가하며 TOC의 대부분은 DOC로 나타났고, SUVA는 유입수 0.97 L/mg/m-1, 1st AGS 1.30 L/mg/m-1, 2nd PAC-AGS 2.03 L/mg/m-1으로 증가하며 1st AGS에서 소수성 물질이 제거되고, 2nd PAC-AGS에서 친수성 물질이 주로 제거되는 것으로 나타났다.
5) 충청북도 소재 A하수처리장의 생물반응조 유입수를 채수하여 본 실험의 유입수로 사용하였고 총 14종의 미량오염물질이 검출되었으며 A하수처리장 생물반응조 유입수 및 유출수와 1st AGS 유출수, 2nd PAC-AGS 유출수의 미량오염물질 농도를 측정하였다. 미량오염물질 농도 합은 A하수처리장 생물반응조 유입수, 유출수 각각 68,016.3 ng/L, 710.4 ng/L 이었고, 1st AGS 유출수, 2nd PAC-AGS 유출수는 각각 1,170.3 ng/L, 18.1 ng/L으로 나타났으며 1st AGS에서 PAC에 친화력이 높은 물질이 우선 제거되고 2nd PAC-AGS에서 대부분의 미량오염물질이 제거 가능한 것으로 나타났다.
6) 특히, 하수에서 검출빈도(Detection Frequency, DF)가 높고 예측무영향농도(Predicted No Effect Concentration, PNEC)낮아 위해성이 높은 물질로 알려진 Diclofenac acid, Carbamazepine은 2 Stage PAC-AGS 공정에서 제거 효율이 높은 것으로 나타나 본 공정은 안정적인 하수고도처리 및 고효율 미량오염물질 처리가 가능한 대안이 될 수 있을 것으로 판단된다.
NotesDeclaration of Competing Interest The authors declare that they have no known competing financial interests or personal relationships that could have appeared to influence the work reported in this paper. Fig. 6.Morphology observation of AGS and EPS. (a) AGS, (b) and (c) EPS.
b)Aerobic Granules: Microbial Landscape and Architecture, Stage and Practical Implications, 2014
c)Formation, extracellular Polymeric substances, and structural stability of aerobic granules enhanced by granular activated carbon, 2019

Fig. 9.Total micropollutants concentration Influent, Effluent of sewage plant and 1st AGS, 2nd PAC-AGS. 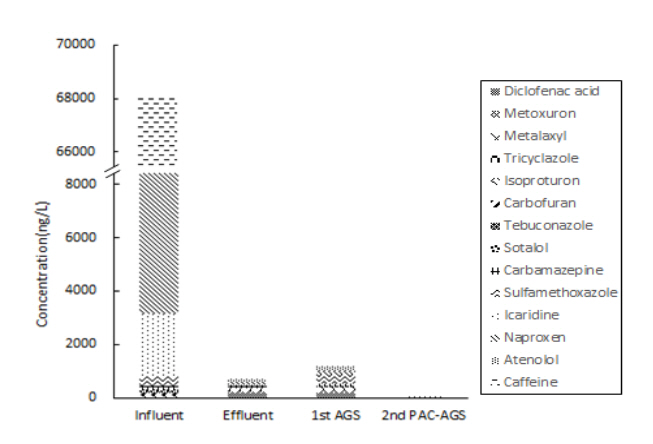
Table 1.Operating condition of 2 Stage PAC-AGS process.
Table 2.Characteristics of influent and effluenta). (unit: mg/L)
Table 3.DOC/TOC, SUVA of influent and effluent.
Table 4.Micropollutants concentration Influent, Effluent of sewage plant and 1st AGS, 2nd PAC-AGS
References1. K. Kummerer, A. Al-Ahmad, V. Mersch-Sundermann, Biodegradability of some antibiotics, elimination of the genotoxicity and affection of wastewater bacteria in a simple test, Chemosphere., 40(7), 701-710(2000).
2. E. J.. Jin, S. C. Lee, E. Y. Kang, Y. J. Kim, W. Y. Choe, Metal-organic frameworks as advanced adsorbent for pharmaceutical and personal care product, Coordination Chem. Rev., 425(15), 213526(2020).
3. S. S. Adav, D. J. Lee, K. Y. Show, J. H. Tay, Aerobic granular sludge: recent advances, Biotechnol. Adv., 26(5), 411-423(2008).
4. M. K. De Kreuk, J. J. Heijnen, M.C.M. van Loosdrecht, Simultaneous COD, nitrogen and phosphate removal by aerobic granular sludge, Biotechnol. Bioeng., 90(6), 761-769(2005).
5. J. Y. Kim, I. H. Yeo, K. S. Hyun, Performance of Biological Granular Activated Carbon/Membrane Filtration System on Micropollutants Removal in Lake Water, J. Kor. Soc. Water Sci. and Technol., 28(6), 63-70(2020).
6. C. L.. Wan, D. J. Lee, X. Yang, Y. Y. Wang, X. Liu, "Calcium precipitate induced aerobic granulation", Bioresour. Technol., 176, 32-37(2015).
7. H. J. Lee, K. S. Kim, Characterization of organic material removal and sludge settling using aerobic granular activated sludge, Kor. Soc. Wat. Environ., 19(6), 699-706(2003).
8. D. Gao, L. Liu, H. Liang, W. M. Wu, Aerobic granular sludge: Characterization, mechanism of granulation and application to wastewater treatment, Crit Rev. Biotechnol., 31(2), 137-152(2011).
9. B. S. Lee, S. W. Choi, Formation and characteristics of granular sludge using aerobic granular reactor, J. Kor. Soc. Environ., 31(12), 1135-1142(2009).
10. Z. Liang, Q. Tu, X. Su, X. Yang, J. Chen, Y. Chen, H. Li, C. Liu, Q. He, Formation, extracellular Polymeric substances, and structural stability of aerobic granules enhanced by granular activated carbon, Environ. Sci. and Pollut. Res., 26(6), 6123-6132(2019).
11. J. H. Tay, Q. S. Liu, Y. Liu, The effect of shear force on the formation, structure and metabolism of aerobic granules, Applied Microbiol. Biotechnol., 57, 227-233(2001).
12. J. J. Beun, E. V. Verhoef, M.C.M. van Loosdrecht, J. J. Heijnen, Stoichiometry and kinetics of poly-β-hydroxybutyrate metabolism under denitrifying conditions in activated sludge cultures, Biotechnol. Bioeng., 68(5), 496-507(2000).
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||