|
The Korean text of this paper can be translated into multiple languages on the website of http://jksee.or.kr through Google Translator.
AbstractMicrobial fuel cell (MFC) technology is receiving a lot of attention recently as a promising technology for generating electricity by treating organic waste resources. Over the past 20 years, the MFC technology has made rapid progress: various research on system architectures, electrochemistry, materials, and microbiology has been conducted for developing practical ideas and fundamental principles. Recently, a lot of research on scaled-up systems for practical application is being conducted in the MFC field. In this review, materials, electrochemistry, system development and scale-up systems of MFCs studied so far are reviewed, and future prospects and directions of MFC technology are presented.
요약미생물 연료 전지(MFC) 기술은 유기성 폐자원을 처리하며 전기를 생산하는 유망한 기술로서 최근 많은 각광을 받고 있다. 지난 20년간 MFC 기술은 급격한 발전을 이뤄왔다. 실용적인 기술 및 근본 원리의 발전을 위한 시스템 구조, 전기화학, 재료, 미생물학 등의 연구가 이뤄져 왔다. MFC의 실용화를 위해 규모를 키운 반응조의 연구도 최근 많이 진행되고 있다. 본 리뷰에서는 지금까지 연구된 MFC의 재료, 전기화학, 시스템 발전 및 스케일업의 성과에 대해 살펴보고 이를 바탕으로 MFC 기술의 향후 전망과 방향을 제시하였다.
1. 서 론현재 인류는 지금까지 경험해 보지 못한 급격한 인구 증가의 시대에 있으며, 이로 인해 안전한 수자원 확보의 많은 물을 소비한다. 2020년 기준 전 세계 인구는 약 78억 명이며, 연간 소비된 물은 약 4.0 × 1012 m3, 물 관련 질병으로 인한 사망자는 약 82.9만 명, 안전하지 않는 식수를 사용하는 사람은 약 20억명이다[1,2]. 전세계 에너지 소비량은 13,508 Mtoe (1.79 × 1016 W, 1.57 × 1014 kWh, 2020년 기준)이다[3]. 인구, 물 소비량, 에너지 소비량 등이 매년 지속적으로 증가하는 현 상황에서, 지속 가능한 지구환경을 위해 현 상황의 돌파구를 열어줄 물-에너지 연계(water-energy nexus) 기술들에 대한 수요는 나날이 증가하고 있다.
미생물의 전기화학 현상을 응용한 미생물 전기화학 기술(microbial electrochemical technology, MET)은 유망한 미래 물-에너지 연계 기술로 각광받고 있다[4,5]. 미생물이 전자를 체외로 방출하여 전기를 발생하는 현상은 1911년 효모와 대장균의 연구를 통해 Potter에 의해 발표됐다[6]. 1931년에 영국 케임브리지 대학교에서는 스택 형태의 전기화학 장치에서 미생물을 촉매로 사용하여 0.2 mA에서 35 V 이상의 전압을 생산했다[7]. 1960년대에 미국 NASA는 장거리 우주 비행에서 유기 폐기물을 전기로 변환하는 데 관심을 보이면서 연료 전지에 대한 아이디어가 대중화됐다. 1962년 Rohrback 그룹에서 Clostridium butyricum을 생체 물질로 사용하여 포도당 발효에 의해 수소를 생산하는 최초의 생물학적 연료 전지를 설계했다[8,9]. 1966년 왕겨를 발효 시 생물학적 연료 전지에 사용할 수 있는 에탄올과 같은 바이오 연료와 유용한 효소를 생성한 것을 확인했고, 이를 통해 6 V에서 40 mA의 전류를 생산했다[9]. 나아가 1999년에 전자를 전극으로 전달하기 위해 매개체를 사용하지 않는 특정 전기화학적 활성 박테리아 종인 Shewanella putrefaciens을 처음 발견했다[10]. 몇 년 후 Geobacter sulfurreducens를 이용하여 전기화학적 작용에 관한 연구가 발표 후에 지구온난화를 일으키지 않는 청정에너지원으로 MFC의 연구가 본격적으로 시작됐다[10-12].
미생물 전기화학 시스템(microbial electrochemical system, MES)에는 여러 기술이 존재한다. 그중 가장 대표적인 기술은 미생물 연료전지(microbial fuel cell, MFC)는 음극(산화전극, anode)에 존재하는 미생물막을 통해 생분해성 기질을 산화하고 전자가 음극으로 외부회로를 통해 양극(환원전극, cathode)으로 이동하여 산소환원 반응을 통해 전류가 생성된다[13].
MFC는 최근 10년간 많은 연구가 진행되고 있다. 구글 학술 검색을 통해 확인한 결과 2010년 약 1,120개의 논문이 발표됐으며, 이후 꾸준히 증가하여 2020년 약 5,090개의 논문이 발표됐다(Fig. 1). 이중 MFC scale-up의 연구는 연구가 활발히 진행함에 따라 2010년 전체 MFC 논문의 9.5%의 비중을 차지했지만, 2019년 13.9%까지 증가했다.
MFC의 스케일 업은 몇 가지 제한 사항에 따라 손실이 발생한다[8,14-16]. 첫 번째로 반응기의 부피가 증가할 때 성능이 비례적으로 증가하지 않는다. 즉, 스케일 업한 반응기의 실제 성능은 저항, 전달 손실과 같은 여러 전기화학적 손실로 인하여 이론적인 값보다 낮다. 두 번째로, 성능을 향상시키기 위하여 여러 반응기를 연결하면 각 반응기 성능의 평준화와 같은 문제가 발생한다. 이러한 문제는 실험실 규모의 반응기에서는 해결할 수 있지만, 스케일 업을 진행한 반응기에서는 아직 해결되지 않았다. 그리하여 본 문헌은 MFC의 원리, 지금까지 연구된 MFC 스케일 업 성능 비교, 실제 하수처리장에 접목한 사례 및 향후 MFC의 전망에 관하여 논한다.
2. MFC 재료의 최근 동향MFC의 구성요소는 여러 가지가 있으나 그중 가장 중요한 구성요소는 음극(anode, 산화전극), 양극(cathode, 환원전극), 분리막이다. 음극은 미생물의 부착 및 산화반응을 하며, 양극은 음극에서 방출된 전자를 수용하여 환원반응을 한다. 분리막은 음극부(anode chamber)와 양극부(cathode chamber)를 물리적으로 분리시켜 주는 역할을 하며, 분리막의 종류에 따라 양이온이나 음이온을 음극부나 양극부로 이동시키기도 한다. 또한, MFC를 제작할 때 분리막을 사용하면 음극부, 양극부로 구분되고 이를 이실형 반응기(two chamber reactor)라 명칭하며, 분리막을 사용하지 않으면 음극부, 양극부를 구분하지 않고 일실형 반응기(single chamber reactor)라 한다. 이러한 음극, 양극, 분리막은 여러 재료를 사용하여 제작한다. 각 재료에 따라 MFC의 전체적인 성능이 달라지며 이에 관한 연구가 활발하게 진행 중이다. 그리하여 이번 장에서는 MFC의 가장 중요한 구성요소인 음극, 양극, 분리막의 재료의 최근 동향에 대해서 소개한다.
2.1. 음극(Anode, 산화전극)2.1.1. 음극의 전극 반응2.1.2. 재료의 동향MFC의 효율적인 음극의 재료는 강도, 화학적 안정성, 낮은 부식률, 높은 전기 전도성, 높은 표면적, 낮은 저항, 저렴한 가격, 강한 생체 적합성 등의 제한 조건이 있다[5,22-25]. 이러한 모든 특성을 가진 재료를 사용하는 것이 매우 바람직하지만 실제 사용 가능한 재료는 물리 화학적 특성과 미생물 부착 및 전자 전달에 대한 전도도에 따라 다르기 때문에 시스템에 맞게 선택을 해야 한다.
MFC에서 일반적으로 사용하는 음극의 재료는 탄소 종이(carbon paper), 탄소 천(carbon cloth), 활성탄 천(activated carbon cloth), 탄소 펠트(carbon felt), 활성 탄소 섬유 펠트(activated carbon fiber felt), 흑연 펠트(graphite felt), 탄소 섬유 브러쉬(carbon fiber brush) 등과 같이 탄소 계열을 많이 사용하고 있다[25-29]. 이러한 탄소 계열의 물질의 대표적인 특성은 안정적이고 상대적으로 저렴하며 전도성 및 화학적 안정성에 의해 가장 널리 사용하고 있다[30,31]. MFC의 음극의 재료로써 탄소 계열뿐만 아니라 금속 및 금속 산화물 재질도 사용하며, 금속 재질은 탄소 계열보다 높은 전도도, 높은 전위창(potential window) 및 높은 촉매 활성도를 보이지만, 탄소 계열보다 부식되기 쉽다[32,33]. 대표적인 금속 재질의 음극은 스테인리스 스틸(stainless steel), 팔라듐(Pd), 금(Au), 니켈(NiO), 망간(MnO2), 코발트(CoxOy), 티타늄(TiO2), 텅스텐(WO3)과 이 금속들의 합금인 니켈망간산화물(Ni0·1Mn0·9O1.45), 니켈티타늄(NiTi), 니켈텅스텐(NiWO4) 등을 사용한다[34-44]. 이러한 음극의 재료에 대한 특성은 Table 2에 나와 있다.
최근 음극 재료는 에너지 생성과 폐수 처리 문제에서 중요한 중요성을 나타내는 두 가지 범주로 더 세분화된다. 이러한 음극 재료는 천연 바이오매스 기반 탄소 음극재, 복합 음극재, 그래핀계 물질로 구분할 수 있다[45].
첫 번째로 천연 바이오매스 기반 음극재는 천연 폐기물과 지속 가능성에서 가치 있는 바이오에너지를 생산하기 위한 잠재적인 친환경 방법을 제공한다. 식물 폐기물은 탄소 기반 음극에서 가장 자주 사용되는 천연 재료이며, 일반적으로 천연 폐기물 유래 음극재로 알려져 있다. 이러한 식물 기반 탄소는 일반적으로 매우 높은 온도(1050℃)에서 탄화가 이루어지며, 탄화 전반에 걸친 수분 증발은 탄소 물질에서 다공성 구조의 발달로 이어진다[46]. 천연 폐기물을 이용한 사례로 빵 조각을 사용하여 3D 미세 다공성 물질을 음극재로 사용한 연구가 있다. 이 연구에서는 음극재의 표면적은 295.07 m2/g이었으며 이를 통해 3134 mW/m2의 최대 전력 밀도를 생산했다. 이는 carbon cloth를 사용한 음극보다 약 3배 더 높은 결과이다[47].
두 번째로 복합 음극재는 최근 몇 년 동안 상당한 관심을 받았다. 복합 기반 재료는 일반적으로 두 가지 이상의 유형의 재료 또는 기본 재료의 개질 및 개선을 통해 시너지 효과를 얻기 위하여 활용되고 있다. 복합 음극재는 금속/금속 산화물, 전도성 고분자, 탄소계 복합재 등으로 분류된다. 음극에 박테리아 부착량 증가 및 저항 손실 감소는 금속/금속 산화물-탄소 기반 재료 복합 재료에 의해 크게 영향을 받는다[48]. 금속 산화물/탄소 복합 재료는 금속 기반 재료만으로는 부식의 문제와 탄소 기반 재료는 낮은 전도성 때문에 큰 관심을 받았다. 따라서 복합재는 이 두 가지 요소를 해결하고 MFC의 높은 성능을 위한 음극을 제공한다.
마지막으로 그래핀계 음극재는 전도성(7200 S/m), 표면적(2600 m2/g), 생체 적합성 및 박테리아 부착과 같은 현재 많은 문제를 충족하여 가장 유망한 재료로 간주된다[49]. 다른 금속 산화물 또는 전도성 고분자와 결합된 그래핀 기반 복합재는 높은 전자 이동 속도와 높은 전기 촉매 활성으로 인해 MFC 전극의 적용 범위를 넓힐 수 있는 돌파구를 제공한다. 현재의 에너지 공급 및 폐수 처리/오염 물질 제거 위기를 충족하기 위해서 MFC 접근 방식을 적용하기 위해 다른 재료와의 합성을 통해 그래핀 기반 재료를 향상시키는 것을 고려해야 한다. 몇 가지 초기 연구는 그래핀으로 개질한 음극이 신호 분자를 분비하도록 박테리아 종을 자극할 수 있음을 보여주었다. 이는 박테리아 성장을 향상시키고 전자 전달의 효율성을 증가시키는 중간 분자로서 MFC 성능에 영향을 미쳤다[31]. 또한, 그래핀의 넓은 표면적은 기질 산화 및 계면 반응을 위한 더 많은 활성화 부위를 제공하여 저항 및 활성화 손실을 감소시켰다.
음극은 MFC에서 중요한 역할을 하지만 가장 큰 문제점은 음극 재료의 비용이다. 또한, 음극의 적절한 설계와 크기는 박테리아 부착에 필요한 표면적을 제공하는 핵심 요소이다. 따라서 음극 재료의 선택은 높은 MFC 성능을 위한 이상적인 음극을 제작하는 데 중요한 단계이다. 종합적으로 현재 음극의 재료로 가장 많은 연구가 되는 것은 각각의 단점을 최소화하고 장점을 극대화하는 복합재이다. 이러한 음극재의 연구는 Table 3에 나와 있다.
2.2. 양극(Cathode, 환원전극)MFC의 주요 구성 요소 중 하나인 양극은 MFC의 성능을 높이는 데 중요한 역할을 한다. MFC 양극에서 발생하는 주된 반응은 산소환원반응(oxygen reduction reaction, ORR)이다[50]. 이러한 ORR이 일어나는 양극은 전류 수집체(current collector), 촉매층(catalyst layer), 확산층(diffusion layer)로 크게 3개의 층으로 구분할 수 있다. 전류 수집체는 양극에서 발생한 전류를 수집하고, 촉매를 부착시키기 위한 지지체로 사용한다[50-52]. 전류 수집체는 일반적으로 탄소 천을 주로 사용했지만 최근 탄소 천보다 저렴하고 높은 전도성을 가진 금속 계열의 망도 많이 사용하고 있으며, 대표적으로 사용하는 금속 계열의 망은 스테인리스 스틸 망(stainless steel mesh, SSM)이다[50,53]. 촉매층은 ORR반응이 일어나는 지점이며, 확산층은 양극의 산소를 투과하고 방수의 기능을 가진다. 이러한 양극은 일반적으로 바인더(binder)를 이용하여 촉매층과 확산층을 제조한다. 바인더는 일종의 접합제로써 촉매층과 전류 수집체의 결합을 용이하게 한다[54]. 가장 널리 사용된 바인더는 NafionTM이지만 높은 가격 때문에 상대적으로 저렴한 Polytetrafluoroethylen (PTFE), Poly (vinylidene fluoride) (PVDF)와 같은 바인더로 대체하여 사용하기도 한다[55-57].
2.2.1. 양극의 전극 반응대부분 MFC의 반응기 전압은 약 0.6 V, 양극 전위는 0.3 V의 값을 가진다(기질을 acetate 사용) [5]. Table 1을 보면 acidic에서 2전자전달 반응의 전위는 0.260 V이고, 이는 과산화수소를 생산하는데 필요한 모든 에너지를 외부의 추가적인 공급 없이 MFC 자체적으로 생산하여 반응을 할 수 있다[57]. 즉, 대부분의 MFC는 4전자전달 반응보다 과산화수소를 생성하는 2전자전달 반응이 주로 일어나며 추가적인 에너지 공급 없이 과산화수소를 생성할 수 있다[58]. 하지만 2전자전달 반응은 4전자전달보다 느려 4전자전달 반응이 선호된다[49].
2.2.2 재료의 동향이상적인 ORR 촉매의 조건은 i) 높은 촉매 활성, ii) 높은 안정성, iii) 높은 선택성 및 iv) 저렴한 비용이다[59]. 일반적으로 백금(Pt) 기반 촉매는 우수한 전기 촉매 활성으로 인해 MFC 양극 ORR 촉매로 활용되어 왔다[5,60-62]. 그러나 백금 기반 촉매의 높은 비용과 희소성으로 인해 새로운 촉매를 찾는 연구를 많이 진행했다. 그중 Fe, Co, Ni, Mn과 같은 전이 금속이나 활성탄과 같은 탄소 기반 재료와 같은 물질이 높은 다공성, 표면적, 전기 전도성 등 ORR 공정에 적합한 것으로 밝혀졌다[61,63-66]. 그리하여 저렴하고 효율적인 양극을 위해 탄소 계열과 전이 금속을 결합한 효율적인 촉매의 연구를 많이 진행하고 있다[56,57,66]. 현재 대표적인 탄소 계열의 촉매는 흑연(graphite), 카본 블랙(carbon black), 활성탄(activated carbon, AC), 탄소 나노튜브(carbon nanotube, CNT), 그래핀(graphene), 금속-질소-탄소 복합 촉매(metal-nitrogen-carbon complex, M-N-C), 금속-유기 골격 촉매(metal-organic framework, MOF)가 있다.
흑연은 비표면적, 생체 적합성, 화학적 안정성, 전자 전도성, 저렴한 비용 등으로 인해 양극 재료로 많이 사용된다[67,68]. 하지만 처리하지 않은 흑연은 촉매 활성 부위가 적어 성능이 좋지 않다[69]. 표면적을 개선하기 위하여 질산으로 처리한 흑연은 ORR을 향상시킨 연구가 있다[70]. 이 연구에 따르면 질산으로 처리된 흑연의 열 활성화를 보고 했으며, 활성 흑연은 OCP가 40 mV 증가했다. 이는 산소 및 질소와 같은 화학적 기능과 표면적이 증가했기 때문이다. 이후 최근 연구에 따르면 흑연에 CuO와 ZnO을 합성하여 새로운 촉매를 개발했다[71]. 결과는 CuO/ZnO/흑연 촉매는 대조군에 비하여 최대 전력 밀도가 32% 증가했다. 이러한 연구에도 불구하고 흑연은 낮은 반응성과 촉매적 특성으로 인하여 많이 사용되지 않는다.
카본 블랙은 탄화수소의 불완전한 열 산화로 인해 카본 블랙이 형성된다. 카본 블랙 자체는 전기 촉매 특성을 가지고 있지만 금속 기반 촉매보다 낮은 성능을 가졌다. 또한, 카본 블랙은 불활성이며 촉매 활성이 매우 낮다. 카본 블랙의 전기 촉매 특성을 향상시키는 효과적인 방법 중 하나는 표면 활성 작용기를 통해 표면을 화학적으로 작용화 및 기능화하는 것이다. 이 방법은 일반적으로 산을 사용하여 산 처리를 사용한다. 한 연구에서, 폴리아닐린(polyaniline, PANI)과 철-탈로시아닌 (iron-phthalocyanine, FePc)으로 기능화된 카본 블랙(PANI/C/FePc)을 촉매로 개발했다[72]. 여기서 사용한 PANI는 FePc를 위한 지지 금속물로 활용됐으며, 카본 블랙의 PANI 기능화는 FePc의 흡수를 향상시켰다. 결과는 탄소 천에 백금 촉매(Pt/C)를 사용하여 제작한 양극보다 약 10% 더 높은 630.5 mW/m2의 최대 전력 밀도를 보였다. 또한, 최근 카본 블랙의 개질 연구에서 질소가 도핑된 카본 블랙(Vulcan XC-72R)을 산 처리하여 질소 공급원으로 피라진아미드(pyrazinamide)로 기능화했다[73]. XPS의 분석 결과는 graphitic-N, pyridinic-N 및 pyrrolic-N과 같은 다양한 형태의 N-기능기를 보였으며, 143 m2/g의 표면적을 보였다. 이 촉매를 MFC에 접목한 결과 371 mW/m2의 최대 전력 밀도를 나타냈으며, 이는 N-기능기의 차이 때문이다.
활성탄은 표면적과 다공성을 향상시키는 탄소의 열처리로 생성한다. 다양한 기질을 사용할 수 있는 활성탄은 저렴한 가격과 높은 표면적으로 MFC의 양극 촉매로 가장 많이 사용하고 있다. 하지만 활성탄은 낮은 전자 전도성 때문에 단일 촉매로 사용하는 것보다 카본 블랙, 탄소 나노튜브 등과 같은 다른 전도성 탄소나 전이 금속을 혼합하여 사용한다. 활성탄 촉매는 활성탄과 카본 블랙을 결합한 방법을 가장 널리 사용하고 있으며, 이는 0.40 S/cm의 활성탄 전도도 보다 더 높은 0.53 S/cm의 전도도를 보였다[74]. 이 활성탄-카본 블랙 촉매를 MFC에 접목한 결과 Pt/C양극보다 41% 더 높은 1900 mW/m2의 최대 전력 밀도를 보였다. 이 외에도 활성탄에 질소를 도핑하여 개질한 연구가 있다[75]. 이 연구는 활성탄을 코발트와 1,10- 페난트롤린(1,10-phenanthroline)으로 800℃에서 개질하여 제작한 양극(Co-N-C/AC)의 최대 전력 밀도가 1,526 mW/m2으로 백금 환원 전극(Pt)보다 56% 높았다.
MFC에 대한 탄소 나노튜브 기반 양극 촉매에 대한 많은 연구 논문이 있다[48,76,77]. 탄소 나노튜브는 우수한 전자 전도성, 우수한 표면적 특성으로 인한 우수한 내식성을 갖추고 있습니다. 탄소 나노튜브는 활성탄, 흑연, 카본 블랙과 마찬가지로 산 처리를 사용한다. 그 외에 헤테로원자의 도핑 방법도 사용하는데 이 방법은 탄소 나노튜브의 ORR 활성을 향상시키는 효과적인 방법으로 간주되며, Co, Fe, Mn 및 기타 전이 금속의 나노 입자도 탄소 나노튜브 표면에 침착되어 생성된 촉매는 다양한 구성의 MFC에서 우수한 ORR 활성 및 성능을 나타냈다[78-80]. 탄소 나노튜브의 연구 중 탄소 천에 질소 도핑한 탄소 나노튜브를 부착시킨 연구를 보면 최대 전력 밀도가 542 mW/m3으로 Pt/C보다 8.6% 더 높은 성능을 보였으며, 이는 탄소 나노뷰트의 우수한 전도도에 기인하며 질소 도핑에 의해서 성능이 더욱 증진됐다[81].
그래핀을 기반으로 하는 전기촉매는 우수한 전자 전도성, 넓은 표면적, 높은 흑연 특성, 화학적 및 물리적 기능화 용이성으로 인해 큰 주목을 받고 있다[82]. 그러나 다른 탄소 물질과 마찬가지로 처리하지 않은 그래핀은 ORR 활성 기능기가 없기 때문에 전기 촉매 응용 분야에 대해 불활성인 것으로 간주된다. 전기음성도가 다른 다양한 헤테로원자로 그래핀을 화학적으로 도핑하는 것은 그래핀을 우수한 전기촉매로 활용하는 효과적인 방법이다. N, B, S, P 및 F와 같은 다양한 헤테로원자는 그래핀 및 기타 탄소 재료에 대한 가능한 첨가제로 사용된다[21]. 헤테로원자 도핑은 그래핀의 전하 밀도를 변경하여 산소의 잠재적 활성 부위를 생성한다[83]. 도핑된 그래핀은 전자 전도성을 향상시켜 금속 나노입자 활성 부위로의 전자 이동을 가속화하고, 이는 흡착된 산소와의 전자 교환에 긍정적인 영향을 미친다. 다양한 형태의 그래핀은 환원그래핀옥사이드(reduced graphene oxide, rGO), 단층 및 다층 그래핀 시트, 그래핀 나노리본과 같은 ORR 촉매로 활용된다[84-86]. 최근 연구 중 산화 그래핀과 구형 실리콘으로 기능화된 세틸트리메틸 암모늄 브로마이드(cetyltrimethyl ammonium bromide) 사이의 정전기적 상호 작용을 활용한 후 알칼리 에칭을 통해 실리콘을 제거하여 질소 도핑된 그래핀에 Co3O4를 합성했다[87]. 합성된 그래핀은 O2 분자당 3.91개의 전자가 이동하여 알칼리성 매질에서 거의 유사한 ORR 활성으로 우수한 ORR 활성을 나타냈으며, 0.59 V의 OCV, 578 mW/m2의 최대 전력 밀도를 생산했다.
금속-질소-탄소(M-N-C, M= Co, Fe, Mn 등)는 금속-대형 탄소 혼합물의 간단한 열분해(400 - 1000℃)에 의해 생성되어 금속이 질소 원자와 결합하는 활성 촉매를 생성할 수 있다[88]. 최초의 M-N-C 촉매의 ORR 활성은 촉매의 ORR 활성이 57Fe Mössbauer 분광법에 의해 N-도핑된 탄소에 배위결합된 Fe 원자의 수에 직접적으로 의존하는 것으로 관찰됐다[89]. 이후 M-N-C에서 ORR 중간체의 흡착/탈착에서 M-N-C 활성 부위의 메커니즘을 확인했다[90]. 이를 통해 M-N-C 촉매는 우수한 ORR 촉매로 제안됐으며, 최근 MFC 양극에 새로운 종류의 활성 촉매로 떠오르고 있다[91]. 최근 연구에서 Fe-N-C 촉매를 개발했는데, N은 키토산 하이드로겔, C는 활성탄을 이용했다[92]. 실험의 결과는 Fe-N-C 촉매는 630 mV의 OCV를 보였으며, 약 120시간 동안 OCV의 변동이 거의 없어 우수한 안정성을 보였다. 또한 2.4 W/m2의 최대 전력 밀도로 대조군인 활성탄 양극보다 약 33% 더 높은 값이다.
금속-유기 골격 촉매(metal-organic framework, MOF)는 완벽하게 배열된 방식으로 규칙적으로 배열된 금속 이온과 유기 리간드로 구성된다[93]. 금속 전구체는 Fe, Co, Mn, Ni, Zn 등을 사용하며, N, S와 같은 헤테로원자를 포함하는 유기 리간드를 사용한다. 가장 중요한 것은 MOF에서 합성된 촉매는 높은 다공성 구조와 특정 촉매 적용에 대한 조정 가능한 특성을 가지고 있다. 대부분의 MOF는 금속이온인 Zn2+와 리간드로 N을 포함하는 2-methyl imidazole로부터 합성된다. 생성된 MOF는 Zn의 끓는점 이상에서 열분해되고 MOF를 생성한다. 열분해 과정에서 Zn2+는 Zn으로 전환 및 증발하여 불활성 가스에 의해 운반된다. 이후 Zn원자가 0인 촉매를 생성하고 동시에 유기 리간드가 N-도핑된 탄소로 분해 및 탄화된다. 대표적인 MOF로 ZIF-8 (Zeolitic imidazolate framework-8)을 사용하여 MFC에 접목한 연구가 있다[94]. 그 결과 2103 mW/m2의 최대 전력 밀도를 생산했으며, ZIF-8에서 파생된 N-도핑된 탄소는 우수한 흑연화, 전자 전도성을 가져서 90% 이상의 COD 제거율, 110시간 동안 운전하여 우수한 내구성이 평가됐다. 이 외에 ZIF-67을 이용한 연구도 있다[93]. 이 연구는 ZIF-67과 활성탄을 초음파로 결합하여 양극을 제작했다. 결과는 4203 mW/m2의 최대 전력 밀도를 생산했으며, 이는 50 mM PBS, cubic 크기(4 × 3 cm)을 사용한 MFC 기준으로 세계 최고의 성능을 달성했다. 지금까지 MFC 양극 촉매로 가장 많이 사용한 물질은 활성탄이지만 낮은 전도성으로 인해 추가적인 물질과 결합하여 사용하고 있다. 하지만 최근 금속-질소-탄소 촉매나 금속-유기 골격 촉매가 새로운 양극 촉매로 각광받고 있으며, 효율적인 양극의 촉매로 사용하기 위해 많은 연구를 진행하고 있다.
2.3. 막(Membrane)과 세퍼레이터(Separator)MFC에서 물리적 분리기 역할을 하는 분리막은 음극부와 양극부 사이에 설치하며, 음극부에서 양극부로 기질의 확산을 효과적으로 방지한다. 또한, 음극부에서 양극부로 양성자의 수송을 용이하게 하고 양극부의 산소를 음극부로 이동하는 것을 방지하거나 전자의 이동을 차단하여 단락 현상을 방지한다[95,96].
분리막은 크게 2가지로 구분되며, 이온 교환을 용이하게 하는 이온막(membrane)과 전자나 양이온과 같은 물질의 이동을 차단하는 세퍼레이터(separator)가 있다. 세퍼레이터는 음극과 양극의 거리가 가까운 경우 전극의 단락 현상이 발생하기 때문에 음극과 양극 사이에 삽입하여 단락 현상을 방지한다[29,97,98]. 이온막은 일반적으로 양이온과 음이온을 교환할 수 있는 기능기를 포함하는 중합체 막이다. 이 막은 유사한 전하 이온(co-ion)을 차단하면서 일부 반대 전하 이온(counter-ion)의 전달을 선택적으로 허용하여 이온을 이동시킨다[99].
이온막은 다공성, 비다공성 막으로 구분할 수 있다[100]. 다공성 막은 나노여과(nanofiltration, NF), 한외여과(ultrafiltration, UF), 미세여과(microfiltration, MF)으로 구분이 가능하며, 비다공성 막은 양성자 교환막(proton exchange membrane, PEM), 음이온 교환막(anion exchange membrane, AEM), 양성자 교환막(bipolar membrane, BPM), 역삼투압막(reverse or forward osmosis, RO or FO)이 있다[5,100,101]. PEM은 CEM (cation exchange membrane)이라고도 하며 막을 통해 양이온이 양극부로 이동하게 하고, AEM은 PEM과는 다르게 음이온을 양극부에서 음극부로 이동하게 한다[102]. 또한, AEM은 막에서 부착된 인산염 또는 탄산염과 같은 양전하는 양성자 운반체를 적용하여 양성자 이동을 촉진할 수 있다[103]. BPM은 음이온 교환층과 양이온 교환층의 구성으로 습윤접합 계면을 형성하는 막이며, BPM의 이온 전도도는 이온막을 가로지르는 이온 플럭스에 의한 것이 아니라 PEM과 AEM 사이의 전이 영역 또는 표면에서 발생한 물 분해 반응을 통해 발생한다[102,104]. 이러한 이온막은 양성자보다 양이온의 전달 속도가 더 높다. 실제 하폐수에는 양이온이 양성자보다 105배 더 높은 농도로 존재하는데, 양이온의 전달 속도가 더 높으면 이온막과 양이온이 결합하여 양성자의 이동을 억제할 수 있다[105-107]. 양성자의 이동이 억제되면 음극부의 pH가 감소하고 양극부의 pH가 증가함에 따라 MFC의 성능을 저하시킬 수 있다. 그에 따라 부직포와 같은 전도성이 없는 일반적인 막을 사용하기도 한다[108-111]. 부직포와 같은 분리막을 사용하면 분리막의 세척이 용이하고 개질이 편하다는 장점이 있으며, 양이온이 많은 폐수에서도 일정한 성능을 달성할 수 있다[112].
2.3.1 최근 동향이온막은 MFC 시스템의 전체 비용과 성능에 상당한 영향을 미치는 주요 구성 요소 중 하나이다. 하지만 내부 저항이 높은 이온막은 이온 교환 및 양성자 확산 감소로 인해 낮은 성능을 보이기 때문에 이온막은 시스템의 내부 저항에서 중요한 역할을 한다[113]. 그리하여 이온막을 사용할 때 재질에 관계없이 내부 저항, 물질 전달률, 전도도, 에너지 회수율, 이온 전도도, 내구성, 산소 확산 방지와 같은 몇 가지 주요 특징을 충족해야 한다[96,100,114]. 이뿐만 아니라 이온막과 관련된 주요 문제 중 하나는 산소와 기질이 반대 방향으로 크로스오버하는 것이다. 음극부에서 양극부로 기질이 이동하면 음극에 미생물이 성장하여 ORR을 하지 못하게 되며, 양극에서 유기 기질이 산화되어 전력 효율이 감소한다. 따라서 MFC를 효율적으로 운전하기 위해 기질과 산소의 균형을 유지하는 것이 중요하다.
막의 생물학적 요염은 막에서 중요한 문제이다. 이온막 표면에 미생물이 부착되는 것을 이온막의 바이오파울링(biofouling)이라 한다. 바이오파울링이 발생하면 이온막의 전자 전도성이 감소하기 때문에 바이오파울링을 줄이거나 제거하는 것이 중요하다[115,116]. 이러한 바이오파울링을 줄이기 위해 부직포와 같은 전도성이 없는 물질에 미생물을 부착시킨 미생물 분리막(microbial separator)의 연구가 진행 중이다. 미생물 분리막은 일종의 여과막으로서 이온의 이동뿐만 아니라 폐수 및 분자의 이동이 가능하고, 분리막에서 기질의 분해가 일어나 전력을 생산할 수 있다. 또한, 분리막에서 오염물질의 처리가 가능하여 바이오파울링이 일어나지 않아 장시간 운전 시 긍정적인 성능을 보여줄 수 있다[117].
미생물 분리막은 현재 많은 연구가 되지 않아 추가적인 연구가 필요하며, 향후 지속 가능한 분리막은 MFC 스케일업에 중요한 부분으로 자리매김할 것이다. 정리하면 MFC에 적합한 이온막은 우수한 이온 전도, 이온 선택성, 절연, 내구성, 생체 적합성, 화학적 안정성, 오염 등이 우수해야 하며 막힘에 민감하지 않고 비용이 저렴해야 한다[118].
3. MFC 전기화학의 최근 동향일반적으로 MFC의 성능을 평가하기 위해서 가장 많이 사용하는 실험은 선형 강하 전압-전류법(linear sweep voltammetry, LSV), 순환 전압전류법(cyclic voltammetry, CV), 전기화학 임피던스 분광법(electrochemical impedance spectroscopy, EIS)로 크게 3가지가 있다.
LSV는 MFC에서 가장 기본적인 성능 평가로 측정하며 전 세계적으로 가장 많이 사용하는 실험이다. 이 실험은 전압(voltage) 및 전위(potential) 또는 전류를 일정한 속도로 강하하는 실험으로 전압 및 전위를 강하하면 전류를, 전류를 강하하면 전압을 측정한다. 일반적으로 전극의 전위를 강하하는 실험을 LSV, 반응기 전압을 강하하는 실험을 분극 실험(polarization test)라고 명칭 한다[55,93,119,120]. 분극 실험은 LSV의 일부분으로 반응기의 전압을 강하하고 그에 따른 전류를 측정한다. 측정 결과를 이용하여 반응기의 분극 곡선(polarization curve), 최대 전력 밀도(maximum power density), 각 전극의 전위 등을 확인하고 반응기의 성능을 평가한다. 최대 전력 밀도는 반응기에서 사용한 전극의 유효 면적이나 부피를 기반으로 반응기에서 생산하는 전력을 확인할 수 있다. 또한, 전극 전위를 기반으로 각 전극 및 내부 저항을 계산할 수 있으며, 이 방법은 2017년 처음 사용되어 현재 세계적으로 반응기 성능 평가의 지표로 많이 사용하고 있다[29,55,97,121-123].
CV는 전기화학적 거동을 설명하기 위해 수행하는데 다시 말하면 가역적인 전기화학 활성을 기반으로 전자 이동 구성요소를 식별 및 설명하기 위하여 수행한다[125,126]. 이러한 CV는 일정한 범위를 지정한 뒤 전극의 전위를 일정한 속도로 주사하여 그에 따른 전류를 측정하며, 대표적으로 음극과 생물막의 전자 전달 작용, 전극에서의 산화 및 환원반응 전위, 시간 경과에 따른 전극의 성능 평가 등을 정량적으로 비교하는데 사용한다[126,127].
MFC 연구의 핵심 중 하나는 전력 생산을 제한하는 생물학적 및 비생물학적 요인을 조사하는 것이다. 이러한 요소는 내부 저항이나 전극의 임피던스(impedance)로 표현할 수 있다[128]. 내부 저항은 위에서 기술한 것과 같이 분극 실험을 통해서 계산이 가능하며 용액 저항, 전자 전달 저항, 확산 저항 3가지로 구분할 수 있다[93,119,120]. 하지만 분극 실험을 통해 계산하면 저항을 구분할 수 없기 때문에 세밀하고 정밀하게 분석하기 위해 내부 용액 또는 전극의 계면 등에서 전하의 역학을 조사하는 유용한 방법인 EIS를 사용하여 분석한다[129].
쿨롱 효율(CE(S|E), coulombic efficiency, %)은 기질로부터 음극으로 실제 전달된 전체 쿨롱의 비율로 정의된다[5,122]. 즉, COD 제거량으로부터 전환된 전류이다. 그리하여 MFC의 운전 시 시간에 따른 전류 생산량을 적분함으로써 쿨롱 효율을 계산한다. 이를 식으로 표현하면 다음과 같다.
M은 32 (산소의 분자량), F는 패러데이 상수(9.64853 × 104 C/mol), b는 4 (산소 1몰당 교환되는 전자의 수), van는 음극의 체적, △COD (g-COD)는 운전 시 COD의 변화,
만약 MFC를 운전 시 회분식이 아닌 연속흐름식으로 운전하면 식은 다음과 같이 바뀐다.
여기서 q는 유입수의 유속이고, △COD는 유입수와 유출수의 COD의 차이 즉, 분해된 COD의 농도이다[5].
MFC의 성능을 평가하는 가장 중요한 요소는 기준 기술에 비해 에너지 회수 측면에서 평가하는 것이다. 에너지 효율(EE, energy efficiency, %)은 기질의 열소열으로부터 생산한 전력의 비율로 정의되며 식은 다음과 같다.
여기서 ΔH는 기질의 연소열(kJ/mol)이고, n은 기질의 양(mol)이다. 이전 연구를 보면 acetate의 연소열을 계산한 문헌이 있다[130,131]. 이 문헌의 계산값을 보면 -874.3 kJ/mol이며 이 값이 실제 미생물 전기화학 시스템에서 가장 정확한 값이다. 그리하여 acetate를 사용하는 경우 기질의 연소열을 -874.3 kJ/mol을 사용하는 것을 추천한다. 기질의 연소열은 문헌마다 다른 값을 사용하거나 표기를 하지 않는다[97,132-135]. 그리하여 MFC의 정확한 비교 분석을 위해서는 동일한 값의 연소열을 사용하거나 사용한 값을 표기해야 한다. 서로 다른 연소열을 사용한 것을 -874.3 kJ/mol로 치환하여 계산한 결과는 Table 6에 나와 있다. 기질의 양은 MFC에서 소모된 기질의 양을 의미하며 이를 식에 연관시켜서 다시 표현하면 다음과 같다[122].
또한, 에너지 회수(ER, energy recovery, kWh/kg-COD)은 스케일 업을 진행한 MFC를 평가할 때 사용된다. 이 에너지 회수는 제거한 COD당 생산한 전력이며, 계산식은 다음과 같다[136].
여기서 P는 전력(W)이며, Q는 유량(L/h), △COD는 분해된 COD의 농도이다.
MFC를 운전할 때 기준전극을 사용하여 운전하는데 이때 주로 Ag/AgCl 전극을 사용한다. Ag/AgCl 전극은 standard hydrogen electrode (SHE)값으로 변환이 가능하며 관계식은 다음과 같다[137,138].
E는 SHE 값(mV), E(0,Ag/AgCl)는 Ag/AgCl 전극의 표준 전위,
이 식을 기반으로 Ag/AgCl 전극과 SHE의 차이를 계산하면 다음과 같다. 계산에서 사용한 전극은 MFC에서 많이 사용하는 3 M KCl과 NaCl을 기준으로 한다. 결과값은 KCl은 +210 mV vs. SHE, NaCl은 +209 mV vs. SHE로 계산된다(25℃, 1 atm 기준). 이를 기반으로 30℃ 기준으로써 계산을 하면 KCl은 207 mV vs. SHE, NaCl은 +206 mV vs. SHE로 3 mV의 차이가 생긴다.
4. Lab scale MFCMFC의 초창기 연구는 전극이나 반응기가 아닌 미생물의 연구를 중점적으로 진행했다. 2002년 CV와 연료 전지를 사용하여 철 환원 박테리아인 Shewanella putrefaciens에서 전극으로 직접 전자가 이동하는 것을 확인했으며, 이는 전자의 이동에 중간 매개체가 없어도 전자를 전극으로 전달할 수 있는 것을 증명했다[139]. 이후 2003년 중간 매개체가 없는 MFC의 성능을 최적화하기 위해 여러 조건에서 실험을 진행했고, 최적의 pH는 7 외부 저항은 500 Ω보다 낮으면 양성자 전달 및 용존 산소 공급을 제한하여 성능이 감소한 것을 밝혔다[140]. 이 시기의 다른 연구를 보면 하수슬러지를 생체촉매로 하고 Mn4+ 흑연 음극과 Fe3+ 흑연 양극을 사용하여 1750 mA/m2의 최대 전류 밀도와 788 mW/m2 최대 전력 밀도를 달성했다[141]. 이러한 결과는 미생물 연료 전지에 의해 전기를 충분히 생산할 수 있음을 증명했다.
이후 2004년부터 연구는 전극, 반응기와 같은 미생물이 아닌 연구가 중점적으로 진행되기 시작했다. 2004년의 연구 중 일실형과 이실형 반응기를 통해 가정 폐수를 처리함과 동시에 전기를 생산하는 것을 증명하는 연구가 있다. 이 연구에서 음극은 탄소 종이, 양극은 탄소 천을 사용했으며, 이실형에서 사용한 이온막은 PEM을 사용했다. 실험 결과는 이실형에서 262 mW/m2, 일실형에서 494 mW/m2의 최대 전력 밀도 및 이실형에서 45-55% 일실형에서 9-12%의 쿨롱 효율을 생산했다. 이는 이온막을 사용하지 않고 산소를 직접 탄소 양극으로 전달하는 시스템이 비용 효율적인 접근 방식에서 필요할 것이라고 했다[142]. 2005년 상향류 MFC가 개발과 일실형 MFC의 전극 간격 및 구성, 온도, 이온 강도(ionic strength)에 따른 성능을 연구했다[143,144]. 이러한 연구는 MFC의 다양한 연구가 시작됐다는 것을 보여주었다. 2006년의 대표적인 연구는 확산층을 촉매층과 분리한 양극, 양극에서 바인더로 주로 사용하던 나피온이 아닌 PTFE의 새로운 발견, 미생물 양극의 개발, 새로운 디자인인 스택 형태의 개발 등이 있었다[52,66,145,146]. 2007년 이전 MFC에서 주로 사용하는 음극은 탄소 종이, 탄소천과 같은 평평한 형태를 사용했지만, 2007년 흑연 과립을 사용한 음극을 관(tubular) 형태의 반응기와 접목시켜 새로운 시스템 개발과 현재 가장 많이 사용하는 브러쉬 형태의 음극이 개발됐다[147,148]. 브러쉬 음극을 사용한 연구에서 2400 mW/m2의 최대 전력 밀도를 생산했으며, 이후 양극의 연구뿐만 아니라 음극의 개질, 새로운 형태의 음극 등 많은 음극의 연구가 시작됐다[149,150].
MFC의 전력 밀도를 향상시키기 위해 많은 연구가 진행됐다. 1999년 음극의 표면적 기반으로 0.001 mW/m2에서 0.01 mW/m2로 증가했으며, 2003년 Mn4+ 흑연 음극과 Fe3+ 흑연 양극을 사용하여 788 mW/m2로 증가했다[141,151]. 2007년에 일실형 반응기에서 음극과 양극이 붙어있는 형태의 전극 2개와 0.2 M의 bicarbonate buffer를 사용하여 2770 mW/m2의 최대 전력 밀도를 달성했다[152]. 이후 전력 밀도는 꾸준히 향상하여 최근 4000 mW/m2 이상의 전력 밀도를 달성했다. 첫 번째로 브러쉬 음극, 활성탄과 ZIF-67을 결합하여 제작한 양극, 50 mM PBS를 사용하여 4203 mW/m2을 달성했으며 이는 50 mM PBS 기준으로 현재 세계에서 가장 높은 수치이다[93]. 두 번째로 탄소 천의 음극, Ni/CoNC의 촉매를 사용한 양극, 130 mM PBS를 사용하여 4335 mW/m2을 달성했다[153]. 마지막으로 탄소 펠트의 음극, 옥수수대를 기반으로 제작한 N-도핑 탄소 펠트 양극, 50 mM PFS (potassium ferricyanide solution)을 사용하여 4990 mW/m2을 달성했다[154].
5. 스케일 업 MFC스케일 업은 크기를 키우는 것 또는 규모를 확대하는 것을 의미한다. 즉, 스케일 업 MFC는 실제 실용화를 위해 반응기의 크기 및 규모를 키우는 것이다. 대부분의 MFC 연구는 실험실 규모에서 수행됐지만 실제 전기 장치에 전력을 공급하는데 필요한 전력 수준을 달성하려면 스케일 업을 하는 것이 불가피하다 [15]. 또한, MFC를 하폐수처리장과 같은 실제 응용 분야에 적합하게 만들려면 스케일 업을 하여 높은 전력 밀도를 달성하는 것이 중요하다.
MFC 스케일 업은 크게 일실형, 이실형, 플레이트(plate), 관(tubular) 및 스택(stack) 형태의 반응기로 구분할 수 있으며, 이 중 주로 관과 스택 형태로 스케일 업을 진행한다[155]. 하지만, MFC 스케일 업은 규모가 커지면 내부 저항의 증가, 전극 간의 거리의 변경, pH, 유량, 온도와 같은 운전조건 등에 의해서 성능이 감소한다[29,119,122,156-159]. 예를 들어 250 L로 규모로 스케일 업된 MFC는 0.47 W/m3의 최대 전력 밀도를 생산했다[160]. 이는 크기에 비례하여 높은 전력 밀도를 생산하지 않고 상대적으로 낮은 전력 밀도를 생산했다. 이는 반응기가 커짐에 따라 음극, 양극, 이온막 등 구성 요소의 내부 저항이 증가했기 때문이다. 이러한 MFC 스케일 업의 성능 감소를 밝히고 최적화를 위해 많은 연구가 진행 중이다. 이 외에도 내부 저항과 반응기 부피를 곱한 부피 기반 저항률의 관점을 연구한 사례가 있으며, 결과는 반응기 부피가 증가하면 부피 기반 저항이 증가하는 것을 확인했다[158]. 또한 MFC의 전극의 표면적과 생성된 전력 사이의 관계를 정량화한 연구는, 최대 전력 밀도가 음극의 표면적의 로그에 비례하는 것을 밝혔다[157].
최근 음극과 양극의 거리와 방향에 따라 MFC 성능과 내부 저항에 상당한 영향을 미치는 것을 확인한 연구가 있다[98]. 결과는 음극의 방향을 수직에서 수평으로 변경하면 최대 전력 밀도가 20% 증가, 음극의 저항은 60% 감소, 내부 저항은 49%가 감소하는 것을 확인했다. 또한 음극의 전류 포집체 중심과 탄소 섬유 중심을 brush 형태의 음극을 사용하는 MFC의 전기 화학을 설명하는데 통계적으로 중요한 기준점으로 발견했다. 그리고 동일한 크기를 가진 brush 형태의 음극을 사용할 때, 음극의 수와 구성이 MFC 성능 및 전기화학에 미치는 영향을 확인하고, MFC 성능 향상을 위한 음극의 위치와 삽입 방법을 제안한 연구도 있다[121]. 마지막으로 MFC 스케일 업을 진행할 때 전력 생산에 영향을 미치는 결정적인 요인은 부피가 커짐에 따라 음극과 양극의 표면적의 증가로 제시했다[161]. 즉, 전극의 표면적이 충분히 증가하면 전력 생산과 유기물 이용률이 극대화되어 더 높은 성능을 달성할 수 있다. 위 연구의 결과들을 종합하면 전극의 간격, 면적, 구성, 부피 등을 고려하고 최적화하면 스케일 업한 MFC의 성능을 증가시킬 수 있다.
5.1. 실험실 규모실험실 규모의 MFC는 1.5 µL에서 L 단위까지 여러 가지 규모의 반응기로 연구됐다[162-166]. 이중 실험실 규모로 스케일 업한 반응기는 1 L 이상의 규모로 간주할 수 있다. 이러한 규모의 반응기는 Table 8와 같이 주로 오랜 시간 동안 운전하거나 연속흐름식 형태로 운전된다[168-170].
MFC 스케일 업에서 중요한 부분인 전극의 연구는 많이 진행되고 있다. 예시로 가정용 폐수를 사용하여 여러 가지 부피와 음극 양극의 크기와 표면적에 따라 성능을 평가한 연구가 있다[167]. 이 연구는 250 mL, 1 L, 1.6 L로 총 3개의 반응기를 구성했다. 250 mL와 1 L 반응기는 사각형 형태의 통과 원통형 형태의 플라스틱 통을 사용하여 반응기를 제작했으며, 1.6 L 반응기는 플렉시글라스(plexiglas)를 사용하여 제작했다. 사용한 음극은 brush 형태로 250 mL에서 직경 5 cm, 길이 7 cm를 사용했으며, 1 L는 직경 5 cm, 길이 14 cm, 마지막으로 1.6 L는 250 mL에서 사용한 음극과 동일한 크기의 음극을 총 4개 사용했다. 양극의 표면적은 250 mL에서 24, 48, 72, 96 cm2까지 크기를 점점 늘려가며 사용했으며, 1 L는 132 cm2, 1.6 L는 290 cm2를 2개 사용했다. 각 규모별 결과는 1.6 L에서 6.8 W/m3, 1 L에서 4.3 W/m3의 최대 전력 밀도를 생산했다. 또한 250 mL에서 양극의 표면적이 96 cm2인 경우에 최대 전력 밀도 78 W/m3을 생산했다. 다른 예시로 MFC에 여러 가지 탄소 과립을 첨가하여 미생물의 성장과 음극의 유효 면적을 증가시킨 연구한 사례가 있다[171,172]. 탄소 과립이 첨가되면 전하 용량(charge storage)이 증가하여 MFC의 최대 전력 밀도가 증가하고 내부 저항이 감소했다. 하지만 너무 많은 탄소 과립은 오히려 쿨롱 효율이 낮아지고 미생물의 다양 성이 낮아졌다. 이러한 연구들은 MFC의 내부 구성요소인 음극, 양극의 면적, 크기에 따라 성능을 연구했으며, 이를 최적화하면 스케일 업에 비례하여 성능을 증가시킬 수 있는 방법 중 하나로 시사되고 있다.
MFC 스케일 업의 연구에서 전극뿐만 아니라 운전조건의 연구도 성능에 많은 영향을 미치는 것으로 밝혀졌다. 회분식으로 1 L 규모의 반응기를 낙농 폐수를 사용하여 MFC 여러 실험 조건에 따라 성능을 평가한 연구를 보면 반응기는 양성자 교환막(PEM)을 사용하여 음극부와 양극부로 구분하여 1 L 규모의 이실형 반응기로 제작했으며, 음극은 brush 형태를 사용했고, 양극은 탄소 천(carbon cloth)에 platinum black을 코팅하여 사용했다[173]. 실험 조건은 운전시간, 음극의 면적, 이온막의 두께, 이온막의 면적 등을 설정했다. 결과는 음극 면적 61 cm2, 48 시간의 운전시간, 효모 추출물 50 mg/L 일 때, 최대 전력 밀도 5.04 mW/m2을 생산했다.
운전조건 중 연속흐름식에서 공기의 흐름과 물이 흐르는 방향을 연구한 문헌이 있다[153,174,175]. MFC의 양극부에 스페이서를 부착하면 공기의 흐름이 원활하게 흐르게 하고 양극 표면의 막힘을 최소화하여 32 W/m3의 최대 전력 밀도를 달성 및 HRT 8시간에서 COD 제거율 57%를 달성했다. 물이 흐르는 방향에 관한 연구는 85 L의 규모로 진행을 했다. 물의 방향은 대각선과 수평 방향 2가지와 추가적으로 HRT 22분과 77분에 따른 성능을 비교 분석했다. 결과는 대각선 방향 HRT 22분은 0.118 W/m2, 77분은 0.106 W/m2, 수평방향 HRT 22분은 0.109 W/m2, 77분은 0.100 W/m2을 나타냈으며, 대각선 방향 HRT 22분이 0.118 W/m2의 최대 전력 밀도로 가장 높은 성능을 달성했다. 이 결과는 수평방향 HRT 77분과 비교하여 최대 전력 밀도가 약 18%의 차이를 보였으며, 이러한 이유는 음극의 과전압의 감소 때문이었다. 이 연구들은 스케일 업에 영향을 미치는 여러 조건들을 밝혔다. MFC 스케일 업에서 운전조건은 중요한 요소임을 밝혔으며, 운전조건을 최적화하면 성능 향상에 긍정적인 영향을 미칠 수 있음을 입증했다.
위 연구들은 스케일 업을 할 경우 성능에 영향을 미칠 수 있는 각 조건들을 연구했다. MFC를 하폐수처리장과 같은 실제 응용 분야에 접목하기 위하여 처리를 진행함과 동시에 에너지를 생산 및 회수하는 연구도 많이 진행 중에 있다[176-178]. 최근에는 MFC 양극에서 금속 촉매 양극을 사용하지 않고 미생물 양극을 사용한 연구도 활발하게 진행 중이다. 이러한 연구 중 1.84 L 규모에서 ANAMMOX 첫 단계에 접목하여 탈질과 전력 생산을 동시에 달성한 연구가 있다[179]. 반응기는 각각 2개의 브러시 형태 음극과 양극을 사용했으며, 이를 병렬로 연결했다. 음극부와 양극부는 이온막을 사용하여 구분했는데 이때 사용한 이온막은 미생물 이온막을 사했였다. 탈질을 위해 초기 유입수의 총 질소 농도를 150, 300, 450, 600 mg/L로 설정했다. 최대 전력 생산은 총 질소 농도가 150 mg/L에서 3.4 W/m3을 달성했으며, 총 질소 농도가 150 mg/L보다 높아지면 오히려 전력 밀도가 떨어졌다. NH4+-N 제거는 총 질소 농도가 50 mg/L일 때 최대 98%까지 달성했다. 이는 미생물 양극을 사용한 MFC는 ANAMMOX 공정의 첫 단계로 적합하는 것을 입증했다.
위의 연구 외에 고강도 축산 폐수를 이용하여 4 L 규모에서 지속적으로 처리함과 동시에 전력 생산한 연구가 있다[180]. 처리는 2단계 공정으로 진행했으며, 1단계는 연속 교반 방식으로 처리를 진행하고 1단계 유출수를 2단계 공정에서 미생물 양극을 사용하여 2차 처리를 했다. 처리 결과는 COD 제거율 97.7%, NH4+-N제거율 85.1%, TN 제거율 43.8%, 2.509 kWh/m3의 순에너지 생산을 달성했다. 또한, 미생물 양극과 이온막을 사용하여 10 L 규모에서 미생물 이온막의 재료와 개수에 따라 성능을 평가한 연구도 있다[181]. 결과는 COD 제거율 86%, 최대 전력 밀도 67.5 mW/m2을 달성했다. 성능은 미생물 양극과 더 높은 투과성을 가진 미생물 이온막에 의해서 제한됐으며, 미생물 이온막 투과성은 미생물 양극과 이온막의 미생물 군집 구조에도 영향을 미친 것을 확인했다.
5.2. 스택 반응기MFC는 현재 실험실 수준의 분석 및 평가 단계에 있지만 최근 몇 년 동안 MFC를 실제 구현에 통합하기 위해 새롭고 독창적인 디자인이 개발됐다. 그중 전극 간격, 면적 및 방향 등의 문제를 해결하기 위해 스택 형태의 연구가 진행되고 있다. 스택 MFC는 연속흐름 시스템에서 하나의 유입수를 공유하는 여러 장치나 모듈을 연결하여 폐수처리를 목적으로 사용할 수 있으며, 몇몇 연구에서 스택 형태는 스케일 업에 더 효과적인 방법일 수 있음을 입증했다[14,84,163,182-187]. 스택 형태의 스케일 업 초기 연구 중 하나는 고강도 축산 폐수를 5개의 모듈로 구성한 스택 MFC에 연결하여 처리했다[184]. 이 연구는 기존의 스택 MFC의 양극의 단점을 극복하기 위하여 새롭게 설계 및 개발했다. 5개의 모듈이 직렬 또는 병렬로 연결됐고, COD 제거율 77%, 최대 전력 밀도 176 W/m2을 달성했다. MFC 스케일 업에서 최적의 구성을 제안하기 위해 연속흐름에서 운전하는 다양한 MFC 크기를 연구한 사례가 있다[182]. 반응기 구성은 소규모 MFC (6.25 mL)를 각각 5 개 및 10 개씩 연결했고, 25 mL 규모 반응기 및 500 mL 규모 반응기의 성능을 비교했다. 그 결과 음극부 부피 단위당 전력 밀도는 대조군 대비 소규모 5개를 연결한 반응기에서 33%, 소규모 10개를 연결한 반응기에서 29%, 25 mL 반응기에서 35%, 500 mL 반응기에서 72% 감소했다. 이러한 결과는 단일 장치의 크기를 늘리는 것보다 여러 소규모 장치를 연결하는 것이 MFC 스케일 업을 더 잘 수행할 수 있음을 시사한다.
MFC 장치가 스택으로 연결된 경우 스택 크기 및 구성에 따라 전압, 전류 또는 둘 모두를 높일 수 있다. 각각의 모듈을 추가하거나 제거를 통해 스택의 전체 부피 및 크기를 조정하여 에너지 요구 사항을 충족할 수 있으므로 매우 유용하다. 그러나 여러 MFC를 직렬로 연결하면 전압 반전, 전압 손실 및 각 모듈별 불규칙한 작동 등과 같은 일부 문제가 발생한다[14,183,188]. 직렬 연결한 MFC의 예시로 5개의 모듈을 직렬로 연결하여 8개월 동안 하수를 처리한 연구가 있다[189]. 이는 연속흐름 방식으로 운전됐으며 COD 제거율과 총 질소 제거 효율은 처음 1달 동안 각각 78%, 77%였지만, 8개월 운전 후 처리 효율이 증가하여 각각 85%, 94% (COD 유출수 농도: 20.7 ± 2.5 mg/L, T-N 유출수 농도: 1.7 ± 0.1 mg/L)를 달성했다. 이 연구에서 COD제거와 질소 제거는 대부분 처음과 두 번째 모듈에서 진행됐으며, 뒤쪽 모듈로 갈수록 유입수의 COD와 총 질소가 낮아져서 높은 성능을 보이지 못했다.
구불구불한 형태(serpentine-type)로 총 40개의 모듈을 연결하여 스택 MFC를 제작한 연구가 있다[185]. 이 연구에서 스택 MFC는 10 L 규모로 제작됐으며 양조장 폐수를 처리했다. 결과는 개방 회로 전압을 23 V까지 생산했으며, 최대 전력 밀도는 4.1 W/m3을 달성했다. 하지만 장시간 운전을 하니 성능이 감소했다. 이는 스택 MFC에서 장시간 운전 시 성능이 저하되는 것은 양극에 의한 것으로 밝혀졌다[185,189]. 스택 MFC를 장시간 운전하면 유입수에 존재하는 여러 유기물과 무기물에 의해 양극 표면에 염, 침전물 및 미생물 부착이 되어 양극이 비활성화됐고 이는 성능 저하로 이어졌다. 이러한 성능 저하를 해결하기 위해 양극에 붙어 있는 염이나 이물질을 물로 세척하면 성능이 회복됐다. 양극 표면에 염이나 침전물이 부착에 의한 성능 저하는 장기간 운전 시 공통적으로 발생하는 문제이다[14,184,185,189-191]. 이를 극복하는 방법 중 하나는 양극에서 수분이 증발하는 양을 줄이거나 부분적으로 잠긴 양극을 충분히 물에 적셔주는 것이다[178,192-194].
스택 MFC는 일반적으로 전기적, 수리학적으로 모두 연결되어 연속흐름 조건에서 운전한다. 하지만, 연결하는 모듈의 수가 증가할수록 모듈간의 연결이 더욱 복잡해지며, 연결한 모듈을 연속흐름 조건으로 연결 및 운전하려면 모듈의 유입 및 유출을 유동적(fluidic)으로 결합해야 한다[182,195]. MFC의 초창기 연구 중에서 모듈을 전기적, 수리학적 연결과 분리에 따른 성능을 평가한 연구가 있다[14]. 이 결과에 따르면 전기적으로 연결되고 수리학적 분리가 된 상태에서의 성능은 1.3 W/m3으로 둘 다 연결된 상태보다 약 36% 더 높은 값을 나타냈다. 이는 수리학적 분리가 스택 MFC에 더 좋은 영향을 미칠 수 있다는 것을 시사한다. 하지만 수리학적 분리가 된 스택 MFC는 기질의 공급 및 배출을 위한 개별적인 재순환이 필요하며 특히 하수처리장과 같은 곳에서 응용을 하기 위해서는 필수적이다. 이러한 연결 문제를 해결하기 위해 양이온 교환막을 추가하여 내부적으로 연결된 새로운 형태의 스택 MFC가 개발됐다[183]. 각 모듈의 성능은 COD제거율과 전력 밀도에 중점을 두었으며, 단일 모듈에서 1 W/m3의 최대 전력 밀도와 32%의 COD 제거율을 보였지만 2개의 모듈을 연결한 결과 1.4 W/m3의 최대 전력 밀도와 54%의 COD 제거율을 달성했다.
5.3. 파일럿(Pilot) 규모 스케일 업파일럿 규모의 반응기를 테스트하는 대표적인 방법은 MFC 기반 시스템을 폐수처리 시설에 접목하는 것이며, 실제 많은 파일럿 규모의 연구들은 실제 하수처리와 접목하여 진행했다[178,196-200]. 하지만 MFC의 연구는 파일럿 규모의 연구보다 실험실 규모로 많이 진행 중에 있으며 파일럿 규모의 연구는 아직 많이 진행되지 않았다. MFC에 대한 첫 번째 파일럿 규모 스케일업은 호주 퀸즐랜드 골드 코스트시에 있는 야탈라에서 진행됐다[201]. 이때 사용한 반응기는 높이가 3 m, 부피는 1 m3로 총 12개를 제작했다. 반응기는 관형 반응기로 내부에 탄소 섬유 brush를 음극으로 사용했고, 반응기 외부는 흑연 섬유 brush를 사용한 양극을 설치했다. 유입수는 반응기 내부로 들어가서 튜브를 통해 위로 흐르고 양극으로 이동했다. 이 연구에 관한 내용은 많이 알려져 있지 않다. 현재까지 알려진 바로는 i) 양조장에서 진행을 했으며, ii) 용액의 전도도가 낮고, iii) 전류 생산이 제한됐으며, iv) 음극부의 유출수에 과도한 COD로 인해 양극에 생물막이 과도하게 축적됐다는 것이다.
최근 파일럿 규모의 연구에서 낮은 농도의 COD로 운영될 때에도 안정성을 보여준 도시 폐수 처리장에 막이 없는 45 L 스택의 통합을 제시했다[202]. 이온막을 사용하여 총 부피 72 L 스택 반응기를 사용하여 회분식과 연속흐름식을 연구한 사례가 있다[203]. 결과는 회분식에서는 51 W/m3의 최대 전력 밀도, 97%의 COD 제거율을 보였고, 연속흐름식에서는 42 W/m3의 최대 전력 밀도, 5.2 kg COD/m3 ・d의 COD 제거율을 달성했다. 하지만 병렬 회로에서 전류 손실이 발생했다. 이 외에도 총 부피 90 L (18 L 모듈 5 개)의 양조장 폐수를 활용한 파일럿 연구에서 직물 기반 분리막을 사용하여 음극과 양극 사이의 단락을 방지하고 생산된 전기를 펌핑 시스템을 구동하는데 사용한 연구가 있다[204].
MFC의 실증을 위해 파일럿 규모로 MFC를 스케일 업하여 실제 하수처리장과 접목한 사례가 있다[117,196,197,199]. 파일럿 규모로 하수처리장에 접목한 사례 중에서 1000 L 스택 MFC 시스템을 구축하여 도시 폐수를 처리한 연구가 있다[197]. 이 연구는 MFC 반응기 안에서 물이 흘러가는 방향을 2가지 방식으로 설정하고 2개의 폐수처리장에서 1년 이상 COD 농도에 따른 폐수 처리 능력을 평가했다. 결과는 유출수의 COD 농도는 50 mg/L 미만으로 COD 제거율 90%, 70 W/m3의 최대 전력 밀도, HRT 2시간으로 도시 폐수 1 m3당 0.033 kWh/m3의 에너지 회수를 달성했다. 다른 연구는 1.5 m3 규모로 미생물 음극, 양극 그리고 분리막을 사용하여 여름부터 겨울까지 4개월 동안 1차 침전조 방류수를 처리했다[117]. 그 결과 HRT 5시간 기준으로 COD (25 ± 7 mg/L), TN (13 ± 2 mg/L), NH4+-N (3 ± 1 mg/L) and SS (10 ± 3 mg/L)를 처리했으며, 미생물 분리기의 경우 1 m3당 406 ± 30 mW/m3의 전력 생산을 달성했다. 이 외에 미생물 양극과 이온막을 이용하여 1.5 m3 규모의 스택 MFC를 개발 및 성능을 평가한 연구가 있다 200). 반응기는 1차 침전지, 생물학적 전기화학 처리조, 2차 침전지로 구분했으며, 원활한 처리를 위하여 생물학적 전기화학 처리조에 폭기를 했다. 각 반응조의 HRT는 1차 침전지 1시간, 생물학적 전기화학 처리조 5시간, 2차 침전지 0.5시간으로 설정했다. 유입수의 방향은 48시간마다 주기적으로 변경하여 음극의 성능을 안정화했고, 이는 물의 흐름에 따라 반응기의 균일성을 유지하는데 효과적인 것을 입증했다. 최대 전력 밀도는 20 mW/m2이었으며, 에너지 요구량은 일반적인 활성 슬러지 공정의 7.3%에 불과했다. 이 외에도 최근 64개의 모듈로 구성하여 1 m3의 규모로 제작한 연구가 있다[196]. 유입수는 하수처리장의 1차 정화조 유출수를 사용했다. 결과는 최대 95%의 COD 제거율, 암모니아는 48%, 유기 미량 오염물질은 65%를 제거했고 약 12%의 에너지 효율로 0.06 kWh/m3의 전력을 생산했다.
파일럿 규모 연구 중 하수처리장이나 양조장과 같은 폐수를 사용한 것이 아닌 실제 화장실에 접목한 연구가 있다[178,198]. 이 연구는 화장실 소변기에 MFC를 접목하여 실제 화장실의 내부 조명에 필요한 전력을 MFC로 생산하여 사용했다[178]. 첫 번째 테스트는 2015년 2월부터 5월까지 브리스틀 웨스트잉글랜드 대학교 Frenchay 캠퍼스에 설치했으며, 두 번째 테스트는 2015년 6월 영국 남서부 Worthy Farm에서 열린 Glastonbury Music Festival에 설치했다. 소변기의 실시간 전기 출력은 온도와 유속에 따라 사용된 MFC의 수에 비례했다. 캠퍼스 소변기는 288개의 MFC로 구성되어 평균 75 mW, 최대 160 mW의 전력을 생산했으며, 축제에 설치된 소변기는 432 개의 MFC로 구성되어 평균 300 mW, 최대 400 mW의 전력을 생산했다. COD 제거율은 캠퍼스 소변기의 경우 약 95%, 축제 소변기의 경우 평균 30%이었다. 이러한 결과는 파일럿 규모의 MFC를 화장실에 접목하여 전력 생산과 COD제거에 MFC를 입증한 첫 번째 시도이다. 이 연구 이후 다시 한 번 Glastonbury Music Festival의 화장실 소변기에 MFC를 접목하여 설치했다[198]. 반응기는 총 12개의 모듈로 이루어진 스택 MFC로 구성했다. 이 실험의 결과는 이전 연구에 비하여 COD 제거율은 37%가 향상됐으며, 전력 생산은 약 30%가 증가함에 따라 에너지 회수는 0.022 kWh/m3에서 0.346 kWh/m3으로 향상됐다. 이 결과는 MFC 스케일 업의 난제 중 하나인 크기가 커짐에 따라 생산되는 전력이 감소하는 것을 개선했으며, 국내 하수처리장에서 하수처리에 필요한 전력 사용량(0.4 kWh/m3)의 약 86.5%를 MFC를 통해 충당할 수 있다[205,206]. 다시 말하면, 스택형 MFC를 통해 향상된 전력 생산은 MFC 실용화의 궁극적인 목표인 에너지 공급형 하수처리장이 가까워졌다는 것을 시사한다.
파일럿 규모의 MFC는 주로 하수처리장에 접목하여 테스트하지만 그 외 습지나 식물 뿌리를 이용하여 테스트하는 경우가 있다[207-211]. 습지에 접목한 연구의 예시로 30 L 파일럿 규모로 습지에 접목하여 연구한 사례가 있다. 이 연구의 결과는 92%의 COD 제거율, 97%의 NH4+-N 제거, 8 mW/m2의 최대 전력 밀도를 달성했다[207]. 연구에서 사용한 전극은 1개의 양극과 4개의 양극을 이용했는데, 이때 음극과 양극을 병열로 연결하는 것이 4개의 음극을 1개의 외부저항과 연결시켜 양극과 연결하는 것보다 더 좋다는 것을 밝혔다. 또한, 습지에 접목하여 MFC를 테스트할 때, 양극과 공기의 접촉을 꾸준히 유지하는 것이 습지에 접목한 MFC의 핵심 요소임을 밝혔다. 식물 뿌리에 접목한 사례는 식물 뿌리 아래 즉, 땅속에 MFC를 접목해서 11.67 mW/m3의 최대 전력 밀도를 달성했다[208]. 이 연구는 MFC를 땅속에 접목하면 MFC의 음극이 오염물질의 산화를 위한 임시 전자 수용체 역할을 해서 오염물질의 처리 성능을 약 33%이상 향상시킬 수 있음을 입증했다. 이러한 연구 결과는 MFC가 하수처리장뿐만 아니라 더 많은 범위에 접목할 수 있으며, 탁월한 폐수처리 능력을 가진 것을 알 수 있다.
6. 향후 전망폐수는 환경 오염의 주요 원인으로 인식되고 있다. 현재 폐수처리기술은 악취, 에너지, 슬러지, 비용 등의 많은 단점이 있다. MFC는 폐수를 처리함과 동시에 추가적인 공정 없이 에너지를 폐수에서 바로 추출할 수 있고, 이 추출된 에너지는 하수처리 공정으로 다시 사용이 가능하여 하수처리공정에 필요한 에너지와 관련된 비용을 줄일 수 있다. 또한, MFC는 활성 또는 혐기성 처리에 비해 슬러지 생산량이 낮고 이전 연구에 따르면 MFC를 통해 여러 종류의 오염물질을 효과적으로 제거할 수 있다[212-214]. 이러한 이점을 제공하는 MFC는 환경친화적인 공정으로 폐수처리 분야에서 혁신적인 기술로 인식되고 있다.
지난 20여년 동안 MFC의 실용화를 위해 많은 연구가 수행됐고, 그에 따라 많은 문제가 확인됐다. 가장 중요한 문제는 MFC의 비용 효율성이다. 이전 연구에 따르면 MFC의 스케일 업에 필요한 비용은 735 - 36,000 $/m3이다[197,215]. 높은 비용의 문제는 MFC의 구성 요소인 전극과 이온막이 주요 원인이었으며. 양극의 촉매와 이온막의 비용이 전체 비용의 약 80%를 차지한다[216]. 대표적으로 양극과 이온막에서 많이 사용하는 촉매인 백금 촉매의 비용은 150 $/g으로 가격이 매우 높으며, 백금 촉매를 사용하면 비용이 크게 증가하여 스케일 업에 적합하지 않다[217]. 즉, 비용을 줄이기 위해 높은 경제성과 성능을 가진 전극과 막 개발이 필요하다. 최근 스케일 업에 미생물을 양극과 이온막에 접목시켜 사용하기 시작했다[117,218]. 미생물 양극과 미생물 이온막은 기존 전극과 이온막의 문제점인 안전성, 내구성, 높은 비용, 막힘 현상, 높은 내부 저항 등을 개선할 수 있다[219,220]. 즉, 미생물 양극과 미생물 이온막은 MFC 스케일 업에 가장 중요한 문제인 비용을 획기적으로 줄일 수 있고 에너지 생산 및 오염물질 제거를 할 수 있어 향후 실용화에 유망한 방법으로 생각된다.
전극과 이온막의 비용 외에도 펌프, 혼합, 폭기와 같은 전력 소비에 관한 운영 비용도 전체적인 비용에 영향을 미친다[221]. 그리하여 수중에 MFC를 사용하거나 스택형 모듈을 사용하여 기존 하수처리장에 접목하여 펌프나 폭기에 필요한 에너지 소비를 줄일 수 있어 비용 효율적이고 지속 가능하다[222]. 운영 비용을 줄이기 위한 방법으로 MFC의 전력 생산을 높이는 것도 있다. 즉, 폐수처리와 관련하여 MFC에 필요한 에너지를 소비하는 것이 아닌 MFC에서 생산한 자체 전력을 이용하여 운영 비용을 낮추는 것이다. 전력 생산을 높이는 방법으로는 전극이나 이온막의 개선도 있지만, 여러 모듈을 사용하는 스택형 반응기를 사용하는 방법도 있다. 스택형 반응기를 사용하면, 에너지 손실을 줄일 수 있어 더 높은 전력을 생산하는 것이 입증됐다[223]. 하지만 반응기를 스택형으로 구성하면 동역학적 불균형 및 전압 역전(voltage reversal)이 생기는 문제가 있다[203,224-225]. 스택 MFC의 높은 성능을 달성하고 전압 역전 등을 방지하려면 전극 유형, 모듈 형태, 연결 방법 등을 신중하게 고려하고 선택해야 한다. 이러한 비용은 MFC의 구성 및 운전 방법 등에 따라 달라지므로 구성 요소의 비용과 운영비용 간의 균형은 전력 생산과 함께 지속 가능한 폐수처리의 핵심이다.
MFC의 실용화를 위해서는 비용뿐만 아니라 운전조건, 장기적인 내구성, COD 및 영양염류의 제거도 고려해야 한다. 운전조건은 온도, pH, 유기물 부하율, 전도도, HRT, 기질의 염도, 접종 방법 등이 연구되고 있으나 이러한 연구들은 대부분 실제 폐수에서 연구되지 않고 특정 기질 및 농도를 사용하여 연구된다[227-233]. 따라서 운전조건에 관한 연구는 MFC 실용화를 위해 실제 폐수를 기반으로 심도 있게 연구되어야 한다. 또한, 실제 폐수를 이용하여 연구를 진행하면 생물학적 오염, 부식, 막힘 현상을 야기할 수 있어 장기적으로 운전하기 위해 내구성에 관한 연구도 필요하다[234-236]. 이러한 연구뿐만 아니라 MFC의 실용화를 위해서는 높은 유기물 및 영양염류의 제거를 달성해야 한다. 하지만 실제 폐수는 많은 오염물질이 존재하여 MFC가 모든 물질을 제거할 수는 없으므로 오염물질의 제거는 기존의 다른 하수처리 공정을 접목하여 전처리와 후처리를 통해 높은 제거율을 달성할 수 있다[237,238].
MFC는 많은 분야에 적용이 가능하지만, 가장 유망한 응용 분야는 폐수처리 분야이다. MFC는 하수처리장에 접목하여 남아있는 유기물을 제거할 수 있고 하수처리장 운영을 위한 에너지를 생산할 수 있다. 이러한 MFC는 성능 개선을 위해 많은 연구가 수행됐고, 실제 하수처리장과 접목하는 성과를 보이는 등 MFC 실용화의 가능성을 보여줬다. 현재 MFC 스케일 업의 연구 추세는 다음과 같다. i) 높은 비용을 줄이기 위한 높은 경제성과 성능을 가진 전극과 막의 개발, ii) 장기간 운전을 위해 오염, 부식 및 막힘에 대한 내성을 가진 재료의 개발, iii) 손실을 최소화하기 위해 여러 개의 모듈을 연결하는 방식인 스택 형태로 스케일 업을 진행한다. 하지만 스케일 업을 방해하는 여러 가지 장애물은 여전히 존재한다. 주요 장애물로는 높은 비용, 내부 손실에 따른 낮은 전력 생산, 내구성 및 오염물질의 제거이다. 따라서 높은 비용과 내부 손실을 줄이기 위해 효율적인 전극과 이온막의 개발과 실제 폐수의 처리 효율을 증가시키는 것이 중요하다. 지금까지 MFC 스케일 업의 연구 결과를 보면 스택 형태로 구성하는 것이 내부 손실을 줄여 높은 성능을 달성할 수 있고 단일 반응기의 규모를 키우는 것보다 저렴하며, 높은 오염물질 처리능력을 보여줬다. 향후 실용화를 위한 스케일 업의 연구 전략을 제안하면 다음과 같다. 첫 번째로 스택 형태의 반응기를 이용, 두 번째로 내부 저항과 비용을 줄이기 위해 이온막이 없는 반응기 사용, 세 번째로 양극을 내구성과 지속가능성의 궁극적인 촉매인 미생물 양극의 사용, 마지막으로 처리 효율을 높이기 위해 다른 하수처리 공정을 접목하여 전처리 및 후처리를 통해 높은 처리 효율 달성이다. 이러한 MFC 기술은 환경, 화학, 에너지, 생물학, 재료 등과 같은 많은 학문이 결합된 연구이다. 즉, 학자들의 긴밀한 협업이 중요하다. 앞으로 지속적인 연구를 진행하면 MFC 기술의 궁극적인 목표인 에너지 공급형 하폐수처리장의 실용화가 멀지 않았으며, 지속 가능한 물에너지 연계(water-energy nexus)의 유일한 기술로 우뚝 설 것이다.
Acknowledgments이 논문은 대한민국 과학기술정보통신부의 재원으로 한국연구재단 중견연구자지원사업(NRF-2021R1A2C1013989), 전남대학교 학술연구비(과제번호 2020-3907) 및 2021학년도 대진대학교 학술연구비의 지원을 받아 수행되었습니다.
NotesDeclaration of Competing Interest The authors declare that they have no known competing financial interests or personal relationships that could have appeared to influence the work reported in this paper. Fig. 1.Numbers of publications of the scientific literature on microbial fuel cells and microbial fuel cell scale-up (Google Scholar). 
Fig. 3.Schematics of two-chamber MFC with PEM (A) and AEM (B). M: metal ion; X: anion; PEM: proton exchange membrane; CEM: cation exchange membrane; AEM: anion exchange membrane. 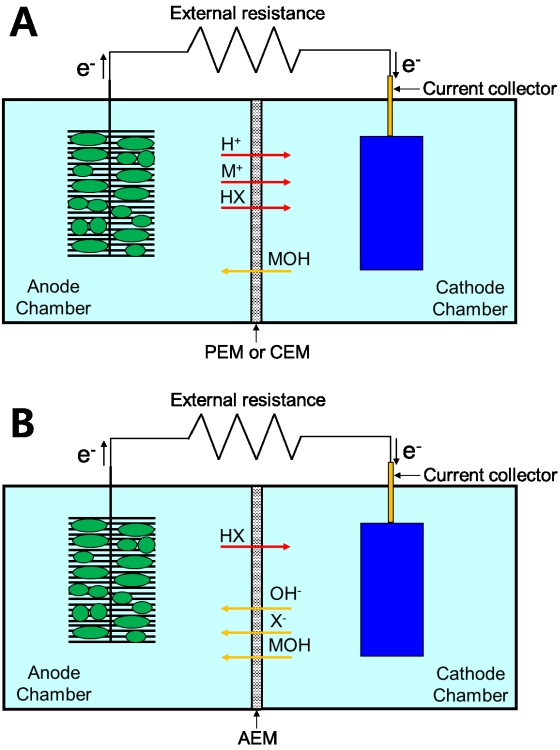
Table 1.Anode and cathode theoretical potentials (E0) and real potentials in MFCs (E). All potentials are shown against SHE. Theoretical condition is STP. E values are adjusted for pH = 7, T = 298.5K. Unless otherwise specified, chemical concentration is 1 mol or 1 atm. [21] Table 2.Characteristics of anode materials in MFC
Table 3.List of biomass, composite material and graphene modified-based anode
GL = Graphite layer; GP = Graphene particles; GOA = Graphene oxide aerogel; GFB = Graphite fiber brush; rGO = Reduced graphene oxide; CF = Carbon felt; GO = Graphene oxide; PANI = Polyaniline; DGMBE = Dual graphene modified bioelectrode; GRF = Graphene riboflavin; Gr = Graphene; CP = Carbon paper; CB = Carbon brush; GOZ = Graphene oxide zeolite; SSM = Stainless steel mesh; CC = Carbon cloth; PAM = Polyacrylamide; PDA-rGO = Polydopamine decorated reduced oxide graphene. Table 4.List of various ORR catalysts for MFCs.
Table 5.List of various types of membrane for MFCs.
Table 6.Energy efficiency corrected using -874.3 kJ/mol heat of combustion.
Table 7.Comparison of maximum power density in various MFC.
Table 8.Recent scale-up studies on microbial fuel cell
References2. Unicef, Progress on household drinking water, sanitation and hygiene, 2000-2020, https://data.unicef.org/resources/progress-on-household-drinking-water-sanitation-and-hygiene-2000-2020/, 2021
3. Enerdata, World energy, https://yearbook.enerdata.co.kr/total-energy/world-consumption-statistics.html, (Nov 01 2018)
4. D. R. Lovley, Bug juice: harvesting electricity with microorganisms, Nature Reviews Microbiology., 4(7), 497-508(2006).
5. B. E. Logan, B. Hamelers, R. Rozendal, U. Schröder, J. Keller, S. Freguia, P. Aelterman, W. Verstraete, K. Rabaey, Microbial fuel cells: methodology and technology, Environmental science & technology., 40(17), 5181-5192(2006).
6. M. C. Potter, Electrical effects accompanying the decomposition of organic compounds, Proc. R. Soc. Lond. B., 84(571), 260-276(1911).
7. B. Cohen, The bacterial culture as an electrical half-cell, J. Bacteriol., 21(1), 18-19(1931).
8. S. G. A. Flimban, I. M. I. Ismail, T. Kim, S.-E. Oh, Overview of Recent Advancements in the Microbial Fuel Cell from Fundamentals to Applications: Design, Major Elements, and Scalability, Energies., 12(17), 3390(2019).
9. A. Shukla, P. Suresh, B. Sheela, A. Rajendran, Biological fuel cells and their applications, Current science., 87(4), 455-468(2004).
10. B. H. Kim, H. J. Kim, M. S. Hyun, D. H. Park, Direct electrode reaction of Fe (III)-reducing bacterium, Shewanella putrefaciens, Journal of Microbiology and Biotechnology., 9, 127-131(1999).
11. D. R. Bond, D. R. Lovley, Electricity Production by Geobacter sulfurreducens Attached to Electrodes, Applied and Environmental Microbiology., 69(3), 1548(2003).
12. J. Sokhee Philemon, Practical Implementation of Microbial Fuel Cells for Bioelectrochemical Wastewater Treatment, Journal of the Korean Society of Urban Environment., 13(2), 93-100(2013).
13. H. Wang, Z. J. Ren, A comprehensive review of microbial electrochemical systems as a platform technology, Biotechnology advances., 31(8), 1796-1807(2013).
14. L. Zhuang, S. Zhou, Substrate cross-conduction effect on the performance of serially connected microbial fuel cell stack, Electrochemistry Communications., 11(5), 937-940(2009).
15. V. Oliveira, M. Simões, L. Melo, A. Pinto, Overview on the developments of microbial fuel cells, Biochemical engineering journal., 73, 53-64(2013).
16. I. Gajda, J. Greenman, I. A. Ieropoulos, Recent advancements in real-world microbial fuel cell applications, Current Opinion in Electrochemistry., 11, 78-83(2018).
17. Y.-C. Song, D.-S. Kim, J.-H. Woo, K. Yoo, J.-W. Chung, C.-Y. Lee, Modification of Anode Surface with Hydrogel and Multiwall Carbon Nanotube for High Performance of Microbial Fuel Cells, Journal of Korean Society of Environmental Engineers., 34(11), 757-764(2012).
18. Y.-C. Song, J.-H. Woo, K.-S. Yoo, Materials for microbial fuel cell: electrodes, separator and current collector, Journal of Korean Society of Environmental Engineers., 31(9), 693-704(2009).
19. B. E. Logan, Exoelectrogenic bacteria that power microbial fuel cells, Nature Reviews Microbiology., 7(5), 375-381(2009).
20. R. K. Thauer, K. Jungermann, K. Decker, Energy conservation in chemotrophic anaerobic bacteria, Bacteriological reviews., 41(1), 100-180(1977).
21. R. Ma, G. Lin, Y. Zhou, Q. Liu, T. Zhang, G. Shan, M. Yang, J. Wang, A review of oxygen reduction mechanisms for metal-free carbon-based electrocatalysts, npj Computational Materials., 5(1), 1-15(2019).
22. S. Tanisho, N. Kamiya, N. Wakao, Microbial fuel cell using Enterobacter aerogenes, Bioelectrochemistry and Bioenergetics., 21(1), 25-32(1989).
23. X.-Y. Wu, F. Tong, T.-S. Song, X.-Y. Gao, J.-J. Xie, C. C. Zhou, L.-X. Zhang, P. Wei, Effect of zeolite-coated anode on the performance of microbial fuel cells, Journal of Chemical Technology & Biotechnology., 90(1), 87-92(2015).
24. T. Huggins, H. Wang, J. Kearns, P. Jenkins, Z. J. Ren, Biochar as a sustainable electrode material for electricity production in microbial fuel cells, Bioresource Technology., 157, 114-119(2014).
25. N. Zhu, X. Chen, T. Zhang, P. Wu, P. Li, J. Wu, Improved performance of membrane free single-chamber air-cathode microbial fuel cells with nitric acid and ethylenediamine surface modified activated carbon fiber felt anodes, Bioresource Technology., 102(1), 422-426(2011).
26. C. Santoro, M. Guilizzoni, J. P. Correa Baena, U. Pasaogullari, A. Casalegno, B. Li, S. Babanova, K. Artyushkova, P. Atanassov, The effects of carbon electrode surface properties on bacteria attachment and start up time of microbial fuel cells, Carbon., 67, 128-139(2014).
27. Y.-Y. Yu, C. X. Guo, Y.-C. Yong, C. M. Li, H. Song, Nitrogen doped carbon nanoparticles enhanced extracellular electron transfer for high-performance microbial fuel cells anode, Chemosphere., 140, 26-33(2015).
28. K. Dolch, J. Danzer, T. Kabbeck, B. Bierer, J. Erben, A. H. Förster, J. Maisch, P. Nick, S. Kerzenmacher, J. Gescher, Characterization of microbial current production as a function of microbe–electrode-interaction, Bioresource Technology., 157, 284-292(2014).
29. T. Nam, S. Son, B. Koo, H. V. H. Tran, J. R. Kim, Y. Choi, S. P. Jung, Comparative evaluation of performance and electrochemistry of microbial fuel cells with different anode structures and materials, international journal of hydrogen energy., 42(45), 27677-27684(2017).
30. M. Zhou, M. Chi, J. Luo, H. He, T. Jin, An overview of electrode materials in microbial fuel cells, Journal of Power Sources., 196(10), 4427-4435(2011).
31. T. Cai, L. Meng, G. Chen, Y. Xi, N. Jiang, J. Song, S. Zheng, Y. Liu, G. Zhen, M. Huang, Application of advanced anodes in microbial fuel cells for power generation: A review, Chemosphere., 248, 125985(2020).
32. J. M. Sonawane, A. Yadav, P. C. Ghosh, S. B. Adeloju, Recent advances in the development and utilization of modern anode materials for high performance microbial fuel cells, Biosensors and bioelectronics., 90, 558-576(2017).
33. V. S. Sarathi, K. S. Nahm, Recent advances and challenges in the anode architecture and their modifications for the applications of microbial fuel cells, Biosensors and Bioelectronics., 43, 461-475(2013).
34. X. Quan, H. Xu, B. Sun, Z. Xiao, Anode modification with palladium nanoparticles enhanced Evans Blue removal and power generation in microbial fuel cells, International biodeterioration & biodegradation., 132, 94-101(2018).
35. M. Jarosz, J. Grudzień, K. Kamiński, K. Gawlak, K. Wolski, M. Nowakowska, G. D. Sulka, Novel bioelectrodes based on polysaccharide modified gold surfaces and electrochemically active Lactobacillus rhamnosus GG biofilms, Electrochimica Acta., 296, 999-1008(2019).
36. D. Zhong, X. Liao, Y. Liu, N. Zhong, Y. Xu, Enhanced electricity generation performance and dye wastewater degradation of microbial fuel cell by using a petaline NiO@ polyaniline-carbon felt anode, Bioresource technology., 258, 125-134(2018).
37. S. Phonsa, P. Sreearunothai, S. Charojrochkul, K. Sombatmankhong, Electrodeposition of MnO2 on polypyrrolecoated stainless steel to enhance electrochemical activities in microbial fuel cells, Solid State Ionics., 316, 125-134(2018).
38. M. Gao, X. Liu, M. Irfan, J. Shi, X. Wang, P. Zhang, Nickle-cobalt composite catalyst-modified activated carbon anode for direct glucose alkaline fuel cell, International Journal of Hydrogen Energy., 43(3), 1805-1815(2018).
39. X. Ying, D. Shen, M. Wang, H. Feng, Y. Gu, W. Chen, Titanium dioxide thin film-modified stainless steel mesh for enhanced current-generation in microbial fuel cells, Chemical Engineering Journal., 333, 260-267(2018).
40. J. L. Varanasi, A. K. Nayak, Y. Sohn, D. Pradhan, D. Das, Improvement of power generation of microbial fuel cell by integrating tungsten oxide electrocatalyst with pure or mixed culture biocatalysts, Electrochimica Acta., 199, 154-163(2016).
41. L. Zeng, W. Zhang, P. Xia, W. Tu, C. Ye, M. He, Porous Ni0. 1Mn0. 9O1. 45 microellipsoids as high-performance anode electrocatalyst for microbial fuel cells, Biosensors and Bioelectronics., 102, 351-356(2018).
42. E. Taşkan, S. Bulak, B. Taşkan, M. Şaşmaz, S. El Abed, A. El Abed, Nitinol as a suitable anode material for electricity generation in microbial fuel cells, Bioelectrochemistry., 128, 118-125(2019).
43. R. Rani, D. Sharma, S. Kumar, Optimization of operating conditions of miniaturize single chambered microbial fuel cell using NiWO4/graphene oxide modified anode for performance improvement and microbial communities dynamics, Bioresource technology., 285, 121337(2019).
44. K.-B. Pu, Q. Ma, W.-F. Cai, Q.-Y. Chen, Y.-H. Wang, F.-J. Li, Polypyrrole modified stainless steel as high performance anode of microbial fuel cell, Biochemical engineering journal., 132, 255-261(2018).
45. A. J. Slate, K. A. Whitehead, D. A. Brownson, C. E. Banks, Microbial fuel cells: An overview of current technology, Renewable and sustainable energy reviews., 101, 60-81(2019).
46. E. Antolini, Nitrogen-doped carbons by sustainable N-and C-containing natural resources as nonprecious catalysts and catalyst supports for low temperature fuel cells, Renewable and Sustainable Energy Reviews., 58, 34-51(2016).
47. L. Zhang, W. He, J. Yang, J. Sun, H. Li, B. Han, S. Zhao, Y. Shi, Y. Feng, Z. Tang, Bread-derived 3D macroporous carbon foams as high performance free-standing anode in microbial fuel cells, Biosensors and Bioelectronics., 122, 217-223(2018).
48. T. Cai, M. Huang, Y. Huang, W. Zheng, Enhanced performance of microbial fuel cells by electrospinning carbon nanofibers hybrid carbon nanotubes composite anode, International journal of hydrogen energy., 44(5), 3088-3098(2019).
49. A. ElMekawy, H. M. Hegab, D. Losic, C. P. Saint, D. Pant, Applications of graphene in microbial fuel cells: the gap between promise and reality, Renewable and Sustainable Energy Reviews., 72, 1389-1403(2017).
50. B. Koo, S. P. Jung, Recent Trends of Oxygen Reduction Catalysts in Microbial Fuel Cells: A Review, J Korean Soc Environ Eng., 41(11), 657-675(2019).
51. H. Dong, H. Yu, X. Wang, Catalysis kinetics and porous analysis of rolling activated carbon-PTFE air-cathode in microbial fuel cells, Environmental science & technology., 46(23), 13009-13015(2012).
52. S. Cheng, H. Liu, B. E. Logan, Increased performance of single-chamber microbial fuel cells using an improved cathode structure, Electrochemistry communications., 8(3), 489-494(2006).
53. F. Zhang, S. Cheng, D. Pant, G. Van Bogaert, B. E. Logan, Power generation using an activated carbon and metal mesh cathode in a microbial fuel cell, Electrochemistry Communications., 11(11), 2177-2179(2009).
54. T. Saito, M. D. Merrill, V. J. Watson, B. E. Logan, M. A. Hickner, Investigation of ionic polymer cathode binders for microbial fuel cells, Electrochimica Acta., 55(9), 3398-3403(2010).
55. S. Son, B. Koo, H. Chai, H. V. H. Tran, S. Pandit, S. P. Jung, Comparison of hydrogen production and system performance in a microbial electrolysis cell containing cathodes made of non-platinum catalysts and binders, Journal of Water Process Engineering., 40, 101844(2021).
56. A. Kraytsberg, Y. Ein-Eli, Review of advanced materials for proton exchange membrane fuel cells, Energy & Fuels., 28(12), 7303-7330(2014).
57. W. Yang, W. He, F. Zhang, M. A. Hickner, B. E. Logan, Single-step fabrication using a phase inversion method of poly (vinylidene fluoride)(PVDF) activated carbon air cathodes for microbial fuel cells, Environmental Science & Technology Letters., 1(10), 416-420(2014).
58. R. A. Rozendal, E. Leone, J. Keller, K. Rabaey, Efficient hydrogen peroxide generation from organic matter in a bioelectrochemical system, Electrochemistry Communications., 11(9), 1752-1755(2009).
59. S. G. Peera, T. Maiyalagan, C. Liu, S. Ashmath, T. G. Lee, Z. Jiang, S. Mao, A review on carbon and non-precious metal based cathode catalysts in microbial fuel cells, International Journal of Hydrogen Energy., 46(4), 3056-3089(2021).
60. S. Gouse Peera, K. K. Tintula, A. K. Sahu, S. Shanmugam, P. Sridhar, S. Pitchumani, Catalytic activity of Pt anchored onto graphite nanofiber-poly (3,4-ethylenedioxythiophene) composite toward oxygen reduction reaction in polymer electrolyte fuel cells, Electrochimica Acta., 108, 95-103(2013).
61. S. G. Peera, A. K. Sahu, A. Arunchander, S. D. Bhat, J. Karthikeyan, P. Murugan, Nitrogen and fluorine co-doped graphite nanofibers as high durable oxygen reduction catalyst in acidic media for polymer electrolyte fuel cells, Carbon., 93, 130-142(2015).
62. S. G. Peera, A. Arunchander, A. K. Sahu, Platinum nanoparticles supported on nitrogen and fluorine co-doped graphite nanofibers as an excellent and durable oxygen reduction catalyst for polymer electrolyte fuel cells, Carbon., 107, 667-679(2016).
63. G. P. Shaik, H.-J. Kwon, T. G. Lee, low-cost and sustainable electrocatalyst, Materials Research Bulletin., 128, 110873(2020).
64. S. G. Peera, J. Balamurugan, N. H. Kim, J. H. Lee, Sustainable Synthesis of Co@NC Core Shell Nanostructures from Metal Organic Frameworks via Mechanochemical Coordination Self-Assembly: An Efficient Electrocatalyst for Oxygen Reduction Reaction, Small., 14(19), 1800441(2018).
65. A. Arunchander, S. G. Peera, S. K. Panda, S. Chellammal, A. K. Sahu, Simultaneous co-doping of N and S by a facile in-situ polymerization of 6-N,N-dibutylamine-1,3,5-triazine2,4-dithiol on graphene framework: An efficient and durable oxygen reduction catalyst in alkaline medium, Carbon., 118, 531-544(2017).
66. S. Cheng, H. Liu, B. E. Logan, Power densities using different cathode catalysts (Pt and CoTMPP) and polymer binders (Nafion and PTFE) in single chamber microbial fuel cells, Environmental science & technology., 40(1), 364-369(2006).
67. M. Rahimnejad, A. Adhami, S. Darvari, A. Zirepour, S.-E. Oh, Microbial fuel cell as new technology for bioelectricity generation: A review, Alexandria Engineering Journal., 54(3), 745-756(2015).
68. Y. Zhang, J. Sun, Y. Hu, S. Li, Q. Xu, Bio-cathode materials evaluation in microbial fuel cells: a comparison of graphite felt, International Journal of Hydrogen Energy., 37(22), 16935-16942(2012).
69. S. Samad, K. S. Loh, W. Y. Wong, T. K. Lee, J. Sunarso, S. T. Chong, W. R. W. Daud, Carbon and non-carbon support materials for platinum-based catalysts in fuel cells, international journal of hydrogen energy., 43(16), 7823-7854(2018).
70. B. Erable, N. Duteanu, S. S. Kumar, Y. Feng, M. M. Ghangrekar, K. Scott, Nitric acid activation of graphite granules to increase the performance of the non-catalyzed oxygen reduction reaction (ORR) for MFC applications, Electrochemistry communications., 11(7), 1547-1549(2009).
71. R. T. Khajeh, S. Aber, K. Nofouzi, Efficient improvement of microbial fuel cell performance by the modification of graphite cathode via electrophoretic deposition of CuO/ZnO, Materials Chemistry and Physics., 240, 122208(2020).
72. Y. Yuan, J. Ahmed, S. Kim, Polyaniline/carbon black composite-supported iron phthalocyanine as an oxygen reduction catalyst for microbial fuel cells, Journal of Power Sources., 196(3), 1103-1106(2011).
73. X. Wang, C. Yuan, C. Shao, S. Zhuang, J. Ye, B. Li, Enhancing oxygen reduction reaction by using metal-free nitrogen-doped carbon black as cathode catalysts in microbial fuel cells treating wastewater, Environmental research., 182, 109011(2020).
74. X. Zhang, Q. Wang, X. Xia, W. He, X. Huang, B. E. Logan, Addition of conductive particles to improve the performance of activated carbon air-cathodes in microbial fuel cells, Environmental Science: Water Research & Technology., 3(5), 806-810(2017).
75. B. Koo, H. Kang, T. Nam, E. Kim, S. Son, S. P. Jung, Performance Enhancement of a Microbial Fuel Cell by Physico-chemical Treatments of Activated-Carbon Catalyst of an Air Cathode, Journal of the Korean Society of Urban Environment., 16(4), 431-439(2016).
76. Q. Yang, X. Zhao, J. Yang, B. Zhou, J. Wang, Y. Dong, H. Zhao, Welding assembly of 3D interconnected carbon nanotubes on carbon fiber as the high-performance anode of microbial fuel cells, International Journal of Hydrogen Energy., 44(36), 20304-20311(2019).
77. U. Karra, S. S. Manickam, J. R. McCutcheon, N. Patel, B. Li, Power generation and organics removal from wastewater using activated carbon nanofiber (ACNF) microbial fuel cells (MFCs), International journal of hydrogen energy., 38(3), 1588-1597(2013).
78. L. Deng, M. Zhou, C. Liu, L. Liu, C. Liu, S. Dong, Development of high performance of Co/Fe/N/CNT nanocatalyst for oxygen reduction in microbial fuel cells, Talanta., 81(1-2), 444-448(2010).
79. Y. Zhang, Y. Hu, S. Li, J. Sun, B. Hou, Manganese dioxide-coated carbon nanotubes as an improved cathodic catalyst for oxygen reduction in a microbial fuel cell, Journal of Power Sources., 196(22), 9284-9289(2011).
80. J. C. Wu, W. M. Yan, W. H. Chiang, S. Thangavel, C. H. Wang, C. T. Wang, Innovative multi processed N doped carbon and Fe3O4 cathode for enhanced bioelectro Fenton microbial fuel cell performance, International Journal of Energy Research., 43(13), 7594-7603(2019).
81. C. Zhang, P. Liang, X. Yang, Y. Jiang, Y. Bian, C. Chen, X. Zhang, X. Huang, Binder-free graphene and manganese oxide coated carbon felt anode for high-performance microbial fuel cell, Biosensors and Bioelectronics., 81, 32-38(2016).
82. M. Kannan, Current status, key challenges and its solutions in the design and development of graphene based ORR catalysts for the microbial fuel cell applications, Biosensors and Bioelectronics., 77, 1208-1220(2016).
83. F. Yu, C. Wang, J. Ma, Capacitance-enhanced 3D graphene anode for microbial fuel cell with long-time electricity generation stability, Electrochimica Acta., 259, 1059-1067(2018).
84. L. Zhuang, Y. Yuan, G. Yang, S. Zhou, In situ formation of graphene/biofilm composites for enhanced oxygen reduction in biocathode microbial fuel cells, Electrochemistry Communications., 21, 69-72(2012).
85. J. Liu, Y. Zhang, Y. Li, J. Li, Z. Chen, H. Feng, J. Li, J. Jiang, D. Qian, In situ chemical synthesis of sandwich-structured MnO a-MnO2/graphene nanoflowers and their supercapacitive behavior, Electrochimica Acta., 173, 148-155(2015).
86. P. Pachfule, D. Shinde, M. Majumder, Q. Xu, Fabrication of carbon nanorods and graphene nanoribbons from a metal-organic framework, Nature Chemistry., 8(7), 718-724(2016).
87. L. Tan, S.-J. Li, X.-T. Wu, N. Li, Z.-Q. Liu, Porous Co3O4 decorated nitrogen-doped graphene electrocatalysts for efficient bioelectricity generation in MFCs, International Journal of Hydrogen Energy., 43(22), 10311-10321(2018).
88. A. A. Eissa, S. G. Peera, N. H. Kim, J. H. Lee, g-C3N4 templated synthesis of the Fe3C@NSC electrocatalyst enriched with Fe-Nx active sites for efficient oxygen reduction reaction, Journal of Materials Chemistry A., 7(28), 16920-16936(2019).
89. U. I. Kramm, J. Herranz, N. Larouche, T. M. Arruda, M. Lefevre, F. Jaouen, P. Bogdanoff, S. Fiechter, I. Abs-Wurmbach, S. Mukerjee, Structure of the catalytic sites in Fe/N/C-catalysts for O2-reduction in PEM fuel cells, Physical Chemistry Chemical Physics., 14(33), 11673-11688(2012).
90. Q. Jia, N. Ramaswamy, H. Hafiz, U. Tylus, K. Strickland, G. Wu, B. Barbiellini, A. Bansil, E. F. Holby, P. Zelenay, Experimental observation of redox-induced Fe–N switching behavior as a determinant role for oxygen reduction activity, ACS nano., 9(12), 12496-12505(2015).
91. S. Rojas-Carbonell, C. Santoro, A. Serov, P. Atanassov, Transition metal-nitrogen-carbon catalysts for oxygen reduction reaction in neutral electrolyte, Electrochemistry Communications., 75, 38-42(2017).
92. W. Yang, X. Wang, R. Rossi, B. E. Logan, Low-cost Fe-N-C catalyst derived from Fe (III)-chitosan hydrogel to enhance power production in microbial fuel cells, Chemical Engineering Journal., 380, 122522(2020).
93. B. Koo, S. P. Jung, Improvement of air cathode performance in microbial fuel cells by using catalysts made by binding metal-organic framework and activated carbon through ultrasonication and solution precipitation, Chemical Engineering Journal., 424, 130388(2021).
94. W. Xue, Q. Zhou, F. Li, B. S. Ondon, Zeolitic imidazolate framework-8 (ZIF-8) as robust catalyst for oxygen reduction reaction in microbial fuel cells, Journal of Power Sources., 423, 9-17(2019).
95. S. Venkata Mohan, G. Velvizhi, J. Annie Modestra, S. Srikanth, Microbial fuel cell: Critical factors regulating bio-catalyzed electrochemical process and recent advancements, Renewable and Sustainable Energy Reviews., 40, 779-797(2014).
96. T. Sadhasivam, K. Dhanabalan, S.-H. Roh, T.-H. Kim, K.-W. Park, S. Jung, M. D. Kurkuri, H.-Y. Jung, A comprehensive review on unitized regenerative fuel cells: Crucial challenges and developments, International Journal of Hydrogen Energy., 42(7), 4415-4433(2017).
97. H. Kang, J. Jeong, P. L. Gupta, S. P. Jung, Effects of brush-anode configurations on performance and electrochemistry of microbial fuel cells, international journal of hydrogen energy., 42(45), 27693-27700(2017).
98. Y. Ahn, B. E. Logan, A multi-electrode continuous flow microbial fuel cell with separator electrode assembly design, Applied microbiology and biotechnology., 93(5), 2241-2248(2012).
99. T. Luo, S. Abdu, M. Wessling, Selectivity of ion exchange membranes: A review, Journal of membrane science., 555, 429-454(2018).
100. S. M. Daud, B. H. Kim, M. Ghasemi, W. R. W. Daud, Separators used in microbial electrochemical technologies: Current status and future prospects, Bioresource Technology., 195, 170-179(2015).
101. S. M. Daud, W. R. W. Daud, B. H. Kim, M. R. Somalu, M. H. A. Bakar, A. Muchtar, J. M. Jahim, S. S. Lim, I. S. Chang, Comparison of performance and ionic concentration gradient of two-chamber microbial fuel cell using ceramic membrane (CM) and cation exchange membrane (CEM) as separators, Electrochimica Acta., 259, 365-376(2018).
102. F. Harnisch, U. Schröder, Selectivity versus mobility: separation of anode and cathode in microbial bioelectrochemical systems, ChemSusChem: Chemistry & Sustainability Energy & Materials., 2(10), 921-926(2009).
103. W.-W. Li, G.-P. Sheng, X.-W. Liu, H.-Q. Yu, Recent advances in the separators for microbial fuel cells, Bioresource technology., 102(1), 244-252(2011).
104. M. Buonomenna, J. Bae, Membrane processes and renewable energies, Renewable and Sustainable Energy Reviews., 43, 1343-1398(2015).
105. S. Choi, J. R. Kim, J. Cha, Y. Kim, G. C. Premier, C. Kim, Enhanced power production of a membrane electrode assembly microbial fuel cell (MFC) using a cost effective poly [2, 5-benzimidazole](ABPBI) impregnated non-woven fabric filter, Bioresource technology., 128, 14-21(2013).
106. R. A. Rozendal, T. H. J. A. Sleutels, H. V. Hamelers, C. J. Buisman, Effect of the type of ion exchange membrane on performance, ion transport, and pH in biocatalyzed electrolysis of wastewater, Water Science and Technology., 57(11), 1757-1762(2008).
107. B. Christgen, K. Scott, J. Dolfing, I. M. Head, T. P. Curtis, An evaluation of the performance and economics of membranes and separators in single chamber microbial fuel cells treating domestic wastewater, PLoS One., 10(8), e0136108(2015).
108. C. Abourached, M. J. English, H. Liu, Wastewater treatment by microbial fuel cell (MFC) prior irrigation water reuse, Journal of Cleaner Production., 137, 144-149(2016).
109. Y. Fan, H. Hu, H. Liu, Enhanced Coulombic efficiency and power density of air-cathode microbial fuel cells with an improved cell configuration, Journal of Power Sources., 171(2), 348-354(2007).
110. Y. Park, S. Park, J. Yu, T. Lee, Effects of anode spacing and flow rate on energy recovery of flat-panel air-cathode microbial fuel cells using domestic wastewater, Bioresource technology., 258, 57-63(2018).
111. Y. Park, J. Yu, E. Widyaningsih, T. Lee, Effect of reactor width and HRT on simultaneous removal of organic compounds and nitrogen in flat-type air-cathode microbial fuel cell, Journal of Korean society of environmental engineers., 41(2), 69-75(2019).
112. C. Munoz-Cupa, Y. Hu, C. C. Xu, A. Bassi, An overview of microbial fuel cell usage in wastewater treatment, resource recovery and energy production., Science of the Total Environment, 142429(2020).
113. J. X. Leong, W. R. W. Daud, M. Ghasemi, K. B. Liew, M. Ismail, Ion exchange membranes as separators in microbial fuel cells for bioenergy conversion: A comprehensive review, Renewable and Sustainable Energy Reviews., 28, 575-587(2013).
114. E. Yang, K.-J. Chae, M.-J. Choi, Z. He, I. S. Kim, Critical review of bioelectrochemical systems integrated with membrane-based technologies for desalination, energy self-sufficiency, and high-efficiency water and wastewater treatment, Desalination., 452, 40-67(2019).
115. Q. Xu, L. Wang, C. Li, X. Wang, C. Li, Y. Geng, Study on improvement of the proton conductivity and anti-fouling of proton exchange membrane by doping SGO@ SiO2 in microbial fuel cell applications, International Journal of Hydrogen Energy., 44(29), 15322-15332(2019).
116. S. G. Flimban, S. H. Hassan, M. M. Rahman, S.-E. Oh, The effect of Nafion membrane fouling on the power generation of a microbial fuel cell, international journal of hydrogen energy., 45(25), 13643-13651(2020).
117. W. He, Y. Dong, C. Li, X. Han, G. Liu, J. Liu, Y. Feng, Field tests of cubic-meter scale microbial electrochemical system in a municipal wastewater treatment plant, Water research., 155, 372-380(2019).
118. M. Oliot, S. Galier, H. Roux de Balmann, A. Bergel, Ion transport in microbial fuel cells: Key roles, theory and critical review, Applied Energy., 183, 1682-1704(2016).
119. S. Jung, M. M. Mench, J. M. Regan, Impedance characteristics and polarization behavior of a microbial fuel cell in response to short-term changes in medium pH, Environmental science & technology., 45(20), 9069-9074(2011).
120. B. Koo, S.-M. Lee, S.-E. Oh, E. J. Kim, Y. Hwang, D. Seo, J. Y. Kim, Y. H. Kahng, Y. W. Lee, S.-Y. Chung, Addition of reduced graphene oxide to an activated-carbon cathode increases electrical power generation of a microbial fuel cell by enhancing cathodic performance, Electrochimica Acta., 297, 613-622(2019).
121. T. Nam, H. Kang, S. Pandit, S.-H. Kim, S. Yoon, S. Bae, S. P. Jung, Effects of vertical and horizontal configurations of different numbers of brush anodes on performance and electrochemistry of microbial fuel cells, Journal of Cleaner Production., 277, 124125(2020).
122. T. Nam, S. Son, E. Kim, H. V. H. Tran, B. Koo, H. Chai, J. Kim, S. Pandit, A. Gurung, S.-E. Oh, Improved structures of stainless steel current collector increase power generation of microbial fuel cells by decreasing cathodic charge transfer impedance, Environmental Engineering Research., 23(4), 383-389(2018).
123. B. P. Cario, R. Rossi, K.-Y. Kim, B. E. Logan, Applying the electrode potential slope method as a tool to quantitatively evaluate the performance of individual microbial electrolysis cell components, Bioresource technology., 287, 121418(2019).
124. M. Á. López Zavala, O. I. Gonzalez Pena, H. Cabral Ruelas, C. Delgado Mena, M. Guizani, Use of cyclic voltammetry to describe the electrochemical behavior of a dual-chamber microbial fuel cell, Energies., 12(18), 3532(2019).
125. J. N. Roy, H. R. Luckarift, C. Lau, A. Falase, K. E. Garcia, L. K. Ista, P. Chellamuthu, R. P. Ramasamy, V. Gadhamshetty, G. Wanger, A study of the flavin response by Shewanella cultures in carbon-limited environments, Rsc Advances., 2(26), 10020-10027(2012).
126. K. Fricke, F. Harnisch, U. Schröder, On the use of cyclic voltammetry for the study of anodic electron transfer in microbial fuel cells, Energy & Environmental Science., 1(1), 144-147(2008).
127. Y. Yuan, S. Zhou, N. Xu, L. Zhuang, Electrochemical characterization of anodic biofilms enriched with glucose and acetate in single-chamber microbial fuel cells, Colloids and Surfaces B: Biointerfaces., 82(2), 641-646(2011).
128. Z. He, F. Mansfeld, Exploring the use of electrochemical impedance spectroscopy (EIS) in microbial fuel cell studies, Energy & Environmental Science., 2(2), 215-219(2009).
129. N. Sekar, R. P. Ramasamy, Electrochemical impedance spectroscopy for microbial fuel cell characterization, J. Microb. Biochem. TechnolS, 6(2), (2013).
130. B. E. Logan, D. Call, S. Cheng, H. V. Hamelers, T. H. Sleutels, A. W. Jeremiasse, R. A. Rozendal, Microbial electrolysis cells for high yield hydrogen gas production from organic matter, Environmental science & technology., 42(23), 8630-8640(2008).
131. D. Call, B. E. Logan, Hydrogen production in a single chamber microbial electrolysis cell lacking a membrane, Environmental science & technology., 42(9), 3401-3406(2008).
132. P. S. Jana, M. Behera, M. Ghangrekar, Performance comparison of up-flow microbial fuel cells fabricated using proton exchange membrane and earthen cylinder, International Journal of Hydrogen Energy., 35(11), 5681-5686(2010).
133. J. Choi, Y. Ahn, Effect of hydrogen producing mixed culture on performance of microbial fuel cells, International journal of hydrogen energy., 39(17), 9482-9489(2014).
134. J. L. Varanasi, S. Roy, S. Pandit, D. Das, Improvement of energy recovery from cellobiose by thermophillic dark fermentative hydrogen production followed by microbial fuel cell, international journal of hydrogen energy., 40(26), 8311-8321(2015).
135. M. Li, K. Lv, S. Wu, S. Chen, Immobilization of Anodophilic Biofilms for Use in Aerotolerant Bioanodes of Microbial Fuel Cells, ACS applied materials & interfaces., 8(51), 34985-34990(2016).
136. Z. Ge, J. Li, L. Xiao, Y. Tong, Z. He, Recovery of electrical energy in microbial fuel cells: brief review, Environmental Science & Technology Letters., 1(2), 137-141(2014).
137. J. Öijerholm, S. Forsberg, H. Hermansson, M. Ullberg, Relation Between the SHE and the Internal Ag∕ AgCl Reference Electrode at High Temperatures, Journal of the Electrochemical Society., 156(3), P56(2009).
138. A. Bard, R. Parsons, J. Jordan, Standard potentials in aqueous solution Marcel Dekker, New York(1985).
139. H. J. Kim, H. S. Park, M. S. Hyun, I. S. Chang, M. Kim, B. H. Kim, A mediator-less microbial fuel cell using a metal reducing bacterium, Enzyme and Microbial technology., 30(2), 145-152(2002).
140. G.-C. Gil, I.-S. Chang, B. H. Kim, M. Kim, J.-K. Jang, H. S. Park, H. J. Kim, Operational parameters affecting the performannce of a mediator-less microbial fuel cell, Biosensors and Bioelectronics., 18(4), 327-334(2003).
141. D. H. Park, J. G. Zeikus, Improved fuel cell and electrode designs for producing electricity from microbial degradation, Biotechnology and bioengineering., 81(3), 348-355(2003).
142. H. Liu, B. E. Logan, Electricity generation using an air-cathode single chamber microbial fuel cell in the presence and absence of a proton exchange membrane, Environmental science & technology., 38(14), 4040-4046(2004).
143. Z. He, S. D. Minteer, L. T. Angenent, Electricity generation from artificial wastewater using an upflow microbial fuel cell, Environmental science & technology., 39(14), 5262-5267(2005).
144. H. Liu, S. Cheng, B. E. Logan, Power generation in fed-batch microbial fuel cells as a function of ionic strength, temperature, and reactor configuration, Environmental science & technology., 39(14), 5488-5493(2005).
145. Z. He, L. T. Angenent, Application of bacterial biocathodes in microbial fuel cells, Electroanalysis: An International Journal Devoted to Fundamental and Practical Aspects of Electroanalysis., 18(19 20), 2009-2015(2006).
146. P. Aelterman, K. Rabaey, H. T. Pham, N. Boon, W. Verstraete, Continuous electricity generation at high voltages and currents using stacked microbial fuel cells, Environmental science & technology., 40(10), 3388-3394(2006).
147. B. Logan, S. Cheng, V. Watson, G. Estadt, Graphite fiber brush anodes for increased power production in air-cathode microbial fuel cells, Environmental science & technology., 41(9), 3341-3346(2007).
148. S. You, Q. Zhao, J. Zhang, J. Jiang, C. Wan, M. Du, S. Zhao, A graphite-granule membrane-less tubular air-cathode microbial fuel cell for power generation under continuously operational conditions, Journal of Power Sources., 173(1), 172-177(2007).
149. Y. Qiao, C. M. Li, S.-J. Bao, Q.-L. Bao, Carbon nanotube/polyaniline composite as anode material for microbial fuel cells, Journal of Power Sources., 170(1), 79-84(2007).
150. S. Cheng, B. E. Logan, Ammonia treatment of carbon cloth anodes to enhance power generation of microbial fuel cells, Electrochemistry Communications., 9(3), 492-496(2007).
151. D. Pant, A. Singh, G. Van Bogaert, S. I. Olsen, P. S. Nigam, L. Diels, K. Vanbroekhoven, Bioelectrochemical systems (BES) for sustainable energy production and product recovery from organic wastes and industrial wastewaters, Rsc Advances., 2(4), 1248-1263(2012).
152. Y. Fan, H. Hu, H. Liu, Sustainable power generation in microbial fuel cells using bicarbonate buffer and proton transfer mechanisms, Environmental science & technology., 41(23), 8154-8158(2007).
153. H. Tang, S. Cai, S. Xie, Z. Wang, Y. Tong, M. Pan, X. Lu, Metal–organic framework derived dual metal and nitrogen doped carbon as efficient and robust oxygen reduction reaction catalysts for microbial fuel cells, Advanced science., 3(2), 1500265(2016).
154. Y. Wang, C. He, W. Li, W. Zong, Z. Li, L. Yuan, G. Wang, Y. Mu, High power generation in mixed-culture microbial fuel cells with corncob-derived three-dimensional N-doped bioanodes and the impact of N dopant states, Chemical Engineering Journal., 399, 125848(2020).
155. S. Pandit, N. Savla, S. P. Jung, Recent advancements in scaling up microbial fuel cells, Integrated Microbial Fuel Cells for Wastewater Treatment., 349-368(2020).
156. I. Ieropoulos, J. Greenman, C. Melhuish, Improved energy output levels from small-scale microbial fuel cells, Bioelectrochemistry., 78(1), 44-50(2010).
157. A. Dewan, H. Beyenal, Z. Lewandowski, Scaling up microbial fuel cells, Environmental science & technology., 42(20), 7643-7648(2008).
158. P. Clauwaert, P. Aelterman, L. De Schamphelaire, M. Carballa, K. Rabaey, W. Verstraete, Minimizing losses in bio-electrochemical systems: the road to applications, Applied microbiology and biotechnology., 79(6), 901-913(2008).
159. X. A. Walter, C. Santoro, J. Greenman, I. A. Ieropoulos, Scalability and stacking of self-stratifying microbial fuel cells treating urine, Bioelectrochemistry., 133, 107491(2020).
160. Y. Feng, W. He, J. Liu, X. Wang, Y. Qu, N. Ren, A horizontal plug flow and stackable pilot microbial fuel cell for municipal wastewater treatment, Bioresource technology., 156, 132-138(2014).
161. B. E. Logan, M. J. Wallack, K.-Y. Kim, W. He, Y. Feng, P. E. Saikaly, Assessment of Microbial Fuel Cell Configurations and Power Densities, Environmental Science & Technology Letters., 2(8), 206-214(2015).
162. F. Qian, M. Baum, Q. Gu, D. E. Morse, A 1.5 µL microbial fuel cell for on-chip bioelectricity generation, Lab on a Chip., 9(21), 3076-3081(2009).
163. A. Dekker, A. T. Heijne, M. Saakes, H. V. Hamelers, C. J. Buisman, Analysis and improvement of a scaled-up and stacked microbial fuel cell, Environmental science & technology., 43(23), 9038-9042(2009).
164. B. Koo, S.-M. Lee, S.-E. Oh, E. J. Kim, Y. Hwang, D. Seo, J. Y. Kim, Y. H. Kahng, Y. W. Lee, S.-Y. Chung, S.-J. Kim, J. H. Park, S. P. Jung, Addition of reduced graphene oxide to an activated-carbon cathode increases electrical power generation of a microbial fuel cell by enhancing cathodic performance, Electrochimica Acta., 297, 613-622(2019).
165. Z. Ge, F. Zhang, J. Grimaud, J. Hurst, Z. He, Long-term investigation of microbial fuel cells treating primary sludge or digested sludge, Bioresource Technology., 136, 509-514(2013).
166. K. Guo, A. Prévoteau, K. Rabaey, A novel tubular microbial electrolysis cell for high rate hydrogen production, Journal of Power Sources., 356, 484-490(2017).
167. S. Cheng, B. E. Logan, Increasing power generation for scaling up single-chamber air cathode microbial fuel cells, Bioresource technology., 102(6), 4468-4473(2011).
168. S. J. Robertson, M. Grattieri, J. Behring, M. Bestetti, S. D. Minteer, Transitioning from batch to flow hypersaline microbial fuel cells, Electrochimica Acta., 317, 494-501(2019).
169. B.-M. An, S.-j. Seo, S. Hidayat, J.-Y. Park, Treatment of ethanolamine and electricity generation using a scaled-up single-chamber microbial fuel cell, Journal of Industrial and Engineering Chemistry., 81, 1-6(2020).
170. K. Bonyoung, P. J. Sokhee, Characterization of Impedance and Polarization of Carbon-Felt Bioanodes and Activated-Carbon Cathodes in a Continuous-Flow Microbial Fuel Cell, Journal of the Korean Society of Urban Environment., 18(2), 177-191(2018).
171. L. Caizán-Juanarena, I. Servin-Balderas, X. Chen, C. J. Buisman, A. ter Heijne, Electrochemical and microbiological characterization of single carbon granules in a multi-anode microbial fuel cell, Journal of Power Sources., 435, 126514(2019).
172. Y. Liu, X. Sun, D. Yin, L. Cai, L. Zhang, Suspended anode-type microbial fuel cells for enhanced electricity generation, RSC Advances., 10(17), 9868-9877(2020).
173. J. V. Boas, V. Oliveira, L. Marcon, M. Simões, A. Pinto, Optimization of a single chamber microbial fuel cell using Lactobacillus pentosus: Influence of design and operating parameters, Science of The Total Environment., 648, 263-270(2019).
174. R. Rossi, D. Jones, J. Myung, E. Zikmund, W. Yang, Y. A. Gallego, D. Pant, P. J. Evans, M. A. Page, D. M. Cropek, Evaluating a multi-panel air cathode through electrochemical and biotic tests, Water research., 148, 51-59(2019).
175. R. Rossi, P. J. Evans, B. E. Logan, Impact of flow recirculation and anode dimensions on performance of a large scale microbial fuel cell, Journal of power sources., 412, 294-300(2019).
176. Y. Dong, W. He, C. Li, D. Liang, Y. Qu, X. Han, Y. Feng, Performance of integrated bioelectrochemical membrane reactor: Energy recovery, pollutant removal and membrane fouling alleviation, Journal of Power Sources., 384, 178-186(2018).
177. C. Li, W. He, D. Liang, Y. Tian, R. S. Yadav, D. Li, J. Liu, Y. Feng, The anaerobic and starving treatment eliminates filamentous bulking and recovers biocathode biocatalytic activity with residual organic loading in microbial electrochemical system, Chemical Engineering Journal., 404, 127072(2021).
178. I. A. Ieropoulos, A. Stinchcombe, I. Gajda, S. Forbes, I. Merino-Jimenez, G. Pasternak, D. Sanchez-Herranz, J. Greenman, Pee power urinal–microbial fuel cell technology field trials in the context of sanitation, Environmental Science: Water Research & Technology., 2(2), 336-343(2016).
179. J. Niu, Y. Feng, N. Wang, S. Liu, Y. Liang, J. Liu, W. He, Effects of high ammonia loading and in-situ short-cut nitrification in low carbon nitrogen ratio wastewater treatment by biocathode microbial electrochemical system, Science of The Total Environment., 755, 142641(2021).
180. H. Wang, Z. Miao, Y. Li, W. He, Y. Qu, Y. Feng, Energetically self-sustaining treatment of swine wastewater in a microbial electrochemical technology-centered hybrid system, Environmental Science: Water Research & Technology., 6(3), 747-756(2020).
181. S. Liu, Y. Feng, J. Niu, J. Liu, N. Li, W. He, A novel single chamber vertical baffle flow biocathode microbial electrochemical system with microbial separator, Bioresource technology., 294, 122236(2019).
182. I. Ieropoulos, J. Greenman, C. Melhuish, Microbial fuel cells based on carbon veil electrodes: Stack configuration and scalability, International Journal of Energy Research., 32(13), 1228-1240(2008).
183. Z. Liu, J. Liu, S. Zhang, Z. Su, A novel configuration of microbial fuel cell stack bridged internally through an extra cation exchange membrane, Biotechnology Letters., 30(6), 1017-1023(2008).
184. L. Zhuang, Y. Zheng, S. Zhou, Y. Yuan, H. Yuan, Y. Chen, Scalable microbial fuel cell (MFC) stack for continuous real wastewater treatment, Bioresource technology., 106, 82-88(2012).
185. L. Zhuang, Y. Yuan, Y. Wang, S. Zhou, Long-term evaluation of a 10-liter serpentine-type microbial fuel cell stack treating brewery wastewater, Bioresource Technology., 123, 406-412(2012).
186. I. Gajda, O. Obata, M. Jose Salar-Garcia, J. Greenman, I. A. Ieropoulos, Long-term bio-power of ceramic microbial fuel cells in individual and stacked configurations, Bioelectrochemistry., 133, 107459(2020).
187. I. Gajda, J. Greenman, I. Ieropoulos, Microbial Fuel Cell stack performance enhancement through carbon veil anode modification with activated carbon powder, Applied Energy., 262, 114475(2020).
188. M. Oliot, L. Etcheverry, R. Mosdale, A. Bergel, Microbial fuel cells connected in series in a common electrolyte underperform: Understanding why and in what context such a set-up can be applied, Electrochimica Acta., 246, 879-889(2017).
189. Y. Park, S. Park, V. K. Nguyen, J. Yu, C. I. Torres, B. E. Rittmann, T. Lee, Complete nitrogen removal by simultaneous nitrification and denitrification in flat-panel air-cathode microbial fuel cells treating domestic wastewater, Chemical Engineering Journal., 316, 673-679(2017).
190. M. Oliot, L. Etcheverry, A. Mosdale, R. Basseguy, M. L. Délia, A. Bergel, Separator electrode assembly (SEA) with 3-dimensional bioanode and removable air-cathode boosts microbial fuel cell performance, Journal of Power Sources., 356, 389-399(2017).
191. J. An, N. Li, L. Wan, L. Zhou, Q. Du, T. Li, X. Wang, Electric field induced salt precipitation into activated carbon air-cathode causes power decay in microbial fuel cells, Water Research., 123, 369-377(2017).
192. I. Gajda, J. Greenman, C. Melhuish, I. A. Ieropoulos, Electricity and disinfectant production from wastewater: Microbial Fuel Cell as a self-powered electrolyser, Scientific Reports., 6(1), 25571(2016).
193. I. Gajda, J. Greenman, C. Melhuish, I. Ieropoulos, Simultaneous electricity generation and microbially-assisted electrosynthesis in ceramic MFCs, Bioelectrochemistry., 104, 58-64(2015).
194. K. Scott, C. Murano, G. Rimbu, A tubular microbial fuel cell, Journal of Applied Electrochemistry., 37(9), 1063-1068(2007).
195. M. Kadivarian, A. A. Dadkhah, M. Nasr Esfahany, Oily wastewater treatment by a continuous flow microbial fuel cell and packages of cells with serial and parallel flow connections, Bioelectrochemistry., 134, 107535(2020).
196. M. Blatter, L. Delabays, C. Furrer, G. Huguenin, C. P. Cachelin, F. Fischer, Stretched 1000-L microbial fuel cell, Journal of Power Sources., 483, 229130(2021).
197. P. Liang, R. Duan, Y. Jiang, X. Zhang, Y. Qiu, X. Huang, One-year operation of 1000-L modularized microbial fuel cell for municipal wastewater treatment, Water Research., 141, 1-8(2018).
198. X. A. Walter, I. Merino-Jiménez, J. Greenman, I. Ieropoulos, PEE POWER® urinal II – Urinal scale-up with microbial fuel cell scale-down for improved lighting, Journal of Power Sources., 392, 150-158(2018).
199. Y. Dong, W. He, D. Liang, C. Li, G. Liu, J. Liu, N. Ren, Y. Feng, Operation strategy of cubic-meter scale microbial electrochemistry system in a municipal wastewater treatment plant, Journal of Power Sources., 441, 227124(2019).
200. A. Mohamed, H. M. Zmuda, P. T. Ha, E. R. Coats, H. Beyenal, Large-scale switchable potentiostatically controlled/ microbial fuel cell bioelectrochemical wastewater treatment system, Bioelectrochemistry., 138, 107724(2021).
201. B. E. Logan, Scaling up microbial fuel cells and other bioelectrochemical systems, Applied Microbiology and Biotechnology., 85(6), 1665-1671(2010).
202. H. Hiegemann, D. Herzer, E. Nettmann, M. Lübken, P. Schulte, K.-G. Schmelz, S. Gredigk-Hoffmann, M. Wichern, An integrated 45L pilot microbial fuel cell system at a full-scale wastewater treatment plant, Bioresource Technology., 218, 115-122(2016).
203. S. Wu, H. Li, X. Zhou, P. Liang, X. Zhang, Y. Jiang, X. Huang, A novel pilot-scale stacked microbial fuel cell for efficient electricity generation and wastewater treatment, Water Research., 98, 396-403(2016).
204. Y. Dong, Y. Qu, W. He, Y. Du, J. Liu, X. Han, Y. Feng, A 90-liter stackable baffled microbial fuel cell for brewery wastewater treatment based on energy self-sufficient mode, Bioresource Technology., 195, 66-72(2015).
205. E. Cho, D. H. Han, J. Ha, Energy Efficiency Evaluation of Publicly Owned Wastewater Utilities, Journal of Environmental Policy., 11(4), 85-105(2012).
206. K. E. Institute, Construction Technology Digital Library, http://218.49.22.39/viewDtlConRpt.do?pMetaCode=OTKCRK200662&gubun=rpt(2019).
207. C. Tang, Y. Zhao, C. Kang, Y. Yang, D. Morgan, L. Xu, Towards concurrent pollutants removal and high energy harvesting in a pilot-scale CW-MFC: Insight into the cathode conditions and electrodes connection, Chemical Engineering Journal., 373, 150-160(2019).
208. P. Srivastava, R. Abbassi, V. Garaniya, T. Lewis, A. K. Yadav, Performance of pilot-scale horizontal subsurface flow constructed wetland coupled with a microbial fuel cell for treating wastewater, Journal of Water Process Engineering., 33, 100994(2020).
209. P. Srivastava, A. K. Yadav, V. Garaniya, R. Abbassi, Chapter 6.3 - Constructed Wetland Coupled Microbial Fuel Cell Technology: Development and Potential Applications, Microbial Electrochemical Technology., 1021-1036(2019).
210. O. Guadarrama-Pérez, T. Gutiérrez-Macías, L. García-Sánchez, V. H. Guadarrama-Pérez, E. B. Estrada-Arriaga, Recent advances in constructed wetland-microbial fuel cells for simultaneous bioelectricity production and wastewater treatment: A review, International Journal of Energy Research., 43(10), 5106-5127(2019).
211. T. Gazali, M. A. Moqsud, Evaluation of Scale-Up And Environmental Factors On Microbial Fuel Cell, International Journal on Advanced Science, Engineering and Information Technology., 9, 861(2019).
212. M. Li, S. Zhou, Y. Xu, Z. Liu, F. Ma, L. Zhi, X. Zhou, Simultaneous Cr (VI) reduction and bioelectricity generation in a dual chamber microbial fuel cell, Chemical Engineering Journal., 334, 1621-1629(2018).
213. A. Singh, A. Kaushik, Removal of Cd and Ni with enhanced energy generation using biocathode microbial fuel cell: Insights from molecular characterization of biofilm communities, Journal of Cleaner Production, 12794(2021).
214. H.-C. Tao, M. Liang, W. Li, L.-J. Zhang, J.-R. Ni, W.-M. Wu, Removal of copper from aqueous solution by electrodeposition in cathode chamber of microbial fuel cell, Journal of hazardous materials., 189(1-2), 186-192(2011).
215. A.-J. Wang, H.-C. Wang, H.-Y. Cheng, B. Liang, W.-Z. Liu, J.-L. Han, B. Zhang, S.-S. Wang, Electrochemistry-stimulated environmental bioremediation: Development of applicable modular electrode and system scale-up, Environmental Science and Ecotechnology., 3, 100050(2020).
216. C. I. Torres, R. Krajmalnik-Brown, P. Parameswaran, A. K. Marcus, G. Wanger, Y. A. Gorby, B. E. Rittmann, Selecting anode-respiring bacteria based on anode potential: phylogenetic, electrochemical, and microscopic characterization, Environmental science & technology., 43(24), 9519-9524(2009).
217. C. Santoro, A. Serov, R. Gokhale, S. Rojas-Carbonell, L. Stariha, J. Gordon, K. Artyushkova, P. Atanassov, A family of Fe-NC oxygen reduction electrocatalysts for microbial fuel cell (MFC) application: relationships between surface chemistry and performances, Applied Catalysis B: Environmental., 205, 24-33(2017).
218. C. Li, W. He, D. Liang, Y. Tian, D. Li, Y. Yu, Y. Feng, The operation characters of biocathode microbial electrochemical system with microbial separator for domestic wastewater treatment: Power generation, long-term stability, and organic removal, Journal of Power Sources., 495, 229785(2021).
219. J. Sun, Y.-y. Hu, Z. Bi, Y.-q. Cao, Simultaneous decolorization of azo dye and bioelectricity generation using a microfiltration membrane air-cathode single-chamber microbial fuel cell, Bioresource Technology., 100(13), 3185-3192(2009).
220. C. Li, W. He, D. Liang, Y. Tian, R. S. Yadav, J. Liu, Y. Feng, Power density of microbial electrochemical system responds to mass transfer characters of non–ion–selective microbial separator, Bioresource Technology., 311, 123478(2020).
221. T. Tommasi, G. Lombardelli, Energy sustainability of Microbial Fuel Cell (MFC): A case study, Journal of Power Sources., 356, 438-447(2017).
222. H. Hiegemann, T. Littfinski, S. Krimmler, M. Lübken, D. Klein, K.-G. Schmelz, K. Ooms, D. Pant, M. Wichern, Performance and inorganic fouling of a submergible 255 L prototype microbial fuel cell module during continuous long-term operation with real municipal wastewater under practical conditions, Bioresource technology., 294, 122227(2019).
223. S.-E. Oh, B. E. Logan, Voltage reversal during microbial fuel cell stack operation, Journal of Power Sources., 167(1), 11-17(2007).
224. B. Kim, S. V. Mohan, D. Fapyane, I. S. Chang, Controlling voltage reversal in microbial fuel cells, Trends in biotechnology., 38(6), 667-678(2020).
225. J. An, J. Nam, B. Kim, H.-S. Lee, B. H. Kim, I. S. Chang, Performance variation according to anode-embedded orientation in a sediment microbial fuel cell employing a chessboard-like hundred-piece anode, Bioresource technology., 190, 175-181(2015).
226. S. Chen, S. A. Patil, R. K. Brown, U. Schröder, Strategies for optimizing the power output of microbial fuel cells: transitioning from fundamental studies to practical implementation, Applied energy., 233, 15-28(2019).
227. Y. Song, J. An, K. J. Chae, Effect of temperature variation on the performance of microbial fuel cells, Energy Technology., 5(12), 2163-2167(2017).
228. P. Kumar, A. K. Mungray, Microbial fuel cell: optimizing pH of anolyte and catholyte by using taguchi method, Environmental Progress & Sustainable Energy., 36(1), 120-128(2017).
229. Y. Ye, H. H. Ngo, W. Guo, S. W. Chang, D. D. Nguyen, Y. Liu, L. D. Nghiem, X. Zhang, J. Wang, Effect of organic loading rate on the recovery of nutrients and energy in a dual-chamber microbial fuel cell, Bioresource technology., 281, 367-373(2019).
230. F. Guo, H. Luo, Z. Shi, Y. Wu, H. Liu, Substrate salinity: A critical factor regulating the performance of microbial fuel cells, a review., Science of The Total Environment, 143021(2020).
231. A. Stefanova, A. Angelov, S. Bratkova, P. Genova, K. Nikolova, Influence of electrical conductivity and temperature in a microbial fuel cell for treatment of mining waste water, Annals of the Constantin Brâncuși University of Târgu Jiu, Letters and Social Science Series., (2018).
232. F. Vicari, S. Mateo, F. Fernandez-Morales, P. Cañizares, A. Galia, O. Scialdone, M. Rodrigo, Influence of the methodology of inoculation in the performance of air-breathing microbial fuel cells, Journal of Electroanalytical Chemistry., 803, 81-88(2017).
233. Y. Ye, H. H. Ngo, W. Guo, S. W. Chang, D. D. Nguyen, X. Zhang, S. Zhang, G. Luo, Y. Liu, Impacts of hydraulic retention time on a continuous flow mode dual-chamber microbial fuel cell for recovering nutrients from municipal wastewater, Science of The Total Environment., 734, 139220(2020).
234. S. Huang, J. Zhang, J. Pi, L. Gong, G. Zhu, Long-term electricity generation and denitrification performance of MFCs with different exchange membranes and electrode materials, Bioelectrochemistry., 140, 107748(2021).
235. Z. Ge, Z. He, Long-term performance of a 200 liter modularized microbial fuel cell system treating municipal wastewater: treatment, energy, cost, Environmental Science: Water Research & Technology., 2(2), 274-281(2016).
236. E. Zhang, F. Wang, Q. Yu, K. Scott, X. Wang, G. Diao, Durability and regeneration of activated carbon air-cathodes in long-term operated microbial fuel cells, Journal of Power Sources., 360, 21-27(2017).
237. R. Valladares Linares, J. Domínguez-Maldonado, E. Rodríguez-Leal, G. Patrón, A. Castillo-Hernández, A. Miranda, D. Diaz Romero, R. Moreno-Cervera, G. Camara-chale, C. G. Borroto, Scale up of microbial fuel cell stack system for residential wastewater treatment in continuous mode operation, Water., 11(2), 217(2019).
238. B. Zhang, H. Zhao, S. Zhou, C. Shi, C. Wang, J. Ni, A novel UASB–MFC–BAF integrated system for high strength molasses wastewater treatment and bioelectricity generation, Bioresource Technology., 100(23), 5687-5693(2009).
239. Y. Ahn, B. E. Logan, Effectiveness of domestic wastewater treatment using microbial fuel cells at ambient and mesophilic temperatures, Bioresource technology., 101(2), 469-475(2010).
240. S. i. Ishii, K. Watanabe, S. Yabuki, B. E. Logan, Y. Sekiguchi, Comparison of electrode reduction activities of Geobacter sulfurreducens and an enriched consortium in an air-cathode microbial fuel cell, Applied and environmental microbiology., 74(23), 7348-7355(2008).
241. J. R. Kim, S. H. Jung, J. M. Regan, B. E. Logan, Electricity generation and microbial community analysis of alcohol powered microbial fuel cells, Bioresource technology., 98(13), 2568-2577(2007).
242. A. A. Yaqoob, M. N. M. Ibrahim, C. Guerrero-Barajas, Modern trend of anodes in microbial fuel cells (MFCs): an overview, Environmental Technology & Innovation., 101579(2021).
243. Y. Yuan, S. Zhou, Y. Liu, J. Tang, Nanostructured macroporous bioanode based on polyaniline-modified natural loofah sponge for high-performance microbial fuel cells, Environmental science & technology., 47(24), 14525-14532(2013).
244. J. Zhang, J. Li, D. Ye, X. Zhu, Q. Liao, B. Zhang, Tubular bamboo charcoal for anode in microbial fuel cells, Journal of Power Sources., 272, 277-282(2014).
245. H. Zhu, H. Wang, Y. Li, W. Bao, Z. Fang, C. Preston, O. Vaaland, Z. Ren, L. Hu, Lightweight, conductive hollow fibers from nature as sustainable electrode materials for microbial energy harvesting, Nano Energy., 10, 268-276(2014).
246. Y. Yuan, T. Liu, P. Fu, J. Tang, S. Zhou, Conversion of sewage sludge into high-performance bifunctional electrode materials for microbial energy harvesting, Journal of Materials Chemistry A., 3(16), 8475-8482(2015).
247. S. Chen, J. Tang, X. Jing, Y. Liu, Y. Yuan, S. Zhou, A hierarchically structured urchin-like anode derived from chestnut shells for microbial energy harvesting, Electrochimica Acta., 212, 883-889(2016).
248. X. Ma, C. Feng, W. Zhou, H. Yu, Municipal sludge-derived carbon anode with nitrogen-and oxygen-containing functional groups for high-performance microbial fuel cells, Journal of Power Sources., 307, 105-111(2016).
249. H. Feng, Y. Jia, D. Shen, Y. Zhou, T. Chen, W. Chen, Z. Ge, S. Zheng, M. Wang, The effect of chemical vapor deposition temperature on the performance of binder-free sewage sludge-derived anodes in microbial fuel cells, Science of The Total Environment., 635, 45-52(2018).
250. H. Yuan, G. Dong, D. Li, L. Deng, P. Cheng, Y. Chen, Steamed cake-derived 3D carbon foam with surface anchored carbon nanoparticles as freestanding anodes for high-performance microbial fuel cells, Science of the Total Environment., 636, 1081-1088(2018).
251. L. Zeng, S. Zhao, M. He, Macroscale porous carbonized polydopamine-modified cotton textile for application as electrode in microbial fuel cells, Journal of Power Sources., 376, 33-40(2018).
252. N. Senthilkumar, M. Pannipara, A. G. Al-Sehemi, PEDOT/NiFe2O4 nanocomposites on biochar as a free-standing anode for high-performance and durable microbial fuel cells, New Journal of Chemistry., 43(20), 7743-7750(2019).
253. Y.-H. Hung, T.-Y. Liu, H.-Y. Chen, Renewable coffee waste-derived porous carbons as anode materials for high-performance sustainable microbial fuel cells, ACS Sustainable Chemistry & Engineering., 7(20), 16991-16999(2019).
254. A. Mehdinia, E. Ziaei, A. Jabbari, Facile microwave-assisted synthesized reduced graphene oxide/tin oxide nanocomposite and using as anode material of microbial fuel cell to improve power generation, International journal of hydrogen energy., 39(20), 10724-10730(2014).
255. X. Y. Wu, F. Tong, T. S. Song, X. Y. Gao, J. J. Xie, C. C. Zhou, L. X. Zhang, P. Wei, Effect of zeolite coated anode on the performance of microbial fuel cells, Journal of Chemical Technology & Biotechnology., 90(1), 87-92(2015).
256. C. Zhang, P. Liang, Y. Jiang, X. Huang, Enhanced power generation of microbial fuel cell using manganese dioxide-coated anode in flow-through mode, Journal of Power Sources., 273, 580-583(2015).
257. X. Quan, B. Sun, H. Xu, Anode decoration with biogenic Pd nanoparticles improved power generation in microbial fuel cells, Electrochimica Acta., 182, 815-820(2015).
258. L. Huang, X. Li, Y. Ren, X. Wang, In-situ modified carbon cloth with polyaniline/graphene as anode to enhance performance of microbial fuel cell, international journal of hydrogen energy., 41(26), 11369-11379(2016).
259. M. Harshiny, N. Samsudeen, R. J. Kameswara, M. Matheswaran, Biosynthesized FeO nanoparticles coated carbon anode for improving the performance of microbial fuel cell, international journal of hydrogen energy., 42(42), 26488-26495(2017).
260. L. Zou, Z. Lu, Y. Huang, Z.-e. Long, Y. Qiao, Nanoporous Mo2C functionalized 3D carbon architecture anode for boosting flavins mediated interfacial bioelectrocatalysis in microbial fuel cells, Journal of Power Sources., 359, 549-555(2017).
261. H. O. Mohamed, M. A. Abdelkareem, M. Obaid, S.-H. Chae, M. Park, H. Y. Kim, N. A. Barakat, Cobalt oxides-sheathed cobalt nano flakes to improve surface properties of carbonaceous electrodes utilized in microbial fuel cells, Chemical Engineering Journal., 326, 497-506(2017).
262. W. Zhang, B. Xie, L. Yang, D. Liang, Y. Zhu, H. Liu, Brush-like polyaniline nanoarray modified anode for improvement of power output in microbial fuel cell, Bioresource technology., 233, 291-295(2017).
263. H. Xu, X. Quan, Z. Xiao, L. Chen, Effect of anodes decoration with metal and metal oxides nanoparticles on pharmaceutically active compounds removal and power generation in microbial fuel cells, Chemical Engineering Journal., 335, 539-547(2018).
264. J. M. Sonawane, S. Al-Saadi, R. K. Singh Raman, P. C. Ghosh, S. B. Adeloju, high-performance anodes for microbial fuel cells, Electrochimica Acta., 268, 484-493(2018).
265. J. Tang, Y. Yuan, T. Liu, S. Zhou, High-capacity carbon-coated titanium dioxide core–shell nanoparticles modified three dimensional anodes for improved energy output in microbial fuel cells, Journal of Power Sources., 274, 170-176(2015).
266. X. Yang, X. Ma, K. Wang, D. Wu, Z. Lei, C. Feng, Eighteen-month assessment of 3D graphene oxide aerogel-modified 3D graphite fiber brush electrode as a high-performance microbial fuel cell anode, Electrochimica Acta., 210, 846-853(2016).
267. J. Chen, Y. Hu, X. Tan, L. Zhang, W. Huang, J. Sun, Enhanced performance of microbial fuel cell with in situ preparing dual graphene modified bioelectrode, Bioresource Technology., 241, 735-742(2017).
268. Q.-Q. Wang, X.-Y. Wu, Y.-Y. Yu, D.-Z. Sun, H.-H. Jia, Y.-C. Yong, Facile in-situ fabrication of graphene/riboflavin electrode for microbial fuel cells, Electrochimica Acta., 232, 439-444(2017).
269. Y. Cheng, M. Mallavarapu, R. Naidu, Z. Chen, In situ fabrication of green reduced graphene-based biocompatible anode for efficient energy recycle, Chemosphere., 193, 618-624(2018).
270. D. Paul, M. T. Noori, P. P. Rajesh, M. M. Ghangrekar, A. Mitra, Modification of carbon felt anode with graphene oxide-zeolite composite for enhancing the performance of microbial fuel cell, Sustainable Energy Technologies and Assessments., 26, 77-82(2018).
271. X.-Q. Lin, Z.-L. Li, B. Liang, J. Nan, A.-J. Wang, Identification of biofilm formation and exoelectrogenic population structure and function with graphene/polyanliline modified anode in microbial fuel cell, Chemosphere., 219, 358-364(2019).
272. J. Y. Chen, P. Xie, Z. P. Zhang, Reduced graphene oxide/polyacrylamide composite hydrogel scaffold as biocompatible anode for microbial fuel cell, Chemical Engineering Journal., 361, 615-624(2019).
273. Y. Li, J. Liu, X. Chen, X. Yuan, N. Li, W. He, Y. Feng, Enhanced electricity generation and extracellular electron transfer by polydopamine–reduced graphene oxide (PDA–rGO) modification for high-performance anode in microbial fuel cell, Chemical Engineering Journal., 387, 123408(2020).
274. J. R. Kim, J.-Y. Kim, S.-B. Han, K.-W. Park, G. Saratale, S.-E. Oh, Application of Co-naphthalocyanine (CoNPc) as alternative cathode catalyst and support structure for microbial fuel cells, Bioresource technology., 102(1), 342-347(2011).
275. B. Mecheri, A. Iannaci, A. D’Epifanio, A. Mauri, S. Licoccia, Carbon-supported zirconium oxide as a cathode for microbial fuel cell applications, ChemPlusChem., 81(1), 80(2016).
276. M. Ghasemi, W. R. W. Daud, M. Rahimnejad, M. Rezayi, A. Fatemi, Y. Jafari, M. Somalu, A. Manzour, Copper-phthalocyanine and nickel nanoparticles as novel cathode catalysts in microbial fuel cells, International Journal of hydrogen energy., 38(22), 9533-9540(2013).
277. X. Zhang, X. Xia, I. Ivanov, X. Huang, B. E. Logan, Enhanced activated carbon cathode performance for microbial fuel cell by blending carbon black, Environmental science & technology., 48(3), 2075-2081(2014).
278. L. Feng, Y. Chen, L. Chen, Easy-to-operate and low-temperature synthesis of gram-scale nitrogen-doped graphene and its application as cathode catalyst in microbial fuel cells, ACS nano., 5(12), 9611-9618(2011).
279. D. Li, J. Liu, H. Wang, Y. Qu, Y. Feng, Effect of long-term operation on stability and electrochemical response under water pressure for activated carbon cathodes in microbial fuel cells, Chemical Engineering Journal., 299, 314-319(2016).
280. X. Zhang, D. Pant, F. Zhang, J. Liu, W. He, B. E. Logan, Long term performance of chemically and physically modified activated carbons in air cathodes of microbial fuel cells, ChemElectroChem., 1(11), 1859-1866(2014).
281. W. Yang, F. Zhang, W. He, J. Liu, M. A. Hickner, B. E. Logan, Poly (vinylidene fluoride-co-hexafluoropropylene) phase inversion coating as a diffusion layer to enhance the cathode performance in microbial fuel cells, Journal of Power Sources., 269, 379-384(2014).
282. X. Li, X. Wang, Y. Zhang, N. Ding, Q. Zhou, Opening size optimization of metal matrix in rolling-pressed activated carbon air–cathode for microbial fuel cells, Applied Energy., 123, 13-18(2014).
283. L. Xiao, J. Damien, J. Luo, H. D. Jang, J. Huang, Z. He, Crumpled graphene particles for microbial fuel cell electrodes, Journal of Power Sources., 208, 187-192(2012).
284. S. Khilari, S. Pandit, M. Ghangrekar, D. Das, D. Pradhan, Graphene supported α-MnO 2 nanotubes as a cathode catalyst for improved power generation and wastewater treatment in single-chambered microbial fuel cells, Rsc Advances., 3(21), 7902-7911(2013).
285. Z. Yan, M. Wang, Y. Lu, R. Liu, J. Zhao, Ethylene glycol stabilized NaBH 4 reduction for preparation carbon-supported Pt–Co alloy nanoparticles used as oxygen reduction electrocatalysts for microbial fuel cells, Journal of Solid State Electrochemistry., 18(4), 1087-1097(2014).
286. C. J. Kirubaharan, D. J. Yoo, A. R. Kim, Graphene/poly (3, 4-ethylenedioxythiophene)/Fe3O4 nanocomposite–An efficient oxygen reduction catalyst for the continuous electricity production from wastewater treatment microbial fuel cells, International Journal of Hydrogen Energy., 41(30), 13208-13219(2016).
287. Q. Wen, S. Wang, J. Yan, L. Cong, Z. Pan, Y. Ren, Z. Fan, MnO2–graphene hybrid as an alternative cathodic catalyst to platinum in microbial fuel cells, Journal of power sources., 216, 187-191(2012).
288. Z. Yan, M. Wang, B. Huang, J. Zhao, R. Liu, Carboxyl multi-wall carbon nanotubes supported Pt–Ni alloy nanoparticles as cathode catalyst for microbial fuel cells, Int. J. Electrochem. Sci., 7, 10825-10834(2012).
289. N. Zhu, J. Huang, W. Shen, L. Tu, P. Wu, H. Ma, Carboxylic carbon nanotube: Catalyst support material and oxygen reduction reaction of microbial fuel cells, Int. J. Electrochem. Sci., 10, 2634-2645(2015).
290. L. Tan, Z.-Q. Liu, N. Li, J.-Y. Zhang, L. Zhang, S. Chen, CuSe decorated carbon nanotubes as a high performance cathode catalyst for microbial fuel cells, Electrochimica Acta., 213, 283-290(2016).
291. Y.-C. Song, J.-H. Woo, K. Yoo, J.-W. Chung, C.-Y. Lee, Dual layered CNT structure air cathode for power generation from microbial fuel cells, KSCE Journal of Civil Engineering., 17(4), 646-650(2013).
292. X. Shi, Y. Feng, X. Wang, H. Lee, J. Liu, Y. Qu, W. He, S. S. Kumar, N. Ren, Application of nitrogen-doped carbon powders as low-cost and durable cathodic catalyst to air– cathode microbial fuel cells, Bioresource technology., 108, 89-93(2012).
293. L. Feng, L. Yang, Z. Huang, J. Luo, M. Li, D. Wang, Y. Chen, Enhancing electrocatalytic oxygen reduction on nitrogen-doped graphene by active sites implantation, Scientific reports., 3(1), 1-8(2013).
294. Y. Su, Y. Zhu, X. Yang, J. Shen, J. Lu, X. Zhang, J. Chen, C. Li, A highly efficient catalyst toward oxygen reduction reaction in neutral media for microbial fuel cells, Industrial & Engineering Chemistry Research., 52(18), 6076-6082(2013).
295. Y. Ahn, I. Ivanov, T. C. Nagaiah, A. Bordoloi, B. E. Logan, Mesoporous nitrogen-rich carbon materials as cathode catalysts in microbial fuel cells, Journal of Power Sources., 269, 212-215(2014).
296. L. Feng, Y. Yan, Y. Chen, L. Wang, Nitrogen-doped carbon nanotubes as efficient and durable metal-free cathodic catalysts for oxygen reduction in microbial fuel cells, Energy & Environmental Science., 4(5), 1892-1899(2011).
297. G. Yue, K. Meng, Q. Liu, One-step synthesis of N-doped carbon and its application as a cost-efficient catalyst for the oxygen reduction reaction in microbial fuel cells, ChemPlusChem., 80(7), 1133(2015).
298. Q. Wen, S. Wang, J. Yan, L. Cong, Y. Chen, H. Xi, Porous nitrogen-doped carbon nanosheet on graphene as metal-free catalyst for oxygen reduction reaction in air-cathode microbial fuel cells, Bioelectrochemistry., 95, 23-28(2014).
299. Y. Liu, K. Li, Y. Liu, L. Pu, Z. Chen, S. Deng, The high-performance and mechanism of P-doped activated carbon as a catalyst for air-cathode microbial fuel cells, Journal of Materials Chemistry A., 3(42), 21149-21158(2015).
300. H. Yuan, Y. Hou, Z. Wen, X. Guo, J. Chen, Z. He, Porous carbon nanosheets codoped with nitrogen and sulfur for oxygen reduction reaction in microbial fuel cells, ACS applied materials & interfaces., 7(33), 18672-18678(2015).
301. D. L. Hoskins, X. Zhang, M. A. Hickner, B. E. Logan, Spray-on polyvinyl alcohol separators and impact on power production in air-cathode microbial fuel cells with different solution conductivities, Bioresource technology., 172, 156-161(2014).
302. J. Chouler, I. Bentley, F. Vaz, A. O’Fee, P. J. Cameron, M. Di Lorenzo, Exploring the use of cost-effective membrane materials for Microbial Fuel Cell based sensors, Electrochimica Acta., 231, 319-326(2017).
303. H. Ilbeygi, M. Ghasemi, D. Emadzadeh, A. F. Ismail, S. Zaidi, S. A. Aljlil, J. Jaafar, D. Martin, S. Keshani, Power generation and wastewater treatment using a novel SPEEK nanocomposite membrane in a dual chamber microbial fuel cell, International Journal of Hydrogen Energy., 40(1), 477-487(2015).
304. A. Sivasankaran, D. Sangeetha, Y.-H. Ahn, Nanocomposite membranes based on sulfonated polystyrene ethylene butylene polystyrene (SSEBS) and sulfonated SiO2 for microbial fuel cell application, Chemical Engineering Journal., 289, 442-451(2016).
305. S. Ayyaru, S. Dharmalingam, A study of influence on nanocomposite membrane of sulfonated TiO2 and sulfonated polystyrene-ethylene-butylene-polystyrene for microbial fuel cell application, Energy., 88, 202-208(2015).
306. E. Mahendiravarman, D. Sangeetha, Increased microbial fuel cell performance using quaternized poly ether ether ketone anionic membrane electrolyte for electricity generation, International journal of hydrogen energy., 38(5), 2471-2479(2013).
307. M. Elangovan, S. Dharmalingam, Preparation and performance evaluation of poly (ether-imide) based anion exchange polymer membrane electrolyte for microbial fuel cell, International Journal of Hydrogen Energy., 41(20), 8595-8605(2016).
308. M. Elangovan, S. Dharmalingam, A facile modification of a polysulphone based anti biofouling anion exchange membrane for microbial fuel cell application, RSC advances., 6(25), 20571-20581(2016).
309. S. Pandit, A. Sengupta, S. Kale, D. Das, Performance of electron acceptors in catholyte of a two-chambered microbial fuel cell using anion exchange membrane, Bioresource technology., 102(3), 2736-2744(2011).
310. A. E. Inglesby, A. C. Fisher, Downstream application of a microbial fuel cell for energy recovery from an Arthrospira maxima fed anaerobic digester effluent, RSC advances., 3(38), 17387-17394(2013).
311. J. Ma, Z. Wang, D. Suor, S. Liu, J. Li, Z. Wu, Temporal variations of cathode performance in air-cathode single-chamber microbial fuel cells with different separators, Journal of Power Sources., 272, 24-33(2014).
312. I. Satar, W. R. W. Daud, B. H. Kim, M. R. Somalu, M. Ghasemi, M. H. A. Bakar, T. Jafary, S. N. Timmiati, Performance of titanium–nickel (Ti/Ni) and graphite felt-nickel (GF/Ni) electrodeposited by Ni as alternative cathodes for microbial fuel cells, Journal of the Taiwan Institute of Chemical Engineers., 89, 67-76(2018).
313. S. P. Jung, E. Kim, B. Koo, Effects of wire-type and mesh-type anode current collectors on performance and electrochemistry of microbial fuel cells, Chemosphere., 209, 542-550(2018).
314. J. R. Kim, J. Rodríguez, F. R. Hawkes, R. M. Dinsdale, A. J. Guwy, G. C. Premier, Premier, Increasing power recovery and organic removal efficiency using extended longitudinal tubular microbial fuel cell (MFC) reactors, Energy & Environmental Science., 4(2), 459-465(2011).
315. Z. Li, L. Yao, L. Kong, H. Liu, Electricity generation using a baffled microbial fuel cell convenient for stacking, Bioresource Technology., 99(6), 1650-1655(2008).
316. F. Zhang, Z. Ge, J. Grimaud, J. Hurst, Z. He, In situ investigation of tubular microbial fuel cells deployed in an aeration tank at a municipal wastewater treatment plant, Bioresource technology., 136, 316-321(2013).
317. A. Gálvez, J. Greenman, I. Ieropoulos, Landfill leachate treatment with microbial fuel cells; scale-up through plurality, Bioresource technology., 100(21), 5085-5091(2009).
318. P. Liang, M. Fan, X. Cao, X. Huang, Evaluation of applied cathode potential to enhance biocathode in microbial fuel cells, Environmental & Clean Technology., 84(5), 794-799(2009).
319. F. Zhang, Z. Ge, J. Grimaud, J. Hurst, Z. He, Long-term performance of liter-scale microbial fuel cells treating primary effluent installed in a municipal wastewater treatment facility, Environmental science & technology., 47(9), 4941-4948(2013).
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||