The Korean text of this paper can be translated into multiple languages on the website of http://jksee.or.kr through Google Translator.
미생물 고정화 담체를 이용한 충전율 및 질산화․탈질 속도에 관한 연구
Abstract
This study investigated characteristics of nitrification/denitrification rate using PVA (Polyvinyl Alcohol) gel immobilized with specific microorganisms. The media for nitrification and denitrification were producted by immobilizing nitrifying microorganisms (Nitrosomonas europaea and Nitrobacter spp.) and denitrifying microorganisms (Psuedomonas, Bacillus and Paracoccus), respectively. When the media filling rate was the 15% (v/v), the microorganism - immobilized media indicated optimum efficiency. The nitrification rate was 12.53 mg NH4+-N/L·hr and the denitrification rate was 20.37 mg NO3--N/L·hr, which was faster than the conventional reaction rate (nitrification: 3.93 mg NH4+-N/L·hr). In order to confirm microbial immobilization, SEM/EDX (Scanning Electron Microscopy/Energy Dispersive X-ray Analyser) analysis of media before and after immobilization was conducted. It showed that the contents of C and N increased from 58.5% and 3.85% to 70.75% and 7.69%, respectively. These results suggest that application of microorganism immobilized media improves treatment efficiency and can also reduce the size of the treatment facility.
Key words: Microorganism Immobilized Media, Nitrogen Removal, Filling Rate, Nitrification Rate, Denitrification Rate
요약
본 연구는 특정 미생물을 고정화시킨 PVA (Polyvinyl Alcohol) gel을 이용한 질산화ᆞ탈질 반응속도를 분석하였다. 질 산화용 담체는 질산화 미생물인 Nitrosomonas europaea, Nitrobacter spp.를 혼합 배양하여 고정화시켰으며 탈질용 담체는 탈 질 미생물인 Psuedomonas, Bacillus, Paracoccus를 고정화시켰다. 미생물 고정화 담체의 효율을 분석하기 위하여 우선 충전율 결정결과 15% (v/v)이 효과적으로 나타났다. 질산화 반응속도는 12.53 mg NH4+-N/L hr, 탈질 반응속도는 20.37 mg NO3--N/L hr로 기존 반응속도(질산화 : 3.93 mg NH4+-N/L hr)보다 빠르게 나타났다. 미생물의 고정화 여부를 확인하기 위하여 미생물 고정화 전ᆞ후의 담체를 대상으로 SEM/EDX (Scanning Electron Microscopy/Energy Dispersive X-ray Analyser)를 분석한 결과, C와 N의 성분이 각각 58.5%와 3.85%에서 70.75%와 7.69%로 증가하였다. 결론적으로 미생물 고정화 담체를 적용할 경우 높 은 처리효율을 얻을 수 있고 처리시설 규모를 줄일 수 있는 장점을 확인하였다.
주제어: 미생물 고정화 담체, 질소 제거, 충전율, 질산화 속도, 탈질 속도
1. 서 론
국내 폐수처리시설의 방류수 수질기준에서 T-N의 기준은 30 mg/L 이하(수질 및 수생태계 보전에 관한 법률 시행규칙, 청정지역 기준, 2016년 1월 1일부터 적용)이며, 이는 수생태의 부영양화 및 생태독성으로 이어진다[ 1~ 3]. 대부분 질소제거는 생물학적 처리에 의존하고 있으며, 경제적인 측면과 유지관리 측면에서 볼 때 생물학적 처리가 가장 유리하며 법적 수질기준을 준수할 수 있는 안정적인 기술이 개발된다면 폐수처리에 있어 생물학적 처리의 중요성이 더욱 증가될 것이다. 또한 최근 T-N과 관련하여 규제강화와 관련된 논의가 활발히 진행되고 있어[ 4] 향후 방류수 수질기준 중 T-N 기준이 보다 강화될 경우 기존 하수처리 공법으로 기준을 만족시키기 위해서는 체류시간(HRT)을 증가시키는 방법 외에는 방안이 없는 상황이다. 미생물 고정화 담체는 미생물유실이 적어 별도의 고액분리시설(침전지 등)이 불필요하여 처리시설 규모를 줄일 수 있는 장점이 있다. 또한 반응조 내부의 미생물을 고농도로 유지하여 기존 공정보다 빠른 시간에 처리가 가능하고 요구되는 처리수질에 따라 다양한 미생물 고정화 담체를 응용하여 상황에 따라 체류시간 감소(반응조 크기 감소) 등도 기대할 수 있다. 그리고 미생물이 담체 내부에 고정화되어 있어 갑작스런 유입부하의 변동 혹은 독성물질 유입에 따른 미생물 활성에 영향이 적다[ 5]. 따라서 본 연구는 하․폐수처리에 주종을 이루는 Bacillus 속미생물과 질산화 및 탈질 미생물을 고정화한 담체를 자체 제작하고 이를 이용한 질산화와 탈질 효율 및 반응속도를 살펴보았다. 담체공법 적용시 가장 중요한 영향인자인 충전율을 결정하고 질산화 및 탈질 반응속도를 도출하였다. 또한 담체 내부에 미생물의 부착여부를 검토하기 위하여 SEM/EDX 분석을 실시하였다.
2. 연구방법
2.1. 미생물 고정화 담체
본 연구에 사용된 미생물 고정화 담체는 PVA 20%와 PEG 15%를 혼합하여 자체 제작하여 사용하였다. 질산화용 담체는 질산화 미생물인 Nitrosomonas europaea, Nitrobacter spp. + Nitrospira spp.를 혼합 배양하여 고정화시켰으며 탈질용 담체는 탈질 미생물인 Psuedomonas, Bacillus, Paracoccus를 1:1:1로 혼합 배양하여 고정화시켰다.
2.2. 미생물 고정화 담체 충전율 실험
충전율 실험은 다른 인자의 영향을 최소화하기 위하여 인공폐수를 대상으로 진행하였으며 성상은 Table 1에 나타내었다. 이때 미생물 성장에 필요한 미량물질(Na-EDTA 2.5 mg/L, FeSO 4·7H 2O 1.5 mg/L, Na 2MoO 4·2H 2O 1 mg/L, CuSO 4·5H 2O 0.3 mg/L, MnCl4·4H 2O 0.3 mg/L, ZnSO 4·7H 2O 0.2 mg/L, H3BO3·2H 2O 0.3 mg/L) [ 6]을 주입하였다. 최적의 충전율을 확인하고자 충전율 10%, 15%, 20%에 따른 질산화 및 탈질 효율을 분석하고자 2 L 정방향 아크릴 반응조에서 batch 형태로 실시하였다. 질산화 반응의 경우 알칼리도가 중요한 영향인자로 알려져 있기 때문에[ 7] 반응 초기부터 NaHCO 3를 이용하여 충분하게 반응(NH 4+-N Conc. × 7.14 mg/L as CaCO 3) 해주었다.
2.3. 질산화 및 탈질반응 속도 실험
반응속도 실험도 J 물재생센터 3처리장 1차침전지 유입수(통합반류수)를 채취하여 50 μm mesh로 거른 후 사용하였으며 원수 성상은 Table 2와 같다. 실험은 2 L의 정방향 아크릴 반응조를 이용하여 batch 형태로 실시하였으며 미생물 고정화 담체의 충전율은 15% (v/v%)로 진행하였다. 질산화 반응은 초기 NH 4+-N 농도 약 135 mg/L (TkN 농도 약 150 mg/L)로 시작하고 알칼리도의 경우 이론적인 값인 1,057 mg/L as CaCO 3 [ 8]보다 높은 1,580 mg/L as CaCO 3로 설정하여 1시간 간격으로 NH 4+-N, Alk, pH, NO 3--N를 측정하여 질산화 속도를 분석하였다. 탈질 반응은 질산화 반응이 끝난 원수를 사용하였으며 유기물 이외의 제한인자가 없으므로 glucose (C 6H 12O 6)를 이용하여 C/N비 7 이상으로 맞추어 진행하였으며, 1시간 간격으로 NO 3--N, COD Cr를 측정하였다. CODCr, T-N, T-P는 Standard Methods 20th에 준하여 실시하였으며, 이온항목인 NH4+-N, NO2--N, NO3--N는 시료를 채취한 후 즉시 여과지(GF/C)에 여과한 후 Spectrophotometric method (DR-2010 HACH USA)와 IC (HIC-20A SHIMADZU Japan)를 이용하여 분석하였다.
2.4. SEM/EDX 분석
미생물 고정화 담체는 담체 내부에서 미생물 성장이 이루어지기 때문에 미생물 성장 여부를 쉽게 판단하기 어렵다. 또한 수중의 유기물 및 영양염류 등이 담체 표면에서의 물질전달로 내부에 있는 미생물에 의해 제거되기 때문에 담체 표면의 두께 정도가 중요하다. 따라서 SEM/EDX 분석을 통하여 미생물 성장 여부 및 담체 표면을 HITACHI사의 SEM (Scanning Electron Microscope)을 이용하여 분석하였다.
3. 결과 및 고찰
3.1. 충전율에 따른 질산화 및 탈질 효율 결과
미생물 고정화 담체에 대한 최적의 충전율을 찾고자 질산화 및 탈질 효율을 분석한 결과, Fig. 1과 Fig. 2에 나타내었다. 질산화 미생물 고정화 담체의 경우 총 5시간까지 분석을 실시하였다. 5시간 후 최종 유출수 NH4+-N 농도는 충전율 10%일 때 8.30 mg/L, 15%는 7.28 mg/L, 20%는 5.42 mg/L로 나타났으며, 이때 제거율은 최대 90%를 나타냈다. 초기 1시간의 질산화 효율을 비교하면 10%는 14.57 mg/L인 반면 20%는 25.14 mg/L로 약 2배의 제거량 차이를 보였다.
탈질 미생물 고정화 담체는 충전율에 상관없이 총 3시간 만에 반응이 완료되었다. 특히 충전율 20%일 때 2시간 이내 NO 3--N 농도가 72 mg/L에서 0.5 mg/L까지 제거되었다. 충전율 10%보다 20%에서 초기 1시간 만에 약 2배 이상의 제거량 차이를 나타내어 질산화 미생물 고정화 담체와 유사한 결과를 보였으며, 이는 기존 미생물 고정화법의 연구[ 9]보다 낮은 충전율에서 높은 제거효율을 보였다. 질산화 및 탈질의 충전율에 따른 효율을 종합적으로 고려하면 15% 이상에서는 차이가 미미한 것을 확인하였다. 따라서 충전율은 미생물 고정화 담체의 양 즉, 경제성과 연관되므로 반응조의 체류시간을 고려하여 충전율을 선정해야하는 것으로 보인다.
3.2. 질산화 및 탈질반응 속도
질산화 및 탈질 반응속도 실험 결과는 다음 Fig. 3과 Fig. 4에 나타난 것과 같다. 초기 TkN 농도 148.14 mg/L에서 8시간 후 47.9 mg/L로 총 100.24 mg/L가 질산화 되었으며, 질산화 속도는 12.53 mg NH 4+-N/L·hr로 나타났다. 일반적인 질산화 속도는 3.93 mg NH 4+-N/L·hr [ 10]로 기존 공정보다 뛰어난 질산화 반응속도를 나타난 것을 확인할 수 있었다. 탈질 반응은 초기 127.6 mg NO 3--N/L에서 6시간 5.4 mg NO 3--N/L 짧은 시간에 완료되었다. 탈질 반응속도는 20.37 mg NO 3--N/L·hr로 질산화 반응과 마찬가지로 빠르게 나타났다. 단위시간당 질산화 및 탈질 반응 속도를 살펴보면 Table 3에 나타낸 바와 같이 시간이 지날수록 낮아졌다. 일반적인 감소곡선과 비슷하게 보였으나, 단위시간당 감소율은 매우 낮게 나타났다. 질산화 반응의 경우 2시간 간격으로 단위시간당 반응속도가 유사하였으며, 탈질반응은 초기 1시간을 제외하고 2, 3, 4시간에서 유사했다. 이러한 특징은 담체 표면에서의 물질 확산에 의한 것으로 판단된다.
3.3. SEM/EDX 분석 결과
미생물 고정화 담체의 내부 및 표면두께 그리고 미생물 성장여부를 측정하고자 미생물 고정화 전(고정화 X)ㆍ후(고정화 O)의 담체를 잘게 절단한 후 내부를 분석한 결과, Fig. 5에 나타난 바와 같다. 담체 표면의 두께는 약 10 μm로 매우 얇게 형성되었으며 Fig. 5(a)에서 보는 바와 같이 담체 내부는 기공 구성이 잘 형성되었다. 미생물 고정화를 진행할 경우 내부에 생성된 각 기공에 미생물이 부착 성장을 하게 된다.
Fig. 5(b)와 Fig. 5(c)를 살펴보면 미생물 고정화 후 담체 내부의 기공이 막히거나 이물질 즉, 미생물 군집이 형성된 것을 확인할 수 있다. 이는 Tulasi 등[ 11]이 제시한 SEM image와 유사하게 나타났으며, 미생물 고정화 담체(질산화용)에 대한 활성화 실험를 진행시 유기물 농도가 매우 낮은 합성 폐수를 사용하였으므로 단순한 유기물 덩어리가 아닌 미생물이 부착된 것으로 판단할 수 있다.
EDX분석을 통하여 담체의 C, H, O, N의 원소 비율을 분석한 결과, 미생물 고정화 전의 C와 N의 비율이 58.5%, 3.85%로 나타났으나 미생물 고정화 후의 비율을 보면 C는 70.75%, N은 7.69%로 증가한 것을 알 수 있다. 절대값이 아니므로 미생물을 정량화 할 수는 없지만 상대적인 수치인 것을 감안하면 미생물 고정화 담체의 미생물이 잘 부착되었다고 판단할 수 있다.( Fig. 6)
4. 결 론
기존 부착성장형 담체보다 향상된 기능을 가진 미생물 고정화 담체의 효과를 비교분석한 결과 다음과 같은 결론을 도출하였다.
1) 충전율 20%일 때, 질산화는 90%, 탈질은 99%의 최대 효율을 보였으며 초기 1시간 이내 제거량은 충전율 10%일 때보다 약 2배로 나타났다. 기존 공정과의 질산화 속도를 비교하면 약 3배 이상 빨랐으며, 탈질 속도 역시 20.37 mg NO3--N/L·hr로 나타났다. 따라서 동일조건하에 미생물 고정화 담체를 적용할 경우 처리시설 규모를 줄일 수 있다. 현장 적용시 HRT와 충전율(경제성)에 따라 시설규모 단축이나 높은 제거효율 확보 등의 다양한 이점을 확보할 것으로 보인다.
2) 미생물 고정화 전후의 담체를 SEM 이미지를 통하여 혼합․배양한 미생물이 담체 내부에 잘 부착된 것을 확인하였다. 그러나 SEM/EDX 분석의 한계점인 미생물에 대한 정량분석이 이루어지지 않아 향후 이 부분에 대한 추가 연구가 필요할 것으로 판단된다.
Acknowledgments
본 연구는 환경부 “글로벌탑 환경기술개발사업”으로 지원받은 과제임(과제번호 : 2016002190001).
Fig. 1.
Results of the filing rate analysis of the nitrification media. 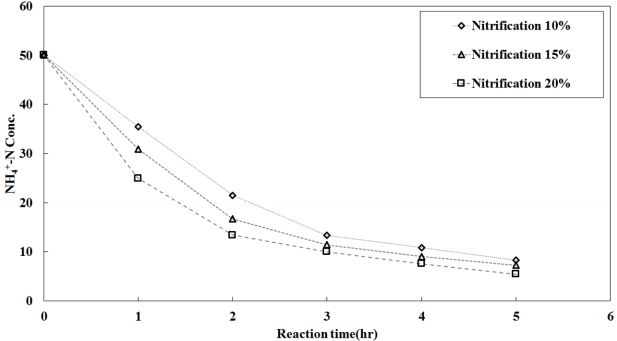
Fig. 2.
Results of the filing rate analysis of the denitrification media. 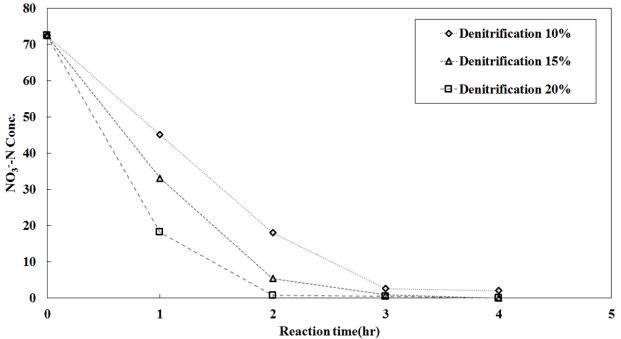
Fig. 3.
Results of the nitrification rate. 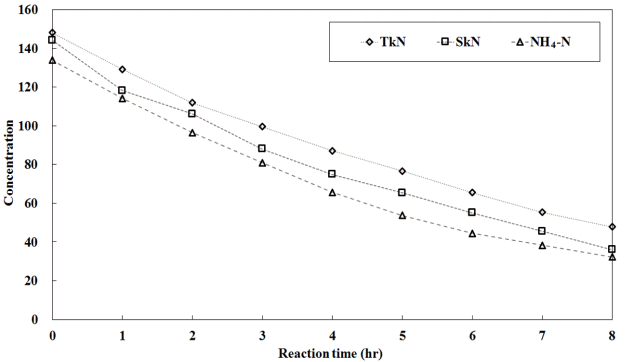
Fig. 4.
Results of the denitrification rate. 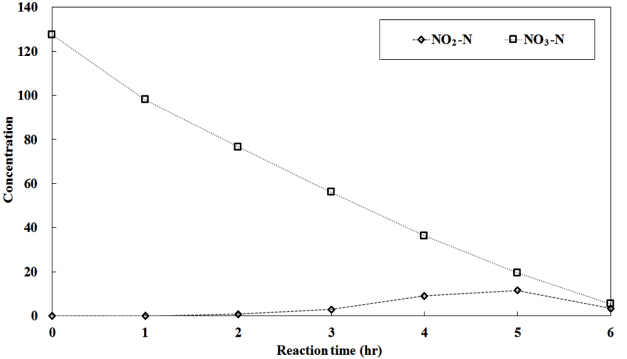
Fig. 5.
Media surface before and after microorganism immobilized. 
Fig. 6.
Results of EDX before and after microorganism immobilized. 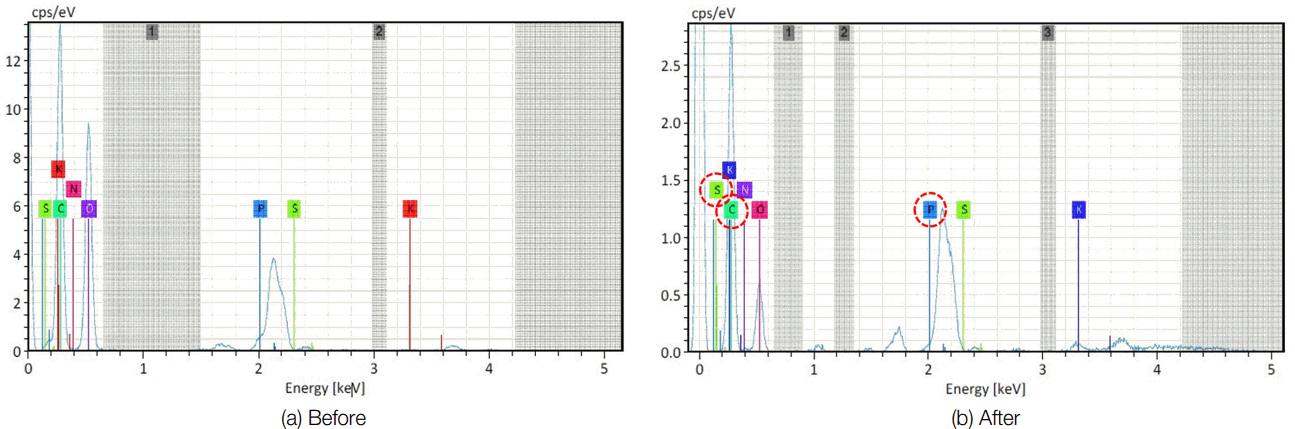
Table 1.
Composition of synthetic wastewater (unit : mg/L)
|
CODCr
|
T-N |
NH4+- |
NO2- |
NO3-- |
T-P |
TSS |
VSS |
|
N |
N |
N |
|
Nitrification wastewater |
4.3 |
57.78 |
50.09 |
3.0 |
4.69 |
7.840 |
- |
- |
|
Denitrification wastewater |
328.1 |
80.20 |
4.78 |
3.0 |
72.42 |
8.009 |
- |
- |
Table 2.
Composition of wastewater (unit : mg/L)
|
CODCr
|
T-N |
NH4+- |
NO2- |
NO3-- |
T-P |
Alk |
|
N |
N |
N |
|
Nitrification wastewater |
213.00 |
169.45 |
122.47 |
- |
- |
3.961 |
1,325 |
|
Denitrification wastewater |
174.97 |
141.03 |
- |
- |
127.60 |
2.572 |
|
Table 3.
Nitrification / denitrification rate change per unit time (unit : mg/L)
|
1 hr |
2 hr |
3 hr |
4 hr |
5 hr |
6 hr |
7 hr |
8 hr |
|
Nitrification rate |
18.92 |
17.23 |
12.31 |
12.48 |
10.57 |
11.07 |
10.02 |
7.46 |
|
Denitrification rate |
29.60 |
21.40 |
20.50 |
19.80 |
16.80 |
14.10 |
- |
- |
References
1. D.. Obaja, S.. Mace, J.. Costa, C.. Sans, J.. Mata-Alvarez, Nitrification, denitrification and biological phosphorus removal in piggery wastewater usinga sequencing batch reactor, Bioresour. Technol., 87, 103-111(2003).  2. W.. Wang, Y.. Ding, et al, Treatment of rich ammonia nitrogen wastewater with polyvinyl alcohol immobilized nitrifier biofortified constructed wetlands, Ecol. Eng., 94, 7-11(2016).  3. B. Y.. Tak, B. S.. Tak, Y. J.. Kim, Y. J.. Park, Y. H.. Yoon, G. H.. Min, Optimization ofcolor and COD removal from livestock wastewater by electrocoagulationprocess application of Box-Behnken design (BBD), J. Ind. Eng. Chem., 28, 307-315(2015).  4. J. Y.. Im, K. I.. Gil, Analysis on Nitrogen Faction of Influent Sewage in Domestic STP Based on Long-term Incubation Method, J. Wetlands Res., 19(2), 216-222(2017).
5. J. K.. Lee, H. W.. Park, et al, A study on the operating conditions for carbon-nitrogen removal in wastewater and sludge reduction using PVA-gel immobilized microorganisms, J. The Korean Soc. Water and Wastewater., 20(6), 875-883(2006).
6. F.. Mermillod-Blondin, et al, Use of slow filtration columns to assess oxygen respiration, consumption of dissolved organic carbon, nitrogen transformations, and microbial parameters in hyporheic sediments, Water Res., 39, 1687-1698(2005).  7. J. W.. Shanahan, M. J.. Semmens, Alkalinity and pH effects on nitrification in a membrane aerated bioreactor: An experimental and model analysis, Water Res., 74, 10-22(2015).  8. K. P.. Mahamalage, D. E.. James, T.. George, S.. Reza, Control of nitrification/denitrification in an onsite twochamber intermittently aerated membrane bioreactor with alkalinity and carbon addition: Model and experiment, Water Res., 115, 94-110(2017).  9. J. S.. Kim, S. J.. Kim, Improvement of activated sludge process by immobilized cell I, Korean Soc. Environ. Eng., 25(10), 1233-1237(2003).
10. G. T.. Jeong, S. H.. Park, et al, Effect of factors of nitrification process in wastewater treatment, The Korean Soc. Biotechnol. and Bioeng., 24(3), 296-302(2009).
11. V. K.. Tulasi, R.. Kadali, V. N.. Yarlagadda, M. S.. Pedapati, P. V.. and Vayalam, Nitrate removal from high strength nitrate-bearing wastes in granular sludge sequencing batch reactors, J. Biosci. and Bioeng., 121(2), 191-195(2016). 
|
|
















