미생물 고정화 담체 적용을 통한 통합 반류수 질소 처리
Treatment of Nitrogen in Recycle Water Using Immobilized Microbial Media
Article information
Abstract
하수처리장의 반류수 유입은 전체의 2∼5%로 적은 양이지만 고농도의 질소로 인하여 충격부하를 일으킬 수 있어 이를 감소시키기 위해 반류수 처리 계열을 따로 운전한다. 이때 장기폭기를 하여 암모니아성 질소를 질산성 질소로 산화하여 하수처리장으로 재유입한다. 질산화 과정에서 알칼리도를 소모하는데 고농도의 암모니아가 존재하는 반류수의 경우 알칼리도가 수중에 얼마나 존재하는지에 따라 질산화 반응이 이루어지는 정도가 결정된다. 하지만 반류수의 수중 알칼리도는 고농도의 암모니아를 100% 질산화하기에 부족하여 알칼리도를 추가로 주입하거나 생성하는 기작이 필요하다. 이에 따라 탈질 반응조를 호기조 전단에 두어 알칼리도 생성에 따른 질산화율을 향상시키고 T-N 제거율을 증가 시킬 수 있을 것으로 판단된다. 본 연구는 반류수를 대상으로 COD fraction 및 Nitrogen fraction 실험을 하여 질산화/탈질반응에 영향을 미치는 유기물 성상을 파악하고, 질산화/탈질 반응 속도를 증가시키고자 미생물 고정화 담체를 적용하여 반류수 중 질소의 효율적인 처리방법을 도출하고자 하였다. 반류수 중 분해 불가능한 용존성 COD는 37% 이상, 입자성 유기질소는 15% 이상으로 나타났고, 질산화・탈질 미생물 고정화 담체를 이용하였을 때 질산화반응속도는 9.34 mg/L・hr, 탈질반응속도는 48.4 mg/L・hr로 도출되었다.
Trans Abstract
The recycle water inflow of the sewage treatment plant is small at 2 to 5% of the total amount, but it may cause impact load due to the high concentration of nitrogen. In order to reduce impact load, recycle water treatment series are separately installed and a long-term aeration is carried out to oxidize ammonia nitrogen into nitric acid. The alkalinity of the recycle water is not sufficient to 100% nitrate the high concentration of ammonia, so that the addition of alkalinity or the generation mechanism is necessary. Therefore, it is considered that the denitrification tank can be placed at the front of the aeration tank to improve the nitrification rate and the T-N removal rate according to the alkalinity generation. The purpose of this study is to investigate the properties of organic materials that affect denitrification・nitrification reaction by COD fraction and nitrite fraction. Furthermore, in order to improve the rate of denitrification·nitrification reaction, this study derives the efficient treatment of recycle water by applying immobilized microbial media. Non-degradable dissolved COD in recycle water was more than 37% and particulate organic nitrogen was more than 15%, nitrification rate was 9.34 mg/L・hr and denitrification rate was 48.4 mg/L・hr.
1. 서 론
우리나라의 강이나 호소 수에서 쉽게 접할 수 있는 녹조 현상은 수년 동안 꼭 해결해야 할 환경오염 문제로 대두되어왔고, 원인물질인 질소(N)와 인(P)의 영양염류는 하수처리장에서 수계로 배출되어 부영양화를 일으키는 것으로부터 기인한다. 인의 경우 응집제를 적용한 물리・화학적 처리가 가능하여 현재는 안정적인 단계에 이르렀지만[1,2] 질소는 유기물과도 직접적인 관련이 있어[3] 물리화학적 처리가 어려워 생물학적 처리를 하고 있음에도[4] 완전하게 제어가 되지 않아 현재에도 많은 연구가 진행되고 있다. 또한 하수처리 시 필연적으로 발생하는 반류수가 하수처리장 유입수에 합류될 경우 2∼5% 미만으로 적은 양이지만 질소의 농도가 높기 때문에 반류수에 의한 유입수의 질소 부하 증가량은 총 유입 질소 부하량의 15∼25% 이상으로 수처리 계통에 충격 부하를 유발한다[5,6]. 따라서 반류수 중 질소를 별도로 처리하여 방류수 수질을 개선하는 방법으로 활성슬러지를 이용한 장기 폭기법을 주로 사용하지만 하수처리장에 따라 질산화에 필요한 영향인자가 다르고 생물학적으로 분해 불가능한 유기물이 존재하기 때문에[7] 미생물의 농도 및 조건을 반류수의 성상에 따라 조절해야 할 것이다. 이에 따라 질산화・탈질 반응에 관여하는 미생물을 분리・배양하여 직접적으로 투입하는 공법으로 Anammox 공법[8], Sharon 공법[9,10], 아질산화-아탈질 공법 등 적용되고 있다. 하지만 미생물 배양에 따른 시간 소비 및 미생물 유실 때문에 일반 생물학적 처리 공정에 범용적으로 적용하기에 어려워 SBR공정에만 적용되고 있는 실정이다[11]. 미생물 유실 방지 및 고농도로 유지할 수 있는 미생물고정화법을 하・폐수처리에 응용하는 연구가 1960년 후반부터 시작되었고[12] 활성슬러지의 복합미생물 및 질산화/탈질에 관여하는 특정 미생물을 고정화시켜 담체를 개발하는 연구가 많이 되고 있으나 대부분 특성 연구 및 일반 하수처리 적용에 국한되어 있고 실제 반류수를 적용한 연구는 미미하다[13~16]. 따라서 본 연구는 COD fraction으로 반류수의 유기물 성상을 파악하고 하・폐수처리에 주종을 이루는 질산화 및 탈질 미생물을 고정화한 담체를 적용하여 고농도 질소 및 난분해성 유기물이 다수 거동하는 반류수 처리의 적용성을 평가하고자 한다.
2. 실험 방법
2.1. 미생물 고정화 담체
질소제거율을 증가하기 위하여 질산화/탈질 반응에 직접적으로 관여하는 질산화 미생물(Nitrobacter sp., Nitrosomonas europaea)과 탈질 미생물(Paracoccus sp. Pseudomonas sp.)을 각각 분리 배양하여 질산화 미생물 고정화 담체(질산화 담체)・탈질 미생물 고정화 담체(탈질 담체)로 분리하여 고정화하였다. 담체는 PVA-PEG 재질의 boric acid 가교를 거친 포괄고정화법으로 3∼5 ㎜ 사이즈로 제조하였다[17].
2.2. 유기물 성상 분석
대상 원수는 서울시 A하수처리장의 농축조, 소화조, 탈수조 및 분뇨정화조 상등액을 합한 통합반류수로 1차 침전을 거친 폐수이고, 유기물의 산화 및 탈질기작에서 미생물에 의한 분해가 가능한 유기물 성상을 알기 위하여 Respirometer (Model: EZ-Owyro)를 사용하여 F/M비 0.05조건으로 호기조 슬러지 적당량을 500 mL 밀폐용기에 넣고 질산화에 의하여 DO가 소모되는 것을 방지하기 위하여 allylthiourea(ATU)를 주입하였다. 24시간 동안 미생물의 산소 호흡률(OUR, Oxygen Utilization Rate)을 측정하여 ∆OSS (readily biodegradable COD 영역) 및 ∆OSH (rapidly hydrolysable COD 영역)를 구하였다[18]. COD fraction 실험은 반류수와 활성슬러지를 적당한 비율로 넣어 24시간 동안 시간에 따른 TCOD, SCOD 농도를 측정하여 유기물의 SI (soluble inert COD, 용존 난분해성)를 측정하였다. ∆SCOD와 ∆BCOD을 이용한 (식 1)에 대입하여 YH 구한 후 (식 2) (식 3)를 이용하여 SS (readily biodegradable COD, 용존 생분해성), SH (rapidly hydrolysable COD, 용존 가수분해) 및 SP (soluble inert microbial products, 난분해성 생성물)를 계산하였다. Nitrogen fraction은 위의 COD Fraction 실험과정에서 TKN, NH3-N을 24시간 동안 1시간 단위로 측정하여 SNI (soluble inert organic nitrogen, 분해되지 않는 용존 유기 질소)를 구하고, (식 4)로 SND(readily biodegradable organic nitrogen, 쉽게 분해되는 용존 유기 질소), XND(slowly biodegradable particulate nitrogen, 천천히 분해되는 입자성 유기질소), XNI(particulate inert organic nitrogen, 분해되지 않는 입자성 유기 질소)를 계산하였다[3].
2.3. 질산화・탈질 회분식 실험
반응속도 실험을 위하여 Fig. 1의 모식도와 같이 반류수를 원수로 하여 4 L 질산화 반응조에 활성슬러지 1.5 L 와 질산화 담체 20% (v/v)를 각각 넣고 시간에 따른 NH3-N 제거율을 측정하였다. 질산화 반응이 완료된 후 원수에 탈질 미생물고정화 담체 20% (v/v)를 넣어 무산소조건에서 탈질율을 실험하였다. 질산화 반응조에는 질산화 반응시 소모되는 알칼리도를 보충하기 위해 NaHCO3 (NH4+-N Conc. × 7.14 ㎎/L as CaCO3) 를 주입하였고, 탈질 반응조에는 유입수의 낮은 COD를 보완하기 위하여 외부탄소원으로 에탄올을 사용하여 C/N비 4의 비율로 주입하였다. 온도와 교반 강도는 25℃, 90 rpm으로 동일 하였고 호기조는 산기관을 설치하여 DO 2 ㎎/L 이상으로 폭기 하였다. 본 실험의 모든 분석은 수질오염공정시험법 및 Standard method에 의거하였다.
3. 결과 및 고찰
3.1. 반류수 특성
3.1.1. COD fraction
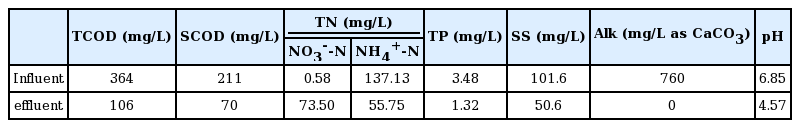
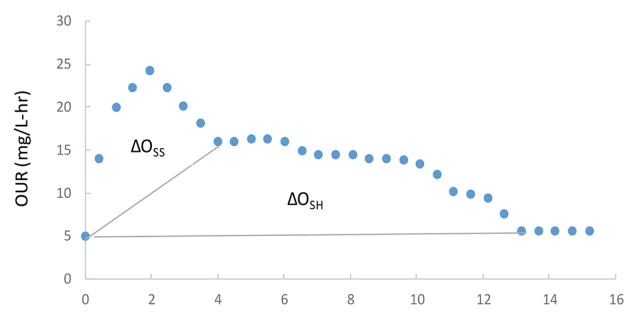
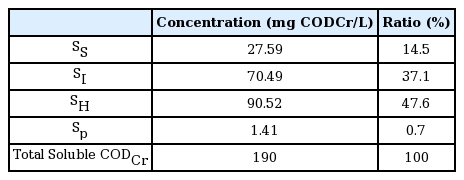
본 연구에서 사용된 A하수처리장 반류수 처리계열의 유입 및 유출수 농도는 아래 Table 1에 나타내었다. SCOD의 유입 농도는 211 ㎎/L이고 유출수는 70 mg/L로 약 33% 난분해성 COD가 거동하는 것으로 나타났고 이는 본 실험에서 도출된 SI 측정값과 유사하였다. NO3-N 농도는 0.58 ㎎/L에서 73.50 ㎎/L로 NH3-N의 50%가 질산화되었지만 TN의 유입수와 유출수의 농도는 변화가 없었다. 이에 따라 반류수 계열의 기존 처리방식은 질산화율을 높여 유입수의 질소 부하는 경감할 수 있지만 질소 제거는 어려운 것으로 사료된다. Fig. 2는 유입수 OUR을 분석한 결과로 곡선은 2단계로 구분된다[18]. 첫 번째는 OUR값이 크게 증가하는 구간으로 빠르게 분해되는 SS에 의한 ∆OSS로 나타내었고 두 번째 구간은 완만하게 감소하는 영역으로 천천히 가수분해 되는 단계인 ∆OSH (SH)로 나타내었다. 이에 따른 ∆OSS, ∆OSH 영역의 값은 각 16, 52.5로 계산되었다. YH를 구하기 위하여 SCOD와 BCOD의 변화량을 측정하였고 SCOD는 -8.83, BCOD는 3.80으로 YH 0.42 gcellCOD(gCOD)-1 값이 도출되었다. (식 2)에 의하여 SS 27.6 ㎎/L, SH 90.52 ㎎/L로 계산되었다. 반류수 COD Fraction 실험을 통하여 총 SCOD 190 ㎎/L중 분해 불가능한 유기물(SI)은 70.5 ㎎/L로 37.1%에 해당하였고, 쉽게 분해되는 유기물(SS)은 14.5%, 천천히 가수분해 되는 유기물(SH)은 47.6%로 나타났다(Table 2). 선행 연구에 따르면 일반 하수에서 SI는 5∼9% 로 존재하고[7,19], 반류수 중 소화 상등액 SI는 70%, 통합 반류수 SI는 32% 존재하는 것으로 보고되었다[6]. 본 연구에서 사용된 통합 반류수의 SI는 37.1%로 일반 하수보다 높은 것을 확인하였고, 분해 불가능한 유기물 제거 기작이 추가로 적용되어야 COD 방류수 수질기준에 만족할 수 있을 것으로 판단된다.
3.1.2. Nitrogen fraction
Table 3과 같이 초기 TKN, Soluble TKN(STKN)과 Soluble NH3-N(SNH)농도는 각각 136 ㎎/L, 113.22 ㎎/L, 103.36 ㎎/L이었고, 24시간 반응 후 Soluble TKN 과 Soluble NH3-N 농도는 각 48.02 ㎎/L, 47 ㎎/L로 측정되었다. 초기 SNI는 9.86 ㎎/L이고, 24시간 후 SNI는 1.1 ㎎/L, SND는 8.8 ㎎/L로 도출되었다. (식 4)에 대입하여 XNI 10.93 ㎎/L, XND 11.85 ㎎/L로 계산되었고, 유기질소는 32.64 ㎎/L로 총 질소의 24%에 해당하였다. 유기질소는 탄소성 유기물을 산화하여 암모니아로 산화하기 때문에[20,21] 유기질소를 제거하기 위해서는 분해 가능한 유기물이 충분히 존재해야 하고, 향후 총 질소 방류수 기준이 강화될 경우를 대비하여 총 질소의 24%에 해당하는 유기질소의 제거에도 관심을 기울여야 할 것으로 사료된다.
3.2. 질산화 및 탈질 반응 속도
3.2.1. 질산화 반응
반류수를 대상으로 질산화 담체와 활성슬러지를 적용한 반응조의 NH3-N 농도를 40시간 동안 1시간 간격으로 측정하였다. Fig. 3과 같이 담체를 적용한 질산화반응의 초기 NH3-N 농도는 128.3 ㎎/L이고 8시간 후 74.8 ㎎/L가 제거되어 질산화 속도는 평균 9.35 ㎎/L・hr로 나타났다. 활성슬러지를 적용한 질산화반응의 초기 NH3-N 농도는 90.5 ㎎/L로 분석되었는데 초기 농도가 담체 반응조보다 낮은 이유는 활성슬러지 식종에 의하여 희석된 것으로 예상되었다. 활성화 슬러지 반응 8시간 후 NH3-N농도는 56.6 ㎎/L로 총 33.9 ㎎/L가 제거되었고 평균 4.24 ㎎/L・hr의 제거율로 질산화 담체를 이용한 질산화 속도에 비하여 2배 이상 낮게 나타났다. 선행연구에서 활성슬러지를 이용한 질산화율(4 ㎎/L・hr 이하)과 비교하여도 본 연구의 질산화 담체를 통한 질산화율이 2배 이상 높은 것을 알 수 있다[22]. 두 실험 모두 8시간 이후부터 20시간까지 NH3-N의 농도의 변화가 없어 질산화반응이 정지되었다고 판단하고 알칼리도를 추가로 주입하였다. 알칼리도를 주입한 지 5시간째 질산화 담체 반응조의 NH3-N은 모두 제거되었고, 활성슬러지 반응조의 NH3-N은 20 ㎎/L 제거되지 않았다. 반류수에 존재하는 알칼리도는 질산화 반응에 평균 8.5 ㎎/L・hr as CaCO3로 약 8시간 동안 소모 되었고, 그 이후 알칼리도는 10 ㎎/L as CaCO3 이하로 감소하여 질산화 반응이 일어나지 않았다. 즉 반류수와 같이 고농도의 암모니아 질산화를 위해서는 알칼리도 생성을 하는 탈질 반응이 없는 경우 알칼리도 소모량을 계산하여 추가로 주입해야 할 것으로 사료된다.
3.2.2. 탈질 반응
3.2.1절에서 질산화 반응을 거친 실 폐수를 탈질 담체가 충전된 4 L 무산소조에 채운 후 시간에 따른 NO3-N, COD를 분석한 결과 Fig. 4(a)와 같이 NO3-N 초기 농도는 142.2 ㎎/L, 8시간동안 반응 후 농도는 85.0 ㎎/L로 약 41% 제거되었다. 초기 8시간 동안의 탈질 속도는 7.15 ㎎/L・h 이였지만 그 후 32시간 동안 NO3-N 제거율은 점차 감소하는 경향을 보였고 이때 원수 내 존재하는 C/N비는 약 1로 확인되었다. Fig. 4(b)는 반응 초기부터 외부탄소원을 C/N비 4이상으로 주입하여 NO3-N 농도를 분석하였는데, 그 결과 탈질 속도는 평균 48.4 ㎎/L・h로 외부탄소원을 주입하지 않았을 때보다 6배 이상 증가하였고 5시간 만에 탈질 반응이 100% 일어났다. 탈질반응에 필요한 외부탄소원을 추가로 주입할 때 약품비가 발생하지만 탈질 속도 증가 및 제거효율 향상에 따라 부지・시설을 축소할 수 있어 경제적인 측면에서 이점이 있다고 사료된다.
4. 결 론
반류수에 존재하는 유기물 중 분해가 가능한 유기물은 SS 14.5%, SH 47.6%로 일반 하수에 비하여 낮게 나타났고, 분해 불가능한 유기물은 37.1%로 높게 나타났다. 총 질소 중 유기질소가 24%, 그 중 입자성 유기질소가 69.8%, 용존성 유기질소가 30.2%로 입자성 유기질소 비율이 더 높았다. 유기질소를 암모니아로 산화하기 위해 유기탄소원이 필요하지만 반류수 내에 유기탄소는 분해 불가능한 성분이 높아 외부탄소원 주입을 고려해야 한다. 반류수 내 고농도 질소제거를 위하여 질산화・탈질미생물 고정화담체를 적용하였을 때, 질산화 반응의 경우 질산화 속도가 10.7 ㎎/L・hr로 일반 활성슬러지보다 2배 이상 높았다. 하지만 수중 알칼리도가 다 소모된 후 질산화반응이 일어나지 않았고 알칼리도를 추가 주입 한 후 질산화 반응이 다시 이루어진 것으로 보아 알칼리도 추가 주입 및 생성 기작이 필요한 것으로 사료된다. 알칼리도 생성 기작으로 탈질반응조를 질산화조 전 단에 설치하는 것을 가정하여 탈질 미생물 고정화 담체를 적용한 탈질 실험한 결과 외부탄소원을 주입하지 않았을 때 탈질 속도는 8.02 ㎎/L・hr로 나타났고, 외부탄소원을 주입했을 때는 평균 48.4 ㎎/L・hr로 6배 이상 증가하였다. 이와 같이 탈질기작을 추가한다면 알칼리도 생성에 따른 질산화율을 향상시키고, T-N 제거율을 증가하여 질소의 충격 부하를 효율적으로 저감시킬 수 있을 것으로 판단된다.
Acknowledgements
본 논문은 2018년도 서울시립대학교 연구년교수 연구비에 의하여 연구되었음.