1. 서 론
IPCC (intergovernmental panel on climate change)는 이산화탄소 저감을 위한 CCS (carbon capture and storage)기술로 연소 후 포집법인 흡수법과 흡착법을 제안하였다[1]. 흡수법과 흡착법은 각각의 장단점이 있으나 장치 구조의 간결성, 흡착제의 재생성 등으로 인하여 흡착법에 대한 연구도 많이 진행되고 있다[2~4].
100℃ 이상의 연돌가스에서 이산화탄소의 흡착 포집을 위해 고온에서도 흡착 가능한 흡착제에 대한 연구가 매우 필요한 실정이다. 일반적으로 제올라이트는 극성분자의 친화도가 매우 높아 이산화탄소의 흡착제로 많이 사용되며 흡착가스의 탈착과정에서 온도와 압력조절이 용이한 물질이다. Park 등[5]은 제올라이트와 활성탄을 이용하여 이산화탄소 흡착실험을 수행 하였으며 이 중 제올라이트가 우수한 흡착 능을 가지는 것으로 나타난 것으로 보고하였다. 이산화탄소 흡착은 주로 물리적 흡착 기전에 의해 이루어지나 일정온도 이상에서는 이산화탄소의 흡착능이 낮아지고 선택성에 문제가 있다고 보고하고 있다[6]. 따라서 연돌가스와 같은 고온상태에서 이산화탄소를 흡착 및 포집하기 위해서는 물리적 흡착 외에 화학적 흡착이 필요하다. 화학적 흡착을 증가하기 위해 주로 아민계 물질을 함침하여 이산화탄소의 흡착효과를 증대시킨다.
대표적인 아민계 물질은 monoethanolamine (MEA), ethylenediamine (EDA), polyethylenimine (PEI) 등이 있고 이들 물질을 활성탄, 제올라이트 등에 함침하는 방법을 사용하며 특히 실리카는 아민류의 함침이 잘 일어나도록 하는 장점을 가진다[7]. 아미노 그룹을 실리케이트나 알루미노실리케이트 표면에 개질화하여 이산화탄소의 흡착능을 개선하는 많은 연구가 진행되어 왔다. Lee 등[8]은 ZSM5형 제올라이트에 PEI를 함침하여 이산화탄소의 흡착능을 약 1.7배 이상 증가시켰으며 제올라이트 13X에 MEA를 함침하여 이산화탄소의 흡착점을 증가시키는 연구를 수행하였다[9]. 또한 Hong 등[10]은 제올라이트 13X에 MEA와 piperazine (PZ)의 함량을 달리하여 이산화탄소의 분리 특성을 연구한 결과 아민 함침 제올라이트의 경우 온도의 증가에 따라 흡착능은 감소하며 흡착온도 50℃에 PZ함침 제올라이트가 1.8배, MEA가 함침된 제올라이트는 20배 이상 흡착능이 증가 한다고 보고하였다. 또한 Jadhav 등[11]은 아민류로 개질화한 제올라이트 13X로 이산화탄소의 흡착능을 개선하였으며 물리적, 화학적 흡착이 이루어진다고 보고하였다.
이산화탄소의 물리·화학적 흡착연구에서 흡착제와 아민계 함침물질의 선정은 매우 중요하다. 특정 흡착제에 아민 물질 간 비교 연구가 많이 진행되어 왔으나 흡착제 간 비교 연구는 부족한 실정이다. 또한 동일 흡착제라도 함침조건, 분석조건에 따라 다른 결과를 도출할 수 있다. 따라서 본 연구에서는 MEA를 함침한 흡착제를 제조하여 동일 실험 조건 하에서 흡착제의 비교 연구를 실시하였다. 흡착제는 ZSM5와 MS13X로 선정하였으며 아민 함침 전·후의 이산화탄소 흡착효율과 표면특성을 비교 분석하였다.
2. 연구재료 및 방법
본 연구에서 사용한 ZSM5 (ACROS, Belgium) 및 Molecular sieve 13X (Fisher Chemical, U.K) 제품을 사용하였으며 ZSM5는 SiO2/Al2O3의 몰비가 400~570이고 파우더 형태였으며 Molecular sieve 13X의 SiO2/Al2O3는 2.6~3.0이었다. 화학적 흡착을 위한 아민계 물질은 순도 99% MEA (JUNSEI, J.P)을 선정하였으며 함침 방법은 Xu 등[12]의 방법을 이용하였다. 이 방법은 아민물질과 메탄올을 15분 교반한 다음 담체를 넣어 15분간 교반 후 함침된 담체를 진공오븐에서 70℃, 16시간 동안 건조 후 사용하였다. 이 방법은 건조 시 진공오븐을 사용함으로 공기와의 접촉시간을 줄이며 건조온도를 70℃로 유지함으로 함침 후 끓는점을 고려하여 아민계 물질의 휘발을 최소화 할 수 있다. 함침량은 30 wt%로 정하였고
함 침 량은 함 침 량 ( wt % ) = 아민의 량 ( g ) 흡 착 제 ( g ) + 아민의 량 ( g ) × 100
Autosorb-iQ & Quadrasorb SI (Quantachrome. U.S.A)를 이용하여 질소 흡·탈착 평가를 실시하였으며 비표면적, 기공 부피를 측정하였다. MEA가 함침된 흡착제인 ZSM5-MEA와 MS13X-MEA는 아민 물질의 휘발을 피하기 위해 343K의 온도에서 18시간 전처리를 하였으며 전처리 후 질소를 이용하여 흡·탈착 특성을 분석하였다. 다공성 물질의 결정구조를 분석하기 위해 XRD (x-ray diffractometer)는 D/max-2500 (Rigaku, J.P)으로 분석하였으며 각 흡착제에 함침된 아민기의 함침특성을 파악하기 위해 FT-IR (Fouier transform infrared spectroscopy)분석은 Frontier(PerkinElmer, U.S.A)를 이용하였다.
3. 결과 및 고찰
3.1. MEA를 함침한 ZSM5와 MS13X의 파과특성
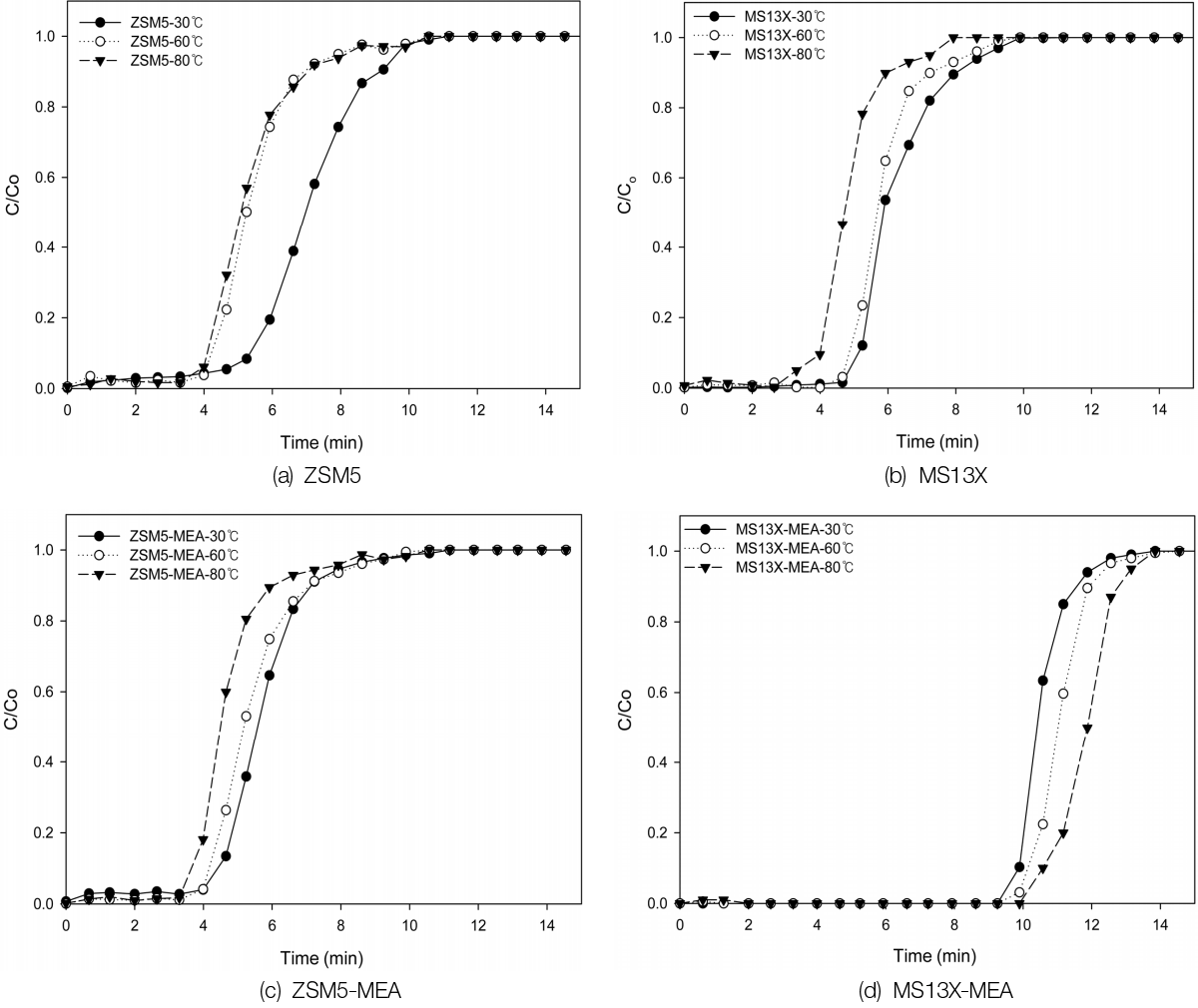
MEA를 함침한 ZSM5와 MS13X의 파과곡선을 Fig. 2에 나타내었다. 본 파과실험의 흡착온도는 30℃, 60℃, 80℃에서 실시하여 온도별 파과특성을 비교하였다. Co는 초기 이산화탄소농도이며 C는 t시간 흡착 후 이산화탄소의 농도를 나타낸다. Fig. 2(a)를 보면 MEA를 함침하지 않은 ZSM5는 4분 대에서 파과가 시작되었으며 온도별 비교 시 30℃에서 파과시간이 약 5.2분으로 이산화탄소의 흡착효율이 가장 높았다. 이는 ZSM5의 물리적 흡착에 기인한 것으로 물리적 흡착 시 온도가 낮을수록 흡착능은 커진다. 따라서 흡착온도가 가장 낮은 30℃에서 흡착능이 커져 파과시간이 길어졌다. 반면에 60℃와 80℃에서는 파과시간이 거의 동일하여 흡착효율의 차이가 없음을 보여주었다. Fig. 2(b)에서 MEA가 함침되지 않은 MS13X로 약 2.7분에서 4.6분대에서 파과가 시작되었으며 ZSM5와 유사한 파과경향을 보여 주었다. 즉 MEA가 함침되지 않은 ZSM5와 MS13X는 유사한 파과특성을 가져 이산화탄소의 흡착능의 차이가 거의 없음을 보여 주었다. Fig. 2(c)는 30 wt%의 MEA가 함침된 ZSM5로 각 흡착온도별 파과 경향이 오히려 MEA가 함침되지 않은 ZSM5에 비해 비슷하거나 오히려 낮아지는 경향을 보여주었다. Lee 등[7]의 연구에 따르면 PEI를 함침한 ZSM5가 함침하지 않은 ZSM5에 비해 이산화탄소의 흡착능은 높아졌으나 본 연구의 결과와는 일치하지 않았다. 이는 MEA 함침 후 ZSM5의 비표면적의 감소로 물리적 흡착 현상이 일어나지 않고 흡착제 표면에 접촉할 수 있는 site가 없기 때문에 일부 화학적 흡착만 일어나 파과시간이 짧아져 흡착능이 감소된 것으로 사료된다. Fig. 2(d)는 30 wt%의 MEA를 함침한 MS13X로 흡착온도에 상관없이 10분 대에서 파과가 시작되었으며 30℃, 60℃, 80℃순으로 흡착효율이 증가됨을 보여 주었다. 이는 MS13X-MEA의 경우 아민기에 의해 이산화탄소의 화학적 흡착능이 증가되어 80℃의 고온에서도 이산화탄소의 흡착능이 증가됨을 보여주었다. 일반적으로 아민기와 이산화탄소의 반응기전은 다음과 같다.
3.2. MEA를 함침한 ZSM5와 MS13X의 흡착량 비교
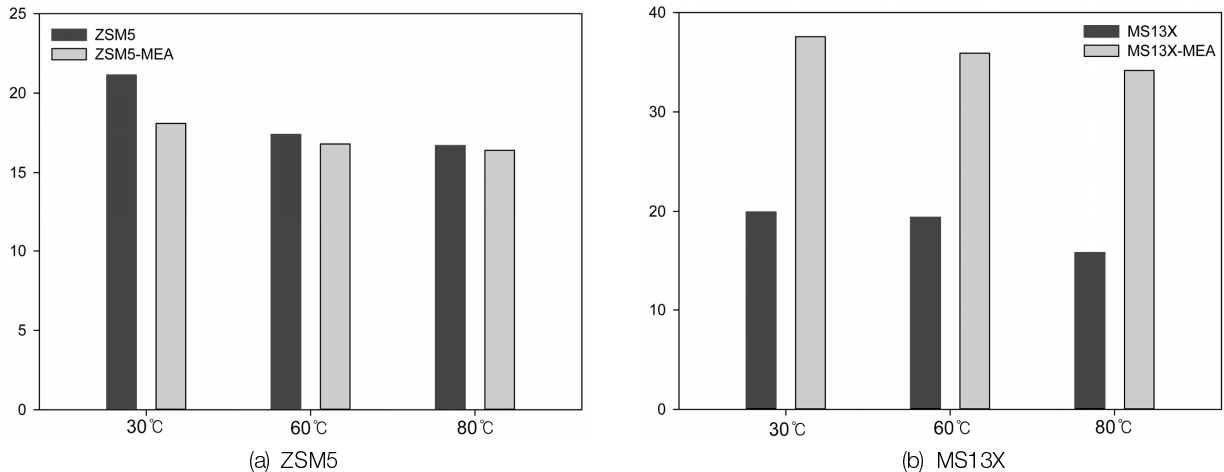
ZSM5와 MS13X의 CO2 흡착량과 MEA 30 wt%를 함침한 ZSM5와 MS13X의 CO2 흡착량을 Fig. 3에 나타내었다. CO2 흡착량의 계산은 q = 1 m ∫ 0 t Q × C i - C 0 d t
ZSM5의 CO2 흡착량은 흡착제 0.5 g 당 30℃에서 약 21.1 mg, 60℃에서 약 17.4 mg, 80℃에서 약 16.7 mg으로 상온에서 흡착량이 가장 높았으며 고온으로 갈수록 흡착량이 낮아졌다. ZSM5-MEA의 경우 30℃에서 약 18.1 mg, 60℃에서 약 16.8 mg, 80℃에서 약 16.4 mg으로 전체적인 경향은 ZSM5와 유사하였으며 MEA를 함침을 하였음에도 불구하고 흡착량의 차이를 보이지 않았으며 오히려 고온에서 약간 낮아지는 경향을 보여주었다. Lee 등[8]은 ZSM5에 PEI (polyethylenimine)를 함침하여 기공구조에 따른 이산화탄소의 흡착량을 평가하였다. 이 연구에서는 PEI가 함침된 ZSM5가 순수 ZSM5에 비해 이산화탄소의 흡착량이 높아진다고 하였으며 이는 PEI 내 아민그룹의 화학적 흡착에 기인한다고 하였다. 그러나 본 연구와는 상이한 결과를 보여주었는데 이는 함침물질과 SiO2/Al2O3의 몰비 차이로 사료된다. 특히 Frantz 등[13]의 연구에 따르면 제올라이트의 Si/Al 비가 작아질수록 이산화탄소 흡착효과가 높아진다고 하였다. 본 연구에 사용된 ZSM5는 몰비가 400정도로 매우 높아 이 영향으로 인해 이산화탄소의 흡착 효율이 감소된 것으로 생각된다.
MS13X의 CO2 흡착량은 30℃에서 약 19.93 mg, 60℃에서 약 19.4 mg, 80℃에서 약 15.7 mg으로 ZSM5와 유사한 경향을 보여주었으며 두 흡착제간의 CO2 흡착량의 차이는 거의 미비하였다. 반면에 MEA를 함침한 MS13X의 CO2 흡착량은 30℃에서 약 34.2 mg, 60℃에서 약 35.9 mg, 80℃에서 약 37.6 mg으로 MS13X에 비해 CO2 흡착량이 약 2배 이상 높아졌으며 흡착온도에 따른 차이는 보이지 않았다. 이는 함침된 MEA가 MS13X의 표면에서 효과적으로 그 기능을 나타내어 흡착능이 증가된 것으로 생각된다. 특히 흡착제 표면에 적절한 양의 MEA를 함침할 경우 함침하지 않은 흡착제에 비해 흡착제와 흡착물질 간의 새로운 상호작용이 발생되며 과량의 MEA는 기공을 완전히 막거나 표면 구조의 특성에 영향을 줄 수 있다고 보고하였다[9]. 특히 Chatti 등[14]은 아미노그룹이 제올라이트의 기공 내에서 용매의 역할을 하여 이 기공들이 이산화탄소의 포집을 위한 마이크로반응기와 같은 역할을 한다고 하였다. 아민으로 개질화된 흡착제의 반응기전은 이산화탄소와 액체 아민간의 반응기전은 동일하다고 하였으며 2 mol의 아민과 1 mol의 이산화탄소가 반응기전을 갖는다. 그러나 본 연구에서는 실험과정 중 물이 존재할 가능성은 낮음으로 형성된 카바메이트와 물의 반응기전은 일어나지 않을 것으로 생각된다.
즉 전체적인 기전은 고체 담체와 작용기를 이용하여 기상물질을 제어함으로 흡착기전이 맞으나 Chatti 등[14]의 제안처럼 작용기가 기공 내에 액상형태로 존재한다면 마이크로적 규모로 흡수현상이 일어난다고 볼 수 있다. 본 연구는 아민기가 화학적 흡착을 한다는 가정 하에서 이루어졌으나 만약 마이크로 규모의 흡수현상이 일어난다면 추후 연구에서 탈착 실험을 진행할 필요가 있을 것으로 사료된다.
3.3. MEA와 EDA 함침 MCM41의 표면분석결과
함침된 흡착제의 표면특성과 흡착효율 및 흡착량의 연관성을 분석하기 위해 BET, XRD, FT-IR분석을 실시하였다. Table 1은 흡착제별 비표면적과 기공부피를 나타내었다. ZSM5의 경우 약 230 m2 /g으로 Lee 등[8]의 합성 ZSM5의 271~328 m2 /g 및 Frantz 등[13]의 연구결과와 비교하여 유사한 비표면적을 나타내었다. 반면에 ZSM5-MEA의 경우 비표면적이 약 88 m2 /g으로 약 3배 이상 감소한 것으로 나타났다. 이는 ZSM5내 기공에 MEA가 함침되어 나타난 현상이며 기공부피 역시 크게 감소하였다. Lee 등[8]은 과잉의 아민 함침량은 ZSM5의 기공을 막음으로써 기공 내 확산을 막아 아민에 의한 효과가 감소한다고 하였다. 이러한 이유로 ZSM5-MEA가 아민을 함침하였음에도 불구하고 이산화탄소의 흡착 효율이 낮은 것으로 사료된다. 또한 Xu 등[15]의 연구에서 β-제올라이트에 MEA를 함침한 결과 비표면적은 574 m2 /g에서 15 m2 /g로 기공부피는 0.230 cm3 /g에서 0.074 cm3 /g로 감소하였으며, Hong 등[10]과 Chatti 등[14]의 연구에서는 제올라이트 13X에 30 wt%의 MEA와 50 wt%의 MEA를 함침한 결과 비표면적은 각각 613.5 m2 /g, 386.4 m2 /g에서 0.4 m2 /g, 14.9 m2 /g로 감소하였으며 기공부피는 각각 0.2935 cm3 /g, 0.2335 cm3 /g에서 3.19 × 10-4 cm3 /g, 0.0441 cm3 /g로 감소하였다고 보고하였다. 본 연구에서는 MEA 함침 전후의 MS13X의 비표면적은 718.335 m2 /g에서 19.945 m2 /g로 기공부피는 0.360 cm3 /g에서 0.099 cm3 /g로 감소함을 보여주어 선행 연구와 유사한 경향를 보여주었다. 특히 Bezerra 등[9], Hong 등[10]과 Chatti 등[15] 연구에서 아민의 함침량이 증가함으로서 비표면적과 기공부피는 점차 감소한다고 보고하였으며 이는 MEA가 미세기공을 채움으로 기공 내 질소의 접근이 제한되어 흡착을 방해하였기 때문이라고 설명하였다.
ZSM5와 MS13X 및 ZSM5-MEA와 MS13X-MEA의 N2 등온 흡·탈착곡선을 Fig. 4에 나타내었다. 두 흡착제 모두 P/Po가 0.1과 0.8 부근의 영역에서 기울기의 변화를 보이며 IUPAC의 분류에 따라 I형 등온선이 나타난다. 이는 각 흡착제의 모세관 응축현상으로 Bezerra 등[9] 및 Hong 등[10]의 연구와 유사한 결과를 보여 주었다. 또한 Frantz 등[13]이 ZSM5를 이용한 이산화탄소 흡착 연구에서 N2 흡·탈착곡선의 결과가 본 연구와 유사하였으며 다공성 구조의 H3형을 보여 주는 히스테리시스에 의해 확인할 수 있다고 하였다.
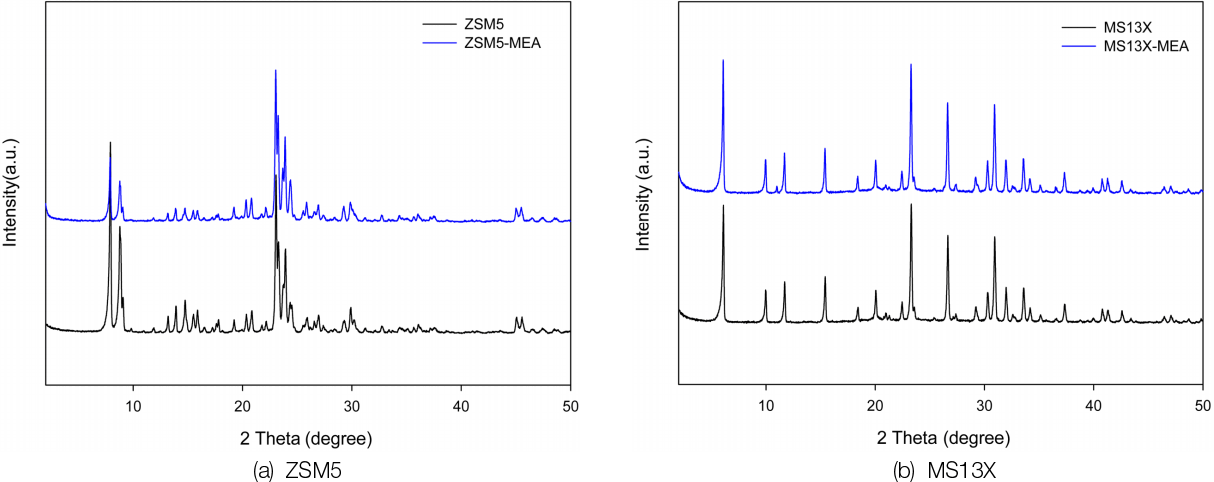
ZSM5와 MS13X 및 개질화된 흡착제의 XRD결과를 Fig. 5에 나타내었다. Frantz 등[12]의 연구에 따르면 ZSM5의 XRD피크 2 값은 7.9°, 8.9°, 23.13°, 23.8°와 24.8°에서 나타난다고 보고하였으며 본 연구에서도 7.9°, 8.7°, 23.04°, 23.89°, 24.37°에서 피크를 보여주어 전형적인 제올라이트의 XRD 패턴을 보여주었다. 특히 ZSM5나 MS13X의 MEA 함침 전후의 XRD 피크 패턴이 유사하였는데 이는 고함량의 MEA를 함침하였음에도 불구하고 제올라이트의 결정구조에 영향을 미치지 않음을 나타내며 함침과정이 결정화에 영향을 주지 않는다고 보고하였다[13]. 또한 Hong 등[10]은 아민류의 함침량을 30 wt%, 50 wt%, 70 wt% 증가함에 따라 XRD의 피크 감도가 낮아진다고 보고 하였으며 이는 함침량의 증가가 제올라이트의 피크를 상쇄시켜 감소된다고 하였다.
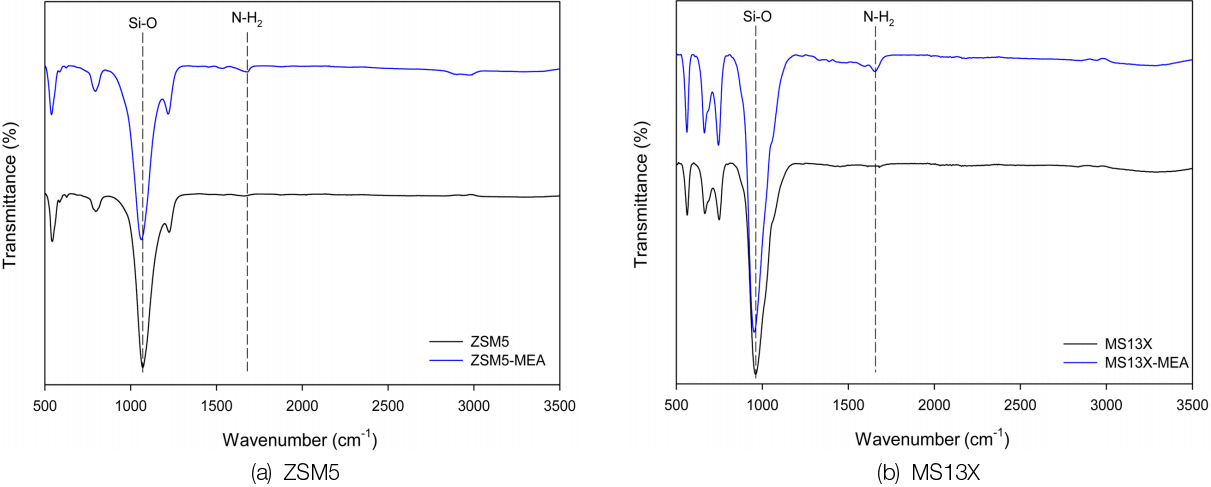
ZSM5 및 MS13X와 함침된 흡착제의 FT-IR 분석 결과를 Fig. 6에 나타내었다. ZSM5와 MS13X의 경우 950~1,060 cm-1 영역에서 Si-O의 대표피크가 나타났다. MEA를 함침한 경우 1,515~1,651 cm-1 영역에서 N-H2 밴드가 관찰되어 아민의 함침여부를 확인할 수 있었으며 Hong 등[10], Pham 등[16]의 논문과 유사한 흡수밴드 특성을 가졌다. Bezerra 등[9]에 따르면 아민류는 1,200에서 1,700 cm-1범위에서 나타난다고 하였다. Hong 등[10]은 3,278 cm-1에서 O-H alcohol피크가 2,934~2,874 cm-1 사이에서 C-H stretch피크가 1,648~1,581 cm-1에서 초기 N-H피크가 관찰되었다고 하였으며 MEA의 함침량이 증가함에 따라 FT-IR의 피크가 증가한다고 보고하였다. Frantz 등[13]에 따르면 ZSM5의 경우 450, 790, 1,080과 1,220 cm-1에서 SiO4 사면체 특성밴드가 나타나고 1220 cm-1에서 ZSM5의 구조 특성이 나타난다고 하였으며 550~450 cm-1의 흡수밴드가 ZSM5형 제올라이트의 특성이라고 보고하였다.
4. 결 론
본 연구에서는 이산화탄소 흡착을 위해 대표적인 아민계 물질인 MEA를 ZSM5와 MS13X에 함침하여 이산화탄소 흡착실험 및 표면분석을 실시한 결과 다음과 같은 결론을 얻었다.
첫째, 이산화탄소 흡착실험에서 ZSM5와 ZSM5-MEA는 함침 전 후의 차이가 나타나지 않았으며 MS13X는 함침된 MS13X-MEA의 흡착량이 2배 이상 증가하는 것으로 나타났다. 특히 MS13X-MEA의 경우 이산화탄소의 흡착량은 30℃에서 약 34.2 mg, 60℃에서 약 35.9 mg, 80℃에서 약 37.6 mg으로 온도의 증가에 따라 약간 증가하는 경향을 보여주었으나 흡착량의 차이 미비하였다. 둘째, BET 표면분석결과 두 흡착제 모두 함침 전후에 크게 차이나 MS13X는 718.335 m2 /g에서 MEA 함침 후 19.945 m2 /g으로 낮아졌으며 기공 부피 또한 0.360 cm3 /g에서 0.099 cm3 /g으로 감소하였다. XRD과 FT-IR의 분석 결과에서는 전형적인 ZSM5와 MS13X의 피크패턴을 보여 주었으며 함침된 흡착제의 경우 특별한 결정구조가 관찰되지 않았다.
본 연구에서 MS13X에 MEA를 함침한 흡착제가 이산화탄소 흡착에 효과적이었으며 60-80℃의 흡착온도 범위에서도 효과적으로 이산화탄소를 흡착하였다. 본 연구의 결과는 추후 CO2 흡착제 개발에 기초적 자료로 활용될 수 있을 것으로 기대된다.